早教吧作业答案频道 -->化学-->
实验中取5克矿石样品,将20克稀盐酸平均分成4次注入,测量并记录每次充分反应后装置C的质量(如表),求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2H
题目详情
实验中取5克矿石样品,将20克稀盐酸平均分成4次注入,测量并记录每次充分反应后装置C的质量(如表)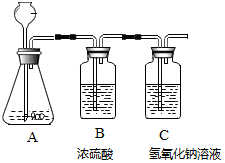 ,求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑)
,求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑)
 ,求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑)
,求出该矿石样品中碳酸钙的质量分数.(碳酸钙与盐酸反应的化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑) | 实验次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/克 | 5 | 5 | 5 | 5 |
| 充分反应后装置C的质量/克 | 150.52 | 151.04 | 151.56 | 151.76 |
▼优质解答
答案和解析
A装置是气体发生装置,B装置是气体干燥装置,C、装置是二氧化碳收集装置.所以C装置的质量增加量为吸收的二氧化碳的质量(忽略AB装置中残余的二氧化碳).
将数据加工如下:
可知生成的二氧化碳的质量为0.52g+0.52g+0.52g+0.2g=1.76g
设生成1.76g二氧化碳需要的碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 1.76g
=
x=4g
则石灰石样品中碳酸钙的质量分数为
×100%=80%
答:石灰石样品中碳酸钙的质量分数为80%
将数据加工如下:
| 实验次数 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量/克 | 5 | 5 | 5 | 5 |
| C装置的起始质量/克 | 150 | 150.52 | 151.04 | 151.56 |
| 充分反应后装置C的质量/克 | 150.52 | 151.04 | 151.56 | 151.76 |
| C装置的质量变化/克 | 推出0.52 | 0.52 | 0.52 | 0.2 |
设生成1.76g二氧化碳需要的碳酸钙的质量为x.
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 1.76g
| 100 |
| 44 |
| x |
| 1.76g |
x=4g
则石灰石样品中碳酸钙的质量分数为
| 4g |
| 5g |
答:石灰石样品中碳酸钙的质量分数为80%
看了 实验中取5克矿石样品,将20...的网友还看了以下:
某同学用刻度尺测得教室内黑板的长度为3.33,那么他这样记录的错误在于,正确的写法应该是.其中准确 2020-04-26 …
录入一份稿件,甲单独录入需要10小时,乙单独录入需要15小时,甲录入四小时后,剩下的由乙录入.录完 2020-05-15 …
一些依靠人工开凿的河道入海的河流,那么在人工河道开凿前它们是怎样入海的?举个例子:北京地区的潮白河 2020-06-05 …
希望小学测量五年级部分学生的身高,为方便起见,在记录时,以1.50米为标准,把1.52米,记+0. 2020-06-11 …
笑笑和淘气用电脑入同样字数的搞件,笑笑每分录入100个字,需要6分完成,淘气用8分钟录完这份稿件, 2020-06-28 …
1.用录音机录下一段自己的声音,和同学们一起听,你认为放出的声音和自己的一样吗,别的同学认为一样吗 2020-07-04 …
問幾個,浙江地理問題,根据成因,浙江境内的主要大河可分几类?浙江的天然大河是怎样入海的?为什么会这 2020-07-13 …
请先生告诉我怎样入定.我非常想入定,请先生介绍一下您的入定过程和经验,是怎样入定的,练了多长时间?末 2020-11-15 …
脚踏实地做凡人阅读答案给五分!本文开头列举了时下常见的几种现象,你认为这样入手的好处是什么? 2020-12-24 …
圆珠笔的长度为:14.0.这样记录的错误在于,正确写法应为. 2021-01-05 …