早教吧作业答案频道 -->化学-->
铜冶金技术以火法冶炼为主.(1)火法炼铜的工艺流程如下:反应Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1反应Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1①
题目详情
铜冶金技术以火法冶炼为主.
(1)火法炼铜的工艺流程如下:

反应Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1
反应Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1
①在反应Ⅱ中,每生成1mol SO2转移电子___mol.
②反应Cu2S(s)+O2(g)═2Cu(s)+SO2(g)的△H=___ kJ•mol-1.
③理论上m1:m2=___.
(2)炼铜的副产品SO2多用于制硫酸和石膏等化学产品.
①制硫酸中重要的一步反应是
2SO2(g)+O2(g)⇌2SO3(g)△H=-196kJ•mol-1.
图表示将2.0mol SO 2 和1.0mol O 2 置于1L密闭容器中,当其他条件一定时,SO2(g)的平衡转化率α随X的变化关系,X(X1、X2)代表压强或温度.
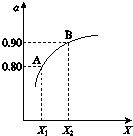
X代表的物理量是___.A对应条件下平衡常数K=___.
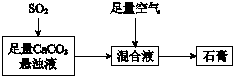
②下图表示的是生产石膏的简单流程,请用平衡移动原理解释向CaCO3悬浊液中通入SO 2发生反应的原因___.
(3)工业硫酸中往往含有一定量SO2,测定过程如下:取m g工业硫酸配成100mL溶液,取出20.00mL溶液,加入1mL指示剂,用c mol•L-1 I2标准溶液滴定,消耗的I2标准溶液V mL,工业硫酸中含有SO2的质量分数的计算式是___.
(1)火法炼铜的工艺流程如下:

反应Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1
反应Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1
①在反应Ⅱ中,每生成1mol SO2转移电子___mol.
②反应Cu2S(s)+O2(g)═2Cu(s)+SO2(g)的△H=___ kJ•mol-1.
③理论上m1:m2=___.
(2)炼铜的副产品SO2多用于制硫酸和石膏等化学产品.
①制硫酸中重要的一步反应是
2SO2(g)+O2(g)⇌2SO3(g)△H=-196kJ•mol-1.
图表示将2.0mol SO 2 和1.0mol O 2 置于1L密闭容器中,当其他条件一定时,SO2(g)的平衡转化率α随X的变化关系,X(X1、X2)代表压强或温度.

X代表的物理量是___.A对应条件下平衡常数K=___.
②下图表示的是生产石膏的简单流程,请用平衡移动原理解释向CaCO3悬浊液中通入SO 2发生反应的原因___.

(3)工业硫酸中往往含有一定量SO2,测定过程如下:取m g工业硫酸配成100mL溶液,取出20.00mL溶液,加入1mL指示剂,用c mol•L-1 I2标准溶液滴定,消耗的I2标准溶液V mL,工业硫酸中含有SO2的质量分数的计算式是___.
▼优质解答
答案和解析
(1)①2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g),硫由-2价变成+4价,所以生成1mol的二氧化硫转移6mol的电子,故答案为:6;
②根据盖斯定律,反应Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1,反应Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1,Cu2S(s)+O2(g)═2Cu(s)+SO2(g)的△H=
=
=-217.4kJ•mol-1,故答案为:-217.4;
③由反应Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g),反应Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)可知,反应Ⅰ生成2mol的氧化亚铜消耗2molCu2S,而2mol的氧化亚铜反应Ⅱ中消耗1mol的硫化亚铜,所以理论上m1:m2=2:1,故答案为:2:1;
(2)①2SO2(g)+O2(g)⇌2SO3(g)△H=-196kJ•mol-1,正反应是放热反应,所以升高温度平衡逆向移动,SO2(g)的平衡转化率α减小,而增大压强平衡正向移动,SO2(g)的平衡转化率α增大,所以X代表的物理量是压强;反应达平衡后,由图可知,SO2的平衡转化率α=0.80,参加反应的二氧化硫为2mol×80%=1.6mol,则:
2SO2(g)+O2(g)⇌2SO3(g)
开始(mol):2 1 0
变化(mol):1.6 0.8 1.6
平衡(mol):0.4 0.2 1.6
所以平衡时浓度:c(SO2)=0.4mol/L,c(O2)=0.2mol/L,c(SO3)=1.6mol/L,故平衡常数k=
=80,故答案为:压强;80;
②碳酸钙的悬浊液中存在溶解平衡,所以而通入二氧化硫与水反应生成亚硫酸酸性比碳酸的酸性强,所以CaCO3悬浊液中存在CaCO3(s)⇌Ca2+(aq)+CO32-(aq),通入SO2时,CO32- 与SO2反应,c(CO32-)减小,溶解平衡正向移动,故答案为:CaCO3悬浊液中存在CaCO3(s)⇌Ca2+(aq)+CO32-(aq),通入SO2时,CO32- 与SO2反应,c(CO32-)减小,溶解平衡正向移动;
(3)根据反应SO2 +I2 +2H2O=H2SO4+2HI,
1mol 1mol
n(SO2) cV×10-3
所以 n(SO2)=cV×10-3mol,则SO2的质量分数的计算式:
×100%=
×100%,故答案为:
×100%.
②根据盖斯定律,反应Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1,反应Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1,Cu2S(s)+O2(g)═2Cu(s)+SO2(g)的△H=
| △HⅠ+△HⅡ |
| 3 |
| 116-768.2 |
| 3 |
③由反应Ⅰ:2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g),反应Ⅱ:2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)可知,反应Ⅰ生成2mol的氧化亚铜消耗2molCu2S,而2mol的氧化亚铜反应Ⅱ中消耗1mol的硫化亚铜,所以理论上m1:m2=2:1,故答案为:2:1;
(2)①2SO2(g)+O2(g)⇌2SO3(g)△H=-196kJ•mol-1,正反应是放热反应,所以升高温度平衡逆向移动,SO2(g)的平衡转化率α减小,而增大压强平衡正向移动,SO2(g)的平衡转化率α增大,所以X代表的物理量是压强;反应达平衡后,由图可知,SO2的平衡转化率α=0.80,参加反应的二氧化硫为2mol×80%=1.6mol,则:
2SO2(g)+O2(g)⇌2SO3(g)
开始(mol):2 1 0
变化(mol):1.6 0.8 1.6
平衡(mol):0.4 0.2 1.6
所以平衡时浓度:c(SO2)=0.4mol/L,c(O2)=0.2mol/L,c(SO3)=1.6mol/L,故平衡常数k=
| 1.62 |
| 0.42×0.2 |
②碳酸钙的悬浊液中存在溶解平衡,所以而通入二氧化硫与水反应生成亚硫酸酸性比碳酸的酸性强,所以CaCO3悬浊液中存在CaCO3(s)⇌Ca2+(aq)+CO32-(aq),通入SO2时,CO32- 与SO2反应,c(CO32-)减小,溶解平衡正向移动,故答案为:CaCO3悬浊液中存在CaCO3(s)⇌Ca2+(aq)+CO32-(aq),通入SO2时,CO32- 与SO2反应,c(CO32-)减小,溶解平衡正向移动;
(3)根据反应SO2 +I2 +2H2O=H2SO4+2HI,
1mol 1mol
n(SO2) cV×10-3
所以 n(SO2)=cV×10-3mol,则SO2的质量分数的计算式:
cV×10-3mol×64g/mol×
| ||
| mg |
| 8cV |
| 25m |
| 8cV |
| 25m |
看了 铜冶金技术以火法冶炼为主.(...的网友还看了以下:
可以参考的公式是:s[1]=a[1];s[n]=s[n-1]>=0?s[n-1]+a[n]:a[n 2020-05-14 …
某垂线用五点法测得流速分别为V0.0=0.58m/s,V0.2=0.58m/s,V0.6=0.55m 2020-05-28 …
matlab解指数方程解不了啊ab怎么是0呢?s=solve('(a+b*0.720930233) 2020-08-02 …
这个程序运行减法的时候有错误.如果我从键盘输入一个负数就会出错.急#include#include# 2020-11-01 …
y''+y'+y=0作拉氏变换,(s^2+s+1)L(y)=0特征方程:s^2+s+1=0为什么是y 2020-11-08 …
甲、乙、丙、丁四人进行射击测试,每人10次射击成绩的平均数均是9.2环,方差分别为S甲2=0.56, 2020-11-30 …
甲、乙、丙、丁四个同学在三次阶段考试中数学成绩的方差分别为s甲2=0.12,s乙2=0.19,S丙2 2020-11-30 …
甲、乙、丙、丁四个同学在三次阶段考试中数学成绩的方差分别为s甲2=0.12,s乙2=0.19,S丙2 2020-11-30 …
甲、乙、丙、丁四人进行射击测试,每人10次射击成绩平均数均是9.2环,方差分别为S甲2=0.56,S 2020-11-30 …
判断一个化学反应的自发性常用焓判据和熵判据,则在下列情况下,可以判定反应一定自发进行的是()。A.Δ 2021-01-12 …