MgSO4·7H2O在医药上常用作泻药,工业上可用氯碱工业中的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和碳酸盐等成分。其主要工艺如下:
MgSO4 · 7H2O 在医药上常用作泻药,工业上可用氯碱工业中的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和碳酸盐等成分。其主要工艺如下:
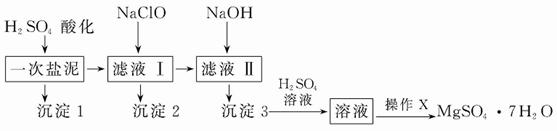
请回答下列问题:
( 1 )用 H2SO4 调节溶液 pH 至 1 ~ 2 , H2SO4 的作用是 ______________________ 。
( 2 )加 NaClO 溶液至 pH 为 5 ~ 6 并加热煮沸 5 分钟~ 10 分钟,沉淀 2 中主要含有 MnO2 和另外两种难溶物,这两种难溶物的化学式分别为 __________________ 、 ________________ ;其中 NaClO 溶液将 MnSO4 转化为 MnO2 的离子方程式为 ____
_____________________________________________________ 。
( 3 )检验滤液Ⅱ中是否含有 Fe3+ 的实验方法是 ________________________ 。
( 4 )“操作 X ”是将溶液 ____________________ 、 ____________________ 、过滤洗涤,即得到 MgSO4 · 7H2O 晶体。
【解析】( 1 )通过加入硫酸可以使一次盐泥中的镁、铁、铝、锰转化为可溶的硫酸盐,同时生成 CaSO4 和 H2SiO3 沉淀而除去。
( 2 ) ClO- 具有强氧化性,将 Mn2+ 转化为 MnO2 。其反应离子方程式为 Mn2++ClO-+H2O====MnO2 ↓ +Cl-+2H+ 。同时将 Fe2+ 转化为 Fe3+ ,其反应离子方程式为 2Fe2++ClO-+2H+====2Fe3++Cl-+H2O ,调节溶液的 pH 使 Fe(OH)3( 完全沉淀 pH ≥ 3.2) 、 Al(OH)3 沉淀 ( 完全沉淀 pH ≥ 3.2) ,分离出来。
( 3 )利用 Fe3+ 与 SCN- 形成特征颜色变化,或与苯酚显紫色等,现象明显,灵敏度高,可检验 Fe3+ 。
( 4 )对滤液蒸发浓缩,得到高浓度的 MgSO4 溶液,然后经冷却结晶即可得到 MgSO4 · 7H2O 晶体。
答案:( 1 )将一次盐泥中的碳酸盐和硅酸盐转化为可溶性的硫酸盐,同时生成硫酸钙和硅酸沉淀而除去
( 2 ) Al(OH)3 Fe(OH)3
Mn2++H2O+ClO-====MnO2 ↓ +Cl-+2H+
( 3 )取滤液Ⅱ 1 mL ~ 2 mL 于试管中,加入少量的 KSCN 溶液,若不显红色,证明滤液Ⅱ中无 Fe3+
( 4 )蒸发浓缩 冷却结晶
宝宝腹泻无小事 家长护理宝宝腹泻要避开常见误区 2020-03-30 …
用2000吨含氧化铁75%的赤铁矿石要炼出多少吨铁?1.用2000吨含氧化铁75%的赤铁矿石要炼出 2020-06-24 …
我国食盐有80%来自底下井盐和岩盐,用盐井水晒盐是制取食盐的常用方法.(1)除去盐水中泥土的操作是 2020-07-04 …
I、镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的.主要步骤如下:(1) 2020-07-08 …
‘开塞露“和高锰酸钾反应在家用“开塞露”(一种泻药,含甘油,不知是否含其它物质)与药用高锰酸钾反应 2020-07-10 …
10条春联的含义要春联及含义要含义含义含义含义含义含义.我是要交作业 2020-07-24 …
关于硬水的问题测知某净化后的天然水5000kg,煮沸后冷却得沉淀237g,冷却水中含MgSO4为84 2020-12-03 …
为什么人误服BaCl2溶液会中毒?医院里抢救此类中毒病人时给病人服用泻药(MgSO4),其原理是什么 2020-12-03 …
在海水晒盐中得到的粗盐中含有许多种杂质,主要是MgSO4、MgCl2、CaSO4,如何除去粗盐溶液中 2020-12-31 …
宝宝腹泻食谱介绍,腹泻要如何预防? 2021-04-03 …