早教吧作业答案频道 -->化学-->
某兴趣小组对碱式碳酸铜的分解产物进行探究.查阅资料①碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3△.
题目详情
某兴趣小组对碱式碳酸铜的分解产物进行探究.
【查阅资料】
①碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3
2CuO+H2O+CO2↑;
②白色的无水硫酸铜遇水会变成蓝色;
③CO还原CuO的实验过程中,固体产物可能有Cu2O(氧化亚铜,红色固体)、铜.
【实验验证】
验证碱式碳酸铜的分解产物,可选装置如下图所示.
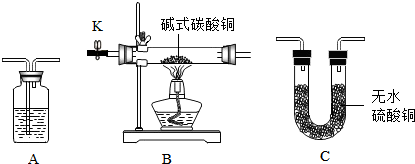
(1)上图装置A中盛放的试剂名称是___.
(2)甲同学将装置按___(填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
【拓展探究】
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分,实验装置如图:
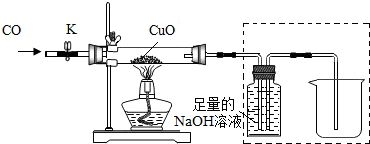
(1)实验过程:打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验数据
(3)实验结论:通过实验中获得的数据进行计算,得出红色固体粉末为(写名称)___
(4)表达交流:下列有关该实验的说法正确的是___.
A.该实验最好在通风橱中进行
B.先通入一会CO再加热是为了排净装置中的空气
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳
D.排入到烧杯中的溶液可能显碱性,也可能显中性.
223
2CuO+H2O+CO2↑;
②白色的无水硫酸铜遇水会变成蓝色;
③CO还原CuO的实验过程中,固体产物可能有Cu2O(氧化亚铜,红色固体)、铜.
【实验验证】
验证碱式碳酸铜的分解产物,可选装置如下图所示.

(1)上图装置A中盛放的试剂名称是___.
(2)甲同学将装置按___(填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
【拓展探究】
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分,实验装置如图:

(1)实验过程:打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验数据
(3)实验结论:通过实验中获得的数据进行计算,得出红色固体粉末为(写名称)___
(4)表达交流:下列有关该实验的说法正确的是___.
A.该实验最好在通风橱中进行
B.先通入一会CO再加热是为了排净装置中的空气
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳
D.排入到烧杯中的溶液可能显碱性,也可能显中性.
△ △ △ 22
2

实验步骤 观察到的现象 获得结论 有关反应的化学方程式 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡 ___ 黑色粉末均为氧化铜 ___ 实验步骤 观察到的现象 获得结论 有关反应的化学方程式 实验步骤 观察到的现象 获得结论 有关反应的化学方程式 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡 ___ 黑色粉末均为氧化铜 ___ 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡 ___ 黑色粉末均为氧化铜 ___

反应前 反应后 玻璃管和内盛氧化铜粉末的总质量为62.0g 玻璃管和内盛红色粉末的总质量为61.7 玻璃管的总质量为60.0g 反应前 反应后 反应前 反应后 玻璃管和内盛氧化铜粉末的总质量为62.0g 玻璃管和内盛红色粉末的总质量为61.7 玻璃管和内盛氧化铜粉末的总质量为62.0g 玻璃管和内盛红色粉末的总质量为61.7 玻璃管的总质量为60.0g 玻璃管的总质量为60.0g
【查阅资料】
①碱式碳酸铜受热分解的化学方程式为:Cu2(OH)2CO3
| ||
②白色的无水硫酸铜遇水会变成蓝色;
③CO还原CuO的实验过程中,固体产物可能有Cu2O(氧化亚铜,红色固体)、铜.
【实验验证】
验证碱式碳酸铜的分解产物,可选装置如下图所示.

(1)上图装置A中盛放的试剂名称是___.
(2)甲同学将装置按___(填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
| 实验步骤 | 观察到的现象 | 获得结论 | 有关反应的化学方程式 |
| 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡 | ___ | 黑色粉末均为氧化铜 | ___ |
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分,实验装置如图:

(1)实验过程:打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验数据
| 反应前 | 反应后 |
| 玻璃管和内盛氧化铜粉末的总质量为62.0g | 玻璃管和内盛红色粉末的总质量为61.7 |
| 玻璃管的总质量为60.0g | |
(4)表达交流:下列有关该实验的说法正确的是___.
A.该实验最好在通风橱中进行
B.先通入一会CO再加热是为了排净装置中的空气
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳
D.排入到烧杯中的溶液可能显碱性,也可能显中性.
223
| ||
②白色的无水硫酸铜遇水会变成蓝色;
③CO还原CuO的实验过程中,固体产物可能有Cu2O(氧化亚铜,红色固体)、铜.
【实验验证】
验证碱式碳酸铜的分解产物,可选装置如下图所示.

(1)上图装置A中盛放的试剂名称是___.
(2)甲同学将装置按___(填字母,且每套装置限用一次)顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
(3)B装置中粉末完全变黑后,乙同学为确认该黑色粉末是氧化铜而不是碳粉,设计如下实验,请完成下表:
| 实验步骤 | 观察到的现象 | 获得结论 | 有关反应的化学方程式 |
| 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡 | ___ | 黑色粉末均为氧化铜 | ___ |
丙同学利用上述实验后的B装置(包括其中药品),探究CO还原CuO所得固体产物的成分,实验装置如图:

(1)实验过程:打开K,缓缓通入CO气体,一段时间后加热.当黑色固体全部变红后停止加热,继续通入CO气体直至玻璃管冷却.
(2)实验数据
| 反应前 | 反应后 |
| 玻璃管和内盛氧化铜粉末的总质量为62.0g | 玻璃管和内盛红色粉末的总质量为61.7 |
| 玻璃管的总质量为60.0g | |
(4)表达交流:下列有关该实验的说法正确的是___.
A.该实验最好在通风橱中进行
B.先通入一会CO再加热是为了排净装置中的空气
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳
D.排入到烧杯中的溶液可能显碱性,也可能显中性.
| ||
| △ |
| . |
| △ |
| . |
| △ |
| . |
| △ |
| . |
.
.
.
.
2

| 实验步骤 | 观察到的现象 | 获得结论 | 有关反应的化学方程式 |
| 取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡 | ___ | 黑色粉末均为氧化铜 | ___ |

| 反应前 | 反应后 |
| 玻璃管和内盛氧化铜粉末的总质量为62.0g | 玻璃管和内盛红色粉末的总质量为61.7 |
| 玻璃管的总质量为60.0g | |
▼优质解答
答案和解析
【实验验证】
(1)上图装置A中盛放的试剂名称是澄清石灰水,目的是为了检验生成物中是否含有二氧化碳.
故填:澄清石灰水.
(2)甲同学将装置按B→C→A顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
故填:B→C→A.
(3)实验步骤:取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡;
实验现象:固体溶解,溶液变成蓝色;
实验结论:黑色粉末为氧化铜;
氧化铜和稀硫酸反应的化学方程式为:CuO+H22SO44=CuSO44+H22O.
【拓展探究】
(3)如果玻璃管中的固体是铜,则铜的质量为:2.0g×
×100%=1.6g,而玻璃管中的固体质量为:62.0g-61.7g=0.3g,因此红色固体粉末为铜和氧化铜.
故填:铜和氧化铜.
(4)A.该实验对一氧化碳进行了收集,因此不需要在通风橱中进行;
B.先通入一会CO再加热是为了排净装置中的空气;
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳;
D.排入到烧杯中的溶液,无论是氢氧化钠溶液,还是碳酸钠溶液,还是氢氧化钠和碳酸钠的混合溶液,都显碱性.
故填:BC.
64 80 64 64 6480 80 80×100%=1.6g,而玻璃管中的固体质量为:62.0g-61.7g=0.3g,因此红色固体粉末为铜和氧化铜.
故填:铜和氧化铜.
(4)A.该实验对一氧化碳进行了收集,因此不需要在通风橱中进行;
B.先通入一会CO再加热是为了排净装置中的空气;
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳;
D.排入到烧杯中的溶液,无论是氢氧化钠溶液,还是碳酸钠溶液,还是氢氧化钠和碳酸钠的混合溶液,都显碱性.
故填:BC.
(1)上图装置A中盛放的试剂名称是澄清石灰水,目的是为了检验生成物中是否含有二氧化碳.
故填:澄清石灰水.
(2)甲同学将装置按B→C→A顺序组合进行实验,验证出碱式碳酸铜的分解产物中有二氧化碳和水.
故填:B→C→A.
(3)实验步骤:取少量黑色粉末于试管中,向其中加入足量的稀硫酸,震荡;
实验现象:固体溶解,溶液变成蓝色;
实验结论:黑色粉末为氧化铜;
氧化铜和稀硫酸反应的化学方程式为:CuO+H22SO44=CuSO44+H22O.
【拓展探究】
(3)如果玻璃管中的固体是铜,则铜的质量为:2.0g×
| 64 |
| 80 |
故填:铜和氧化铜.
(4)A.该实验对一氧化碳进行了收集,因此不需要在通风橱中进行;
B.先通入一会CO再加热是为了排净装置中的空气;
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳;
D.排入到烧杯中的溶液,无论是氢氧化钠溶液,还是碳酸钠溶液,还是氢氧化钠和碳酸钠的混合溶液,都显碱性.
故填:BC.
| 64 |
| 80 |
故填:铜和氧化铜.
(4)A.该实验对一氧化碳进行了收集,因此不需要在通风橱中进行;
B.先通入一会CO再加热是为了排净装置中的空气;
C.装置图中虚线框内的装置既能吸收二氧化碳,又能收集一氧化碳;
D.排入到烧杯中的溶液,无论是氢氧化钠溶液,还是碳酸钠溶液,还是氢氧化钠和碳酸钠的混合溶液,都显碱性.
故填:BC.
看了 某兴趣小组对碱式碳酸铜的分解...的网友还看了以下:
过碳酸钠(化学式xNa2CO3•yH2O2)遇水易分解为碳酸钠和过氧化氢,有效增加水体中的溶解氧. 2020-04-08 …
阅读下面的资料来回答问题33.(8分)阅读下列材料:材料一(图略)19世纪70年代日本新式学校19 2020-05-13 …
在Ba(OH)2,NaOH,Cu,Mg,CuSO4.稀H2SO4等物质钟,选取恰当的物质,写出符合 2020-06-03 …
在日常生活中,如取款、上网等都需要密码.有一种用“分解因式”法产生的密码,在日常生活中如取款、上网等 2020-11-07 …
下列各句中,没有语病的一句是A.2月12日,石家庄市中级人民法院宣告有着53年历史的三鹿集团正式破产 2020-11-12 …
经济学题目,请各位帮忙解答1.某企业成本函数为c=x2+100,c为总成本,x为产品x的产量(10分 2020-11-15 …
对话式教学是谁最先提出?苏格拉底还是柏拉图?雅典学园是不是对话式教学?那吕克昂学园呢? 2020-11-15 …
19世纪后半期,中国的教育发生了历史性的变化,这主要表现在()A.废除了科举制度B.新式学堂成为培育 2020-12-18 …
3D打印是以数字模型文件为基础,以粉末状金属或塑料等黏合材料为原料,通过逐层打印的方式生产各种形状的 2020-12-18 …
2013年9月26日,一汽大众佛山工厂正式投产,该工厂生产的全新高尔夫车型正式下线,佛山分公司生产基 2021-01-06 …