早教吧作业答案频道 -->化学-->
肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1(1)写出肼和N2O4反应反应生成N
题目详情
肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
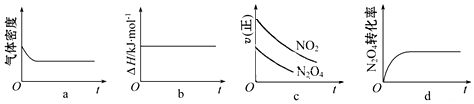
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.
(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.

(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.242
22241-1
242222-1
242
24224

3
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.

(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:
①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ•mol-1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式___;
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)⇌2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___.

(3)肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼-空气燃料电池放电时负极的电极反应式是___.
(4)传统制备肼的方法,是以NaClO氧化NH3,制得肼的稀溶液.该反应的离子方程式是___.242
22241-1
242222-1
242
24224

3
▼优质解答
答案和解析
(1)肼可作为火箭发动机的燃料,与氧化剂N22O44反应生成N22和水蒸气,
①N22(g)+2O22(g)=N22O44(l)△H11=-19.5kJ•mol-1-1
②N22H44(l)+O22(g)=N22(g)+2H22O(g)△H22=-534.2kJ•mol-1-1
根据盖斯定律将方程式②×2-①得肼和N22H44 反应的热化学方程式:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol,
故答案为:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol;
(2)a、反应方程式两边气体的质量不相等,密度不变,说明达到了平衡状态,故a正确;
b、反应过程中,反应热不会变化,不是变量,无法判断是否达到平衡状态,故b错误;
c、根据图象,正反应速率还在减小,则说明未达到平衡状态,故c错误;
d、四氧化二氮的转化率不变,说明正逆反应速率相等,达到了平衡状态,故d正确;
故选ad;
(3)肼一空气燃料碱性电池中,负极上肼失电子和氢氧根离子反应生成水和氮气,电极反应式为:N22H44+4OH---4e--=4H22O+N22↑,
故答案为:N22H44+4OH---4e--=4H22O+N22↑;
(4)NH33与NaClO发生氧化还原反应可得到肼(N22H44)、氯化钠和水,所以该反应的离子方程式为:2NH33+ClO--=N22H44+Cl--+H22O,
故答案为:2NH33+ClO--=N22H44+Cl--+H22O.
①N22(g)+2O22(g)=N22O44(l)△H11=-19.5kJ•mol-1-1
②N22H44(l)+O22(g)=N22(g)+2H22O(g)△H22=-534.2kJ•mol-1-1
根据盖斯定律将方程式②×2-①得肼和N22H44 反应的热化学方程式:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol,
故答案为:2N22H44(l)+N22O44(l)=3N22(g)+4H22O(g)△H=-1048.9kJ/mol;
(2)a、反应方程式两边气体的质量不相等,密度不变,说明达到了平衡状态,故a正确;
b、反应过程中,反应热不会变化,不是变量,无法判断是否达到平衡状态,故b错误;
c、根据图象,正反应速率还在减小,则说明未达到平衡状态,故c错误;
d、四氧化二氮的转化率不变,说明正逆反应速率相等,达到了平衡状态,故d正确;
故选ad;
(3)肼一空气燃料碱性电池中,负极上肼失电子和氢氧根离子反应生成水和氮气,电极反应式为:N22H44+4OH---4e--=4H22O+N22↑,
故答案为:N22H44+4OH---4e--=4H22O+N22↑;
(4)NH33与NaClO发生氧化还原反应可得到肼(N22H44)、氯化钠和水,所以该反应的离子方程式为:2NH33+ClO--=N22H44+Cl--+H22O,
故答案为:2NH33+ClO--=N22H44+Cl--+H22O.
看了 肼可作为火箭发动机的燃料,与...的网友还看了以下:
(1)肼(N2H4)可作为火箭发动机的燃料,与氧化剂N2O4反应生成N2和水蒸气.已知:①N2(g 2020-04-07 …
呼吸面具里有Na2O2,可吸收CO2放出O2,若用超氧化钾(KO2)代替过氧化钠,也能吸收CO2生 2020-04-08 …
以Mycountry'sclimate写一篇英语作文1.写出我国东南西北的气候特点2.写出哈尔滨的 2020-05-13 …
求几篇600字的作文1写人的2写动物的3写饰品的4推销的5写景的6写水果的7有些人(事或物)令你得 2020-06-07 …
语文寒假作业!1.写出10组可以颠倒使用的成语,如“万水千山——千山万水”、“光明正大——正大光明 2020-07-25 …
(2006•玉溪)如图,半径分别为4cm和3cm的⊙O1,⊙O2相交于A,B两点,且O1O2=6c 2020-07-31 …
I.已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol2H2(g)+O2(g) 2020-10-30 …
《我发现了他(她)的魅力》作文1.写人.2.有一个发现的转变.3.关于阳光、乐观的特点.4.语言优美 2020-11-30 …
九、习作。下面共有两个作文题目,请你任选一个按要求写作。1.写一封信,向你的亲友介绍你游览过的一处景 2020-12-02 …
(2003•哈尔滨)如图,⊙O1与⊙O2相交于A、B两点,O1A切⊙O2于点A,过点O;作⊙O2的割 2020-12-05 …