早教吧作业答案频道 -->化学-->
Ni和Fe在工业生产和新型材料领域有广泛的应用.黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物.室温为非活性物质.温度升高后变得活泼.在空气中氧化成三氧
题目详情
Ni和Fe在工业生产和新型材料领域有广泛的应用.黄铁矿被称“愚人金”,化学成分是FeS2,晶体属正方体晶系的硫化物矿物.室温为非活性物质.温度升高后变得活泼.在空气中氧化成三氧化二铁和二氧化硫,主要用于接触法制造硫酸:回答下列问题:
(1)将FeS2与稀盐酸反应得到H2S2,H2S2分子中,共价键的类型是___;FeS2氧化得到SO2,在SO2分子中的S原子的杂化轨道类型是___.-
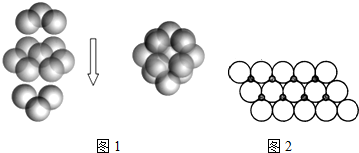
(2)FeS2的晶体中的Fe2+离子的排列方式如图1所示:
①每个Fe2+周围最近的等距离的S22-离子有___个.
②已知FeS2的晶胞参数是a0=0.54nm,它的密度为___g•cm-3(列式并计算,阿伏加德罗常数为6.02×1023).
(3)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为___(用含有a的代数式表示).在一定温度下,NiO晶体可以自发地分散并形成“单分子层”(如图2),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为___g(氧离子的半径为1.40×10-10m,
≈1.732).

(1)将FeS2与稀盐酸反应得到H2S2,H2S2分子中,共价键的类型是___;FeS2氧化得到SO2,在SO2分子中的S原子的杂化轨道类型是___.-
(2)FeS2的晶体中的Fe2+离子的排列方式如图1所示:
①每个Fe2+周围最近的等距离的S22-离子有___个.
②已知FeS2的晶胞参数是a0=0.54nm,它的密度为___g•cm-3(列式并计算,阿伏加德罗常数为6.02×1023).
(3)NiO晶体结构与NaCl晶体类似,其晶胞的棱长为a cm,则该晶体中距离最近的两个阳离子核间的距离为___(用含有a的代数式表示).在一定温度下,NiO晶体可以自发地分散并形成“单分子层”(如图2),可以认为氧离子作密致单层排列,镍离子填充其中,列式并计算每平方米面积上分散的该晶体的质量为___g(氧离子的半径为1.40×10-10m,
| | 3 |
▼优质解答
答案和解析
(1)H2S2分子中,存在H-S键为极性共价键和S-S键为非极性共价键,在SO2分子中的S原子的价层电子对数为6+02=3,所以S原子的杂化轨道类型为sp2杂化,故答案为:极性共价键、非极性共价键;sp2;(2)①每个Fe2+周围最...
看了 Ni和Fe在工业生产和新型材...的网友还看了以下:
“人和”的意义为什么“人和”是人文社会最高的境界? 2020-05-14 …
人和实业集团股份有限公司(以下简称“人和公司”)是一家在国内上市的大型多元化投资公司。人和公 2020-05-19 …
以我身边的人和是为题目写一篇600字九年级作文 2020-06-10 …
地利不如人和中的地利、人和是什么意思? 2020-06-11 …
有8个人都是四月份出生,并且都属猪,当他们岁数连乘积是17597125,8个人和是我只知道至少要有 2020-06-16 …
其年始改称元和是什么意思? 2020-06-30 …
某单位有技术人员240人,其中高级职称者只占10﹪,今年该单位从外部聘请了若干名高级职称人员进来, 2020-07-06 …
2004年3月,英国业余历史学家宣称郑和是美洲大陆的发现者,如果他的证据成立,全世界的历史书都要改写 2020-12-10 …
2004年3月,英国业余历史学家宣称郑和是美洲新大陆的发现者,如果他的证据成立,全世界的历史书都要改 2020-12-16 …
关关跳了36下欢欢跳了48下乐乐跳的是关关和欢欢的总数的14分之11淘淘说3个人和是我的3分之2 2020-12-22 …