早教吧作业答案频道 -->化学-->
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图:(1)将NaCl溶液进行电解,在电解槽的阴极区获得的产品有.(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是
题目详情
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图: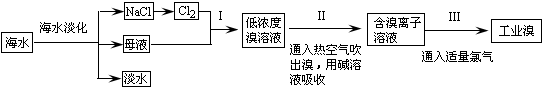
(1)将NaCl溶液进行电解,在电解槽的阴极区获得的产品有___.
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是___.
(3)某化学小组同学为了解从工业溴中提纯溴的方法,查阅有关资料,Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性.他们参观生产过程后,设计了如下实验装置: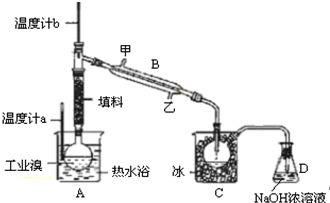
①图中仪器B的名称:___.
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是___.
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:___.
④C中液体产生颜色为___.
(4)请从图中选用四个装置(可重复使用)完成向溶液A中通入过量Cl2的实验,将所选装置的编号填入下列对应的方框,在对应方框下括号内填入相关试剂;
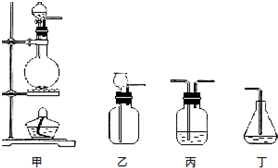
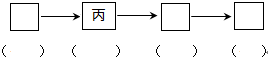
(5)若食盐样品中混有NaBr杂质,为了测定该食盐样品的纯度,可设计如下实验过程: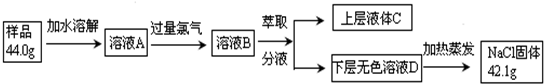
由实验数据测得氯化钠的纯度=___.

(1)将NaCl溶液进行电解,在电解槽的阴极区获得的产品有___.
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是___.
(3)某化学小组同学为了解从工业溴中提纯溴的方法,查阅有关资料,Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性.他们参观生产过程后,设计了如下实验装置:

①图中仪器B的名称:___.
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是___.
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件:___.
④C中液体产生颜色为___.
(4)请从图中选用四个装置(可重复使用)完成向溶液A中通入过量Cl2的实验,将所选装置的编号填入下列对应的方框,在对应方框下括号内填入相关试剂;


(5)若食盐样品中混有NaBr杂质,为了测定该食盐样品的纯度,可设计如下实验过程:

由实验数据测得氯化钠的纯度=___.
▼优质解答
答案和解析
(1)电解饱和氯化钠溶液,在阳极上产生氯气,阴极上产生氢气,同时生成了氢氧化钠,即H2、NaOH,故答案为:H2、NaOH;
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,目的是低浓度的Br2溶液在提取时消耗过多的原料和能源,转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素,
故答案为:提高溴的富集程度;
(3)①由装置图可知,提纯溴利用的原理是蒸馏,仪器B为冷凝管,
故答案为:冷凝管;
②溴单质是一种强氧化剂,易腐蚀橡胶制品,所以整套装置不能用橡胶塞和橡胶管,
故答案为:Br2腐蚀橡胶;
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件是:控制温度计b的温度,并收集59℃的馏分,
故答案为:控制温度计b的温度,并收集59℃的馏分;
④控制温度59℃,使溴单质挥发,通过冷凝得到呈深红棕色或红棕色的液态溴单质,
故答案为:深棕红色或红棕色;
(4)若食盐样品中混有NaBr杂质,加水溶解后通入氯气,经萃取分液后得到氯化钠溶液和溴的四氯化碳溶液,对氯化钠溶液进行蒸发结晶,得到氯化钠固体,根据氯化钠和样品的质量,可得到该食盐样品的纯度,该实验方法为定量法中的重量法,实验室用浓盐酸和二氧化锰在加热条件下反应生成氯气,用丙除去氯化氢,然后在丙中反应,尾气也可用丙处理,氯气的制取选用二氧化锰和浓盐酸,故选用甲装置,饱和食盐水除去氯化氢,通气体A溶液中选用丙装置,过量的氯气用丙装置中的氢氧化钠除去,
故答案为: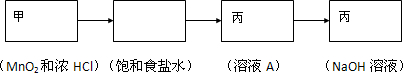 ;
;
(5)设样品中溴化钠的质量为xg,
2NaBr+Cl2=2NaCl+Br2 △m
206 117 89
x 44-42.1=1.9
=
x=4.4,故原固体混合物中氯化钠的质量分数为
×100%=90.0%,
故答案为:90.0%.
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,目的是低浓度的Br2溶液在提取时消耗过多的原料和能源,转化为HBr后易被氧化剂氯气氧化为溴单质,用于富集溴元素,
故答案为:提高溴的富集程度;
(3)①由装置图可知,提纯溴利用的原理是蒸馏,仪器B为冷凝管,
故答案为:冷凝管;
②溴单质是一种强氧化剂,易腐蚀橡胶制品,所以整套装置不能用橡胶塞和橡胶管,
故答案为:Br2腐蚀橡胶;
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件是:控制温度计b的温度,并收集59℃的馏分,
故答案为:控制温度计b的温度,并收集59℃的馏分;
④控制温度59℃,使溴单质挥发,通过冷凝得到呈深红棕色或红棕色的液态溴单质,
故答案为:深棕红色或红棕色;
(4)若食盐样品中混有NaBr杂质,加水溶解后通入氯气,经萃取分液后得到氯化钠溶液和溴的四氯化碳溶液,对氯化钠溶液进行蒸发结晶,得到氯化钠固体,根据氯化钠和样品的质量,可得到该食盐样品的纯度,该实验方法为定量法中的重量法,实验室用浓盐酸和二氧化锰在加热条件下反应生成氯气,用丙除去氯化氢,然后在丙中反应,尾气也可用丙处理,氯气的制取选用二氧化锰和浓盐酸,故选用甲装置,饱和食盐水除去氯化氢,通气体A溶液中选用丙装置,过量的氯气用丙装置中的氢氧化钠除去,
故答案为:
 ;
;(5)设样品中溴化钠的质量为xg,
2NaBr+Cl2=2NaCl+Br2 △m
206 117 89
x 44-42.1=1.9
| 206 |
| x |
| 89 |
| 1.9 |
x=4.4,故原固体混合物中氯化钠的质量分数为
| 44.0-4.4 |
| 44.0 |
故答案为:90.0%.
看了 海水是巨大的资源宝库,从海水...的网友还看了以下:
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规 2020-04-12 …
(2013•江苏)用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作.下 2020-04-12 …
下列变化中亚硫酸表现的性质属于酸性的是()A.能使酸性高锰酸钾溶液褪色B.在空气中久置,溶液pH变 2020-05-13 …
(盐城,2006)不纯的NaCl样品中可能含有KCl、、中的一种或几种.称取11.7g样品加到水中 2020-05-13 …
检验SO2中是否混有CO2气体,可采用的方法是()A.通过品红溶液,若品红溶液褪色,则说明混有CO 2020-05-13 …
过氧乙酸是一种常用的消毒剂.工业品过氧乙酸原液通常是15%过氧乙酸溶液(密度为1.15g.cm-3 2020-06-23 …
下列过程中,不涉及化学变化的是A.浓硫酸加入蔗糖固体中B.氨气溶于水,水溶液呈碱性C.SO2使品红 2020-06-27 …
下列关于SO2性质的说法中,不正确的是()A.能使品红溶液褪色B.能与水反应生成硫酸C.能与NaO 2020-07-05 …
某K2C03样品中含有Na2C03、KN03和Ba(N03)2三种杂质中的一种或二种.现将13.8 2020-07-09 …
某固体样品中,可能含有Na2CO3、Na2SO4、NaCl、Cu(NO3)2、Ca(NO3)2中的 2020-07-25 …