早教吧作业答案频道 -->化学-->
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:请填写下列空白:(1)从海带中提取碘元素的步骤中,选用的实验仪器不能都用到的是A.海带灼
题目详情
海带中含有丰富的碘.为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
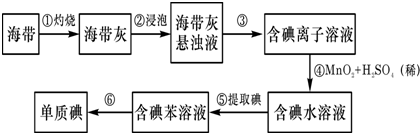
请填写下列空白:
(1)从海带中提取碘元素的步骤中,选用的实验仪器不能都用到的是___
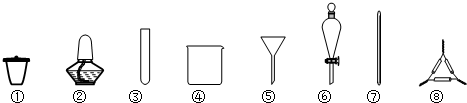
A.海带灼烧灰化,选用①②⑧B.加水浸泡加热,选用②④⑦
C.过滤得到滤液,选用④⑤⑦D.萃取和分液,选用③④⑥
(2)步骤⑤中,某学生选择用苯来提取碘水中的单质碘的理由是___.(选填序号)
a.单质碘与苯不发生化学反应 b.碘在苯中溶解度小于水
c.碘在苯中溶解度大于水 d.苯与水互不相溶
提取碘的过程中,不能使用的有机溶剂是___.(选填序号)
a.酒精 b.汽油 c.四氯化碳
(3)步骤④中MnO2的作用是___ (选填:氧化剂、还原剂、催化剂).
(4)单质碘有许多用途,其中之一是生产加碘食盐中的碘剂--碘酸钾(KIO3).合格加碘食盐含碘量(以I计)为20-50mg/Kg,则每千克该加碘食盐中碘酸钾的最小质量为___mg.
(5)已知:2Fe3++2I-→2Fe2++I2 氯气既可以氧化Fe2+,也可以氧化I-. 往200mLFeI2溶液中通入8.96L(标准状况)Cl2,反应完成后,溶液中有
Fe2+被氧化,则原FeI2溶液的物质的量浓度___.

请填写下列空白:
(1)从海带中提取碘元素的步骤中,选用的实验仪器不能都用到的是___

A.海带灼烧灰化,选用①②⑧B.加水浸泡加热,选用②④⑦
C.过滤得到滤液,选用④⑤⑦D.萃取和分液,选用③④⑥
(2)步骤⑤中,某学生选择用苯来提取碘水中的单质碘的理由是___.(选填序号)
a.单质碘与苯不发生化学反应 b.碘在苯中溶解度小于水
c.碘在苯中溶解度大于水 d.苯与水互不相溶
提取碘的过程中,不能使用的有机溶剂是___.(选填序号)
a.酒精 b.汽油 c.四氯化碳
(3)步骤④中MnO2的作用是___ (选填:氧化剂、还原剂、催化剂).
(4)单质碘有许多用途,其中之一是生产加碘食盐中的碘剂--碘酸钾(KIO3).合格加碘食盐含碘量(以I计)为20-50mg/Kg,则每千克该加碘食盐中碘酸钾的最小质量为___mg.
(5)已知:2Fe3++2I-→2Fe2++I2 氯气既可以氧化Fe2+,也可以氧化I-. 往200mLFeI2溶液中通入8.96L(标准状况)Cl2,反应完成后,溶液中有
| 1 |
| 2 |
▼优质解答
答案和解析
(1)A.将海带灼烧灰化,应在坩埚中加热,用到的仪器有①、②和⑧,必要时还可用到三脚架或铁架台带铁圈,故A正确;
B.加水浸泡加热,应在烧杯中进行,加热用酒精灯,用玻璃棒搅拌,用到的仪器为②④⑦,故B正确;
C.过滤时用到④、⑤和⑦,故C正确;
D.萃取和分液用到④⑥,不用试管,故D错误.
故选D;
(2)萃取剂的选择原理:苯与水、I2均不发生化学反应,和水互不相溶,要萃取的物质在其中的溶解度大于在水中的溶解度,选择用苯来提取碘水中的单质碘的理由是a.单质碘与苯不发生化学反应,c.碘在苯中溶解度大于水,d.苯与水互不相溶,提取碘的过程中,不能使用的有机溶剂是a.酒精,酒精和溶液不能分层,
b.汽油,c.四氯化碳在水溶液中不溶都能分层,碘单质在四氯化碳,汽油中溶解度大于水中,可以做萃取剂,
故答案为:a c d;a;
(3)在酸性环境下,二氧化锰能将碘离子氧化为碘单质,即2I-+MnO2+4H+═Mn2++I2+2H2O,Mn元素的化合价降低,MnO2作为氧化剂,
故答案为:氧化剂;
(4)1kg食盐中至少含碘元素20mg,即含Ⅰ物质的量为
=1.575×10-4 mol,故每千克食盐中n(KIO3)=n(I)=1.57×10-4 mol,质量=1.575×10-4 mol×214g/mol=33.7mg,
故答案为:33.7;
(5)已知:还原性强弱:I->Fe2+,往200mL碘化亚铁溶液中缓慢通入8.96L(标准状况)氯气,氯气先氧化碘离子,再氧化亚铁离子,已知氯气的物质的量为
=0.4mol,发生反应离子方程式为:Cl2+2I-=2Cl-+I2,碘离子完全氧化后,溶液中有
的Fe2+被氧化成Fe3+,发生反应离子方程式为:
Cl2+2Fe2+=2Cl-+Fe3+,设原碘化亚铁溶液的物质的量浓度为cmol/L,则c(I-)=2c(FeI2)=2c,c(Fe2+)=cmol/L,
所以与碘离子反应消耗的氯气为n(Cl2)=
n(I-)=
×2c×0.2L=0.2cmol,
反应完成后溶液中有
的Fe2+被氧化成Fe3+,则与亚铁离子反应消耗的氯气为n(Cl2)=
×
n(Fe2+)=
c×0.2L=0.05cmol,所以0.05cmol+0.2cmol=0.4mol
解得:c=1.6mol/L,
故答案为:1.6mol/L;
B.加水浸泡加热,应在烧杯中进行,加热用酒精灯,用玻璃棒搅拌,用到的仪器为②④⑦,故B正确;
C.过滤时用到④、⑤和⑦,故C正确;
D.萃取和分液用到④⑥,不用试管,故D错误.
故选D;
(2)萃取剂的选择原理:苯与水、I2均不发生化学反应,和水互不相溶,要萃取的物质在其中的溶解度大于在水中的溶解度,选择用苯来提取碘水中的单质碘的理由是a.单质碘与苯不发生化学反应,c.碘在苯中溶解度大于水,d.苯与水互不相溶,提取碘的过程中,不能使用的有机溶剂是a.酒精,酒精和溶液不能分层,
b.汽油,c.四氯化碳在水溶液中不溶都能分层,碘单质在四氯化碳,汽油中溶解度大于水中,可以做萃取剂,
故答案为:a c d;a;
(3)在酸性环境下,二氧化锰能将碘离子氧化为碘单质,即2I-+MnO2+4H+═Mn2++I2+2H2O,Mn元素的化合价降低,MnO2作为氧化剂,
故答案为:氧化剂;
(4)1kg食盐中至少含碘元素20mg,即含Ⅰ物质的量为
| 20×10-3g |
| 127g/mol |
故答案为:33.7;
(5)已知:还原性强弱:I->Fe2+,往200mL碘化亚铁溶液中缓慢通入8.96L(标准状况)氯气,氯气先氧化碘离子,再氧化亚铁离子,已知氯气的物质的量为
| 8.96L |
| 22.4L/mol |
| 1 |
| 2 |
Cl2+2Fe2+=2Cl-+Fe3+,设原碘化亚铁溶液的物质的量浓度为cmol/L,则c(I-)=2c(FeI2)=2c,c(Fe2+)=cmol/L,
所以与碘离子反应消耗的氯气为n(Cl2)=
| 1 |
| 2 |
| 1 |
| 2 |
反应完成后溶液中有
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 4 |
解得:c=1.6mol/L,
故答案为:1.6mol/L;
看了 海带中含有丰富的碘.为了从海...的网友还看了以下:
读某国地形图和气候材料,回答下列各题.(1)描述巴基斯坦的地形特点.(2)巴基斯坦有东方的“水果篮 2020-04-09 …
从五带的划分看,我国大部分地区位于()A.北温带B.热带C.北寒带 2020-05-14 …
读中国略图,结合相关知识回答38-40题.从五带的划分看,我国大部分地区位于()A.北温带B.热带 2020-05-14 …
从五带的划分来看,我国领土大部分位于()A.热带B.北温带C.南温带D.北寒带 2020-05-14 …
仔细观察左边亚洲范围示意图,回答下列问题(1)从东西半球看,亚洲大部分位于半球;从五带的划分看,大 2020-05-14 …
读图,回答下列问题.(1)从东西半球看,亚洲大部分位于半球;从南北半球看,大部分位于半球;从五带的 2020-05-14 …
从五带的划分来看,我国领土大部分在()A.热带B.亚热带C.北温带D.寒带 2020-05-15 …
读图,描述一下亚洲的地理位置.(1)从东西半球看,亚洲大部分位于半球.(2)从五带的划分看,亚洲大 2020-05-17 …
读亚洲地形图,回答问题.(1)从五带的位置看,亚洲地跨带、带和带,东、北、南三面濒临海洋,其中东临 2020-05-17 …
从五带的位置看,亚洲地跨带、带和带,东、北、南三面濒临海洋,其中东临洋,北临洋,南临洋,西部深入到 2020-07-01 …