向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量.其中主要含硫各物种(H2S、HS-、S2-)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示
向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸至过量.其中主要含硫各物种(H2S、HS-、S2-)的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与滴加盐酸体积的关系如图所示(忽略滴加过程H2S气体的逸出).下列说法不正确的是( )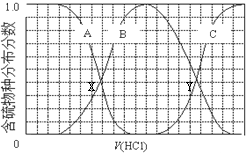
A. 含硫物种B表示HS-
B. 在滴加盐酸过程中,溶液中c(Na+)与含硫各物种浓度的大小关系为:c(Na+)=3[c(H2S)+c(HS-)+c(S2-)]
C. X,Y为曲线的两交叉点,若能知道X点处的pH,就可以计算出H2S的Ka值
D. NaHS呈碱性,若向溶液中加入CuSO4溶液,恰好完全反应,所得溶液呈强酸性,其原因是Cu2++HS-═CuS↓+H+
故A正确;
B.C浓度一直在增加为H2S,向等物质的量浓度Na2S、NaOH混合溶液中滴加稀盐酸,因体积相同,设Na2S、NaOH各为1mol,则n(Na)=3n(S),溶液中含硫的微粒为HS-、S2-、H2S,则c(Na+)=3[c(H2S)+c(HS-)+c(S2-)],或溶液中存在电荷守恒得到c(Na+)=c(Cl-)+c(OH-)+c(HS-)+2c(S2-)-c(H+);
故B正确;
C.图象分析可知A为S2-,B为HS-,C表示H2S,当滴加盐酸至Y点时,表示两者含量相等,所以Ka=
| c(HS-)c(H+) |
| c(H2S) |
D.NaHS溶液中加入CuSO4溶液,硫化铜难溶于稀酸会发生反应Cu2++HS-=CuS↓+H+,溶液显示强酸性,故D正确;
故选C.
下列说法正确的是()A.已知0.1mol•L-1的醋酸溶液中存在电离平衡:CH3COOH⇌CH3C 2020-05-14 …
某温度下,等体积、c(H+)相同的盐酸和醋酸溶液分别加水稀释,溶液中的c(H+)随溶液体积变化的曲 2020-05-17 …
下列离子方程式书写正确的是()A.向稀硫酸中加入氢氧化钡溶液H++SO42-+Ba2++HO-=H 2020-06-22 …
某溶液中含有H+、SO42-、NO3-三种离子,其中H+、SO42-的物质的量浓度分别为7.0mo 2020-07-15 …
某温度下,下列溶液肯定呈酸性的是A.含H+的溶液B.加酚酞显无色的溶液C.pH<7的溶液D.c(H 2020-07-15 …
在0.1mol/L的CH3COONa溶液中,加入少量NaOH溶液及加水,将溶液中各种离子、分子、p 2020-07-29 …
25℃时,向10mL0.01mol/LKOH溶液中滴加0.01mol/L苯酚溶液,混合溶液中粒子浓 2020-07-29 …
气体C与气体G反应可生成固体单质B一些反应所需和生成的水没有标出1.固体A--固体B+溶液H+气体C 2020-10-31 …
将NaIO3溶液逐滴加入含5molNaHSO3的溶液中,依次发生反应:①IO3-+HSO3-→I-+ 2020-11-01 …
在离子浓度都为0.1mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是()A. 2020-12-05 …