已知:Fe2+能被稀硝酸氧化,反应方程式为:3Fe(NO3)2+4HNO3(稀)→3Fe(NO3)3+NO↑+2H2O现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的质量分
已知:Fe 2+ 能被稀硝酸氧化,反应方程式为:
3Fe(NO 3 ) 2 +4HNO 3 (稀)→3Fe(NO 3 ) 3 +NO↑+2H 2 O
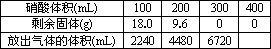
现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的质量分数为0.20的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体的体积(标准状况下)与剩余固体的质量如下表:
(1)由NO与HNO 3 的关系可知,稀硝酸的物质的量浓度为________mol·L -1 .
(2)稀硝酸的密度为________g/cm 3 .
(3)放出2240 mL气体时,反应的离子方程式是________,放出4480 mL气体时,消耗金属的质量为________g.
(4)原混合物中铁和铜的物质的量比为________.
(5)加入400 mL稀硝酸,反应完全后,溶液中NO 3 - 的物质的量为________mol.
(6)当溶液中Cu 2+ 、Fe 2+ 的物质的量浓度相等时,放出气体的体积________mL(标准状况下).
解析:
(1)4(2分) (2)1.26(2分) (3)3Fe+8H++2NO3-→3Fe3++2NO↑+4H2O(2分) 16.8(2分) (4)2∶1(2分) (5)1.20(3分) (5)7840(3分)
1如何除KCL中的FECL3?2如何除CU(NO3)2中的HG(NO3)2?3用3个办法制取MGC 2020-04-10 …
Hg(NO3)2加NaCl反应是什么 2020-04-26 …
Fe(NO3)2加热分解反应为FE(NO3)2----Fe2O3+NO2+O2(未配平),将Fe( 2020-05-14 …
cu加cu(No3)2加稀硫酸的反应为什么会反应?CU与稀硫酸反应本来不会溶解,为什么加CU(No 2020-05-17 …
cu加cu(No3)2加稀硫酸反应现象,原因?求现象 2020-05-17 …
已知Zn(NO3)2分解的化学方程式为:2Zn(NO3)2===(加热的情况下)2ZnO+4NO2 2020-06-28 …
英语翻译通过连续7年的定位试验,研究了日光温室生产中不同生产模式施肥对土壤NO3—N时空分布及累积的 2020-11-23 …
此人太懒.没办法.理解下.4乘-3的平方加6.22.5加-3.3加-12.5加3.3.42乘-2\3 2020-11-23 …
(铀)是重要的核工业原料,常见化合价有+4和+6。硝酸铀酰[UO2(NO3)2]加热可发生如下分解: 2020-12-01 …
2分之[1加2]乘[2加3]分之[1加2加3]乘2加3加4分之1加2加3加4.2分之[1加2]乘[2 2020-12-17 …