早教吧作业答案频道 -->化学-->
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如图的实验装置.(1)实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)△
题目详情
某化学实验小组的同学为探究和比较SO2和氯水的漂白性,设计了如图的实验装置.
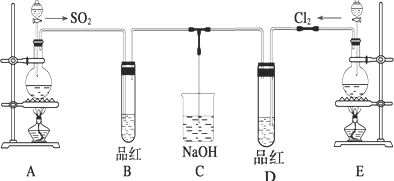
(1)实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O.若有6mol的HCl参加反应,则转移的电子总数为___;
(2)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:___,D:___;
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:B:___,D:___;
(3)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样.请你分析该现象的原因(用化学方程式表示)___.

(1)实验室用装置E制备Cl2,其反应的化学方程式为:MnO2+4HCl(浓)
| ||
(2)①反应开始一段时间后,观察到B、D两个试管中的品红溶液出现的现象是:B:___,D:___;
②停止通气后,再给B、D两个试管分别加热;两个试管中的现象分别为:B:___,D:___;
(3)另一个实验小组的同学认为SO2和氯水都有漂白性,二者混合后的漂白性肯定会更强.他们将制得的SO2和Cl2按1:1同时通入到品红溶液中,结果发现褪色效果并不像想象的那样.请你分析该现象的原因(用化学方程式表示)___.
▼优质解答
答案和解析
(1)依据MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O可知,Mn化合价由+4价→+2价,则每有1molMnO2参加反应,消耗4mol氯化氢,生成1mol氯气,转移2mol,若有6mol的HCl参加反应,则转移的电子总数为1.5NA;
故答案为:1.5NA;
(2)二氧化硫、次氯酸都具有漂白性,所以观察到B、D两个试管中的品红溶液出现的现象都是品红溶液褪色;
二氧化硫是因为与有机色素化合生成不稳定的无色物质而具有漂白性,次氯酸因为具有强的氧化性,能够将有机色素氧化生成稳定的无色物质而具有漂白性,
所以加热后B试管中现象为:褪色的品红又恢复成红色;D试管现象为:无明显现象;
故答案为:品红溶液褪色;品红溶液褪色;褪色的品红又恢复成红色;无明显现象;
(3)氯气具有较强的氧化性,二氧化硫具有较强的还原性,在水溶液中两者1:1发生反应:Cl2+SO2+2H2O═2HCl+H2SO4,生成物都无漂白性,因而SO2和Cl2按1:1同时通入到品红溶液时,品红溶液并不退色,
故答案为:Cl2+SO2+2H2O═2HCl+H2SO4.
| ||
故答案为:1.5NA;
(2)二氧化硫、次氯酸都具有漂白性,所以观察到B、D两个试管中的品红溶液出现的现象都是品红溶液褪色;
二氧化硫是因为与有机色素化合生成不稳定的无色物质而具有漂白性,次氯酸因为具有强的氧化性,能够将有机色素氧化生成稳定的无色物质而具有漂白性,
所以加热后B试管中现象为:褪色的品红又恢复成红色;D试管现象为:无明显现象;
故答案为:品红溶液褪色;品红溶液褪色;褪色的品红又恢复成红色;无明显现象;
(3)氯气具有较强的氧化性,二氧化硫具有较强的还原性,在水溶液中两者1:1发生反应:Cl2+SO2+2H2O═2HCl+H2SO4,生成物都无漂白性,因而SO2和Cl2按1:1同时通入到品红溶液时,品红溶液并不退色,
故答案为:Cl2+SO2+2H2O═2HCl+H2SO4.
看了某化学实验小组的同学为探究和比...的网友还看了以下:
关于x的整系数一元二次方程ax2-bx+c=0(a≠0)中,若a+b是偶数,c是奇数,则()A.方 2020-04-09 …
关于地球磁场与古地质学中同一地质时期的古岩石剩磁方向不同的原因为什么说有漂移运动,不同大陆漂移方向 2020-04-26 …
设,若“方程满足,且方程至少有一根”,就称该方程为“漂亮方程”。则“漂亮方程”的个数为A.8B.1 2020-06-12 …
(1)“漂移”是一种高难度的汽车表演项目.有一种“漂移”方法如下:当汽车在水平地面上疾驶时,车对地 2020-06-13 …
现有一件刚用洗涤剂洗过的衣服,“拧干”后湿衣服上残留的溶液为200g,其中含洗涤剂的质量分数为1% 2020-06-29 …
岳西天仙河景区,蜿蜒二十余公里,乘上古老的竹排漂流其间,冲激流,过险滩,其乐无穷;观两岸,青山依依 2020-07-24 …
读南极图回答下列问题(1).图中甲、乙两箭头能正确表示地球自转方向的是;丙、丁两箭头能正确表示西风漂 2020-11-21 …
漂流急流飞舟,惊险刺激,如图所示,当游客坐在橡皮筏内顺流而下时,以橡皮筏为参照物,游客是的;当橡皮筏 2020-12-19 …
大觉山位于抚州市资溪县境内,大觉山漂流急流飞舟,惊险刺激,如图所示,当游客坐在橡皮筏内顺流而下时,以 2020-12-19 …
O3漂白方程式 2021-01-12 …