早教吧作业答案频道 -->化学-->
如图是在实验室进行二氧化硫制备与验证性质实验的组合装置,部分固定装置未画出.(1)装置B中试剂X是,装置D中盛放NaOH溶液的作用是.(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸
题目详情
如图是在实验室进行二氧化硫制备与验证性质实验的组合装置,部分固定装置未画出.
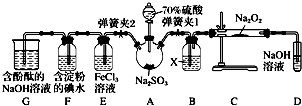
(1)装置B中试剂X是___,装置D中盛放NaOH溶液的作用是___.
(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是___.
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为___;发生反应的离子方程式是___.
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:
取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应.上述方案是否合理?___(填“合理”或“不合理”),原因是___.

(1)装置B中试剂X是___,装置D中盛放NaOH溶液的作用是___.
(2)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体,检验SO2与Na2O2反应是否有氧气生成的操作及现象是___.
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为___;发生反应的离子方程式是___.
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:
取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应.上述方案是否合理?___(填“合理”或“不合理”),原因是___.
▼优质解答
答案和解析
A中制备二氧化硫,X干燥二氧化硫,C中检验SO2与Na2O2反应是否有氧气,D中氢氧化钠溶液吸收剩余的二氧化硫,防止污染空气.E装置验证二氧化硫的还原性,F检验I-还原性弱于SO2,G装置验证二氧化硫为酸性气体,并吸收二氧化硫,防止污染空气.
(1)装置B中试剂X干燥氯气,盛放试剂是浓硫酸,二氧化硫与氢氧化钠反应生成亚硫酸钠和水,离子方程式为SO2+2OH-=SO32-+H2O,所以装置D中盛放NaOH溶液的作用是:吸收未反应的SO2,防止污染空气,
故答案为:浓硫酸;吸收未反应的SO2,防止污染空气;
(2)检验SO2与Na2O2反应是否有氧气生成的方法是:将带火星的木条放在D试管口处,看木条是否复燃,
故答案为:将带火星的木条放在D试管口处,看木条是否复燃;
(3)F中的离子方程式为:SO2+I2+2H2O=2I-+SO42-+4H+,该反应中二氧化硫为还原剂,碘离子为还原产物,氧化还原反应中,还原剂的还原性强于还原产物,能说明I-还原性弱于SO2,现象为:F中溶液蓝色褪去,
故答案为:F中溶液蓝色褪去; SO2+I2+2H2O=2I-+SO42-+4H+;
(4)FeCl3与SO2作用,三价铁具有氧化性,二氧化硫具有还原性,三价铁能将二氧化硫氧化为硫酸,自身被还原为亚铁离子,即2FeCl3+SO2+2H2O═2FeCl2+H2SO4+2HCl,可通过检验硫酸根离子,检验该反应的发生,硝酸具有强氧化性,但该实验中硝酸的存在干扰该SO2与FeCl3反应的验证,3SO2SO2+2HNO3+2H2O=3H2SO4+2NO,所以取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,硫酸根离子不一定来自于SO2与FeCl3反应产物,故该实验设计不合理,
故答案为:不合理;E中溶解的SO2与稀硝酸反应也生成SO42-.
(1)装置B中试剂X干燥氯气,盛放试剂是浓硫酸,二氧化硫与氢氧化钠反应生成亚硫酸钠和水,离子方程式为SO2+2OH-=SO32-+H2O,所以装置D中盛放NaOH溶液的作用是:吸收未反应的SO2,防止污染空气,
故答案为:浓硫酸;吸收未反应的SO2,防止污染空气;
(2)检验SO2与Na2O2反应是否有氧气生成的方法是:将带火星的木条放在D试管口处,看木条是否复燃,
故答案为:将带火星的木条放在D试管口处,看木条是否复燃;
(3)F中的离子方程式为:SO2+I2+2H2O=2I-+SO42-+4H+,该反应中二氧化硫为还原剂,碘离子为还原产物,氧化还原反应中,还原剂的还原性强于还原产物,能说明I-还原性弱于SO2,现象为:F中溶液蓝色褪去,
故答案为:F中溶液蓝色褪去; SO2+I2+2H2O=2I-+SO42-+4H+;
(4)FeCl3与SO2作用,三价铁具有氧化性,二氧化硫具有还原性,三价铁能将二氧化硫氧化为硫酸,自身被还原为亚铁离子,即2FeCl3+SO2+2H2O═2FeCl2+H2SO4+2HCl,可通过检验硫酸根离子,检验该反应的发生,硝酸具有强氧化性,但该实验中硝酸的存在干扰该SO2与FeCl3反应的验证,3SO2SO2+2HNO3+2H2O=3H2SO4+2NO,所以取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,硫酸根离子不一定来自于SO2与FeCl3反应产物,故该实验设计不合理,
故答案为:不合理;E中溶解的SO2与稀硝酸反应也生成SO42-.
看了如图是在实验室进行二氧化硫制备...的网友还看了以下:
在探究弹簧的弹性势能的大小与哪些因素有关时,小阳提出了如下猜想:猜想1:弹性势能的大小与弹簧被压缩 2020-06-18 …
在猜想弹性势能可能与哪几个物理量有关的时候,有人猜想弹性势能可能与弹簧的劲度系数k、与弹簧的伸长量 2020-06-23 …
(2014•黄浦区二模)已知弹簧在其弹性限度内,它的长度y(厘米)与所挂重物质量x(千克)的关系可 2020-07-11 …
与关节牢固性和灵活性相适应的结构特点是:①关节周围有肌肉组织②坚韧的关节囊③关节腔内有滑液④关节面 2020-07-15 …
恩格尔定律在微经中的定义内容是什么好像是与弹性有关系 2020-07-23 …
关于弹力做功与弹性势能变化的关系,判断正确的是()A.弹力做正功,弹性势能一定减小B.弹力做正功,弹 2020-11-02 …
在探究弹性势能的大小跟哪些因素有关时,小明提出了如下猜想:猜想一:弹性势能的大小与弹簧被压缩的程度有 2020-11-02 …
关节十分灵活的原因是()A.关节面覆盖着即光滑又有弹性的关节软骨B.关节囊非常坚韧,把相邻的两骨牢牢 2020-11-02 …
在探究弹性势能的大小跟哪些因素有关时,小明提出了如下猜想:猜想一:弹性势能的大小与弹簧被压缩的程度有 2020-11-02 …
(2008•滨州二模)“蹦极”是冒险者的运动,质量为50kg的运动员,在一座高桥上做“蹦极”运动,他 2020-11-13 …