早教吧作业答案频道 -->化学-->
如图为两种途径制备硫酸的过程(反应条件略),下列说法不正确的是()A、途径②增大02浓度可提高SO2转化率B、含lmolH2S04的浓溶液与足量NaOH反应,放出的热量即
题目详情
如图为两种途径制备硫酸的过程(反应条件略),下列说法不正确的是( )
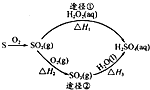

| A、途径②增大0 2 浓度可提高SO 2 转化率 |
| B、含l mol H 2 S0 4 的浓溶液与足量NaOH反应,放出的热量即为中和热 |
| C、途径②中S0 2 和S0 3 均属于酸性氧化物 |
| D、若△H l <△H 2 +△H 3 ,则2H 2 0 2 (aq)=2H 2 0(1)+0 2 (g)为放热反应 |
▼优质解答
答案和解析
考点:酸、碱、盐、氧化物的概念及其相互联系 吸热反应和放热反应 化学平衡的影响因素 专题: 分析:A、增大一种反应物的浓度可以增大另外一种反应物的转化率;B、中和反应的定义:强酸与强碱的稀溶液混合生成1mol水放出的热量为中和热;C、二氧化硫与三氧化硫均属于酸性氧化物;D、焓值小于0为放热反应,据此解答即可. A、增大一种反应物的浓度可以增大另外一种反应物的转化率,故途径②增大02浓度可提高SO2转化率正确,故A正确;B、中和反应的定义:强酸与强碱的稀溶液混合生成1mol水放出的热量为中和热,含l mol H2S04的浓溶液与足量NaOH反应生成2mol水,且浓溶液溶于水放热,故B错误;C、二氧化硫与三氧化硫均属于酸性氧化物,故C正确;D、焓值小于0为放热反应,故D正确,故选B. 点评:本题主要考查的是盖斯定律的应用、化学反应吸热与放热的判断、酸性氧化物和中和热的概念,难度不大.
看了如图为两种途径制备硫酸的过程(...的网友还看了以下:
化学实验室现有98%的浓硫酸,但在实验室中常用到较稀的硫酸.要把50g质量分数为98%的浓硫酸,稀 2020-04-12 …
这道题是不是有错6、取甲种硫酸300克和乙种硫酸250克,再加水200克,可混合成浓度为50%的硫 2020-04-26 …
大侠们帮忙,十万火急第一题:溶质质量分数为98%的浓硫酸(密度=1.98g/cm3),其物质量浓度 2020-04-27 …
在400L浓度为1mol/L的硫酸溶液中加入多少升密度为1.84g/cm^3浓度为98%的硫酸溶液 2020-05-17 …
接触法制备硫酸接触法制硫酸,三种主要设备分别称为沸腾炉、接触室、吸收塔.在这三种设备里所发生的主要 2020-06-05 …
已知硫酸溶液的浓度愈大,其密度就愈大,现将质量分数为3A%的硫酸溶液与质量分数为A%的硫酸溶液等体 2020-07-07 …
用30毫升质量分数为70%硫酸(密度=1.6克/立方厘)米用它配置质量分数为28%的硫酸溶用40毫 2020-07-11 …
用明矾配制溶质为百分之16的硫酸铜溶液100克,需要加水的质量用胆矾配置溶质质量分数为16%的硫酸 2020-07-26 …
质量份数为20%的硫酸与质量份数为50%的硫酸等体积混合为什么质量分数大于35%? 2020-11-01 …
硫酸厂接到一批订单,急需一批浓度为60%的硫酸1200吨.厂长高兴地叫来生产科长告诉他快去准备.可生 2020-11-21 …