早教吧作业答案频道 -->化学-->
I.如图为相互串联的三个装置,试回答:(1)若利用乙池在铁片上镀银,则B是(填电极材料),电极反应式是;应选用的电解质溶液是.(2)若利用乙池进行粗铜的电解精炼,则
题目详情
I.如图为相互串联的三个装置,试回答:
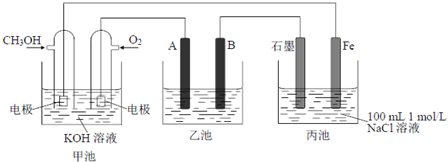
(1)若利用乙池在铁片上镀银,则B是___(填电极材料),电极反应式是___;应选用的电解质溶液是___.
(2)若利用乙池进行粗铜的电解精炼,则___极(填“A”或“B”)是粗铜,若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为___.
(3)丙池滴入少量酚酞试液,电解一段时间___(填“C”或“Fe”)极附近呈红色.
(4)写出甲池负极的电极反应式:___.若甲池消耗3.2gCH3OH气体,则丙池中阳极上放出的气体物质的量为___.
II.(5)请利用反应Fe+2Fe3+=3Fe2+设计原电池.
设计要求:①该装置尽可能提高化学能转化为电能的效率;
②材料及电解质溶液自选,在图中做必要标注;
③画出电子的转移方向.

(1)若利用乙池在铁片上镀银,则B是___(填电极材料),电极反应式是___;应选用的电解质溶液是___.
(2)若利用乙池进行粗铜的电解精炼,则___极(填“A”或“B”)是粗铜,若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为___.
(3)丙池滴入少量酚酞试液,电解一段时间___(填“C”或“Fe”)极附近呈红色.
(4)写出甲池负极的电极反应式:___.若甲池消耗3.2gCH3OH气体,则丙池中阳极上放出的气体物质的量为___.
II.(5)请利用反应Fe+2Fe3+=3Fe2+设计原电池.
设计要求:①该装置尽可能提高化学能转化为电能的效率;
②材料及电解质溶液自选,在图中做必要标注;
③画出电子的转移方向.
▼优质解答
答案和解析
(1)在铁片上镀银,金属铁是阴极材料,金属银是阳极材料,选择硝酸银为电解质溶液,在甲池中,通氧气的电极是正极,所以乙池中A是阳极,B是阴极,B电极上发生反应:Ag++e-=Ag,故答案为:铁片;Ag++e-=Ag;AgNO3溶液;
(2)乙池中A是阳极,B是阴极,利用乙池进行粗铜的电解精炼,金属铜为阴极,粗铜作阳极,活泼的金属在阳极上失电子得到金属阳离子,Fe以Fe2+的形式进入电解液中,不参与放电的Au、Ag形成阳极泥,故答案为:A;Au、Ag以单质的形式沉积在c(阳极)下方,Fe以Fe2+的形式进入电解液中;
(3),在甲池中,通氧气的电极是正极,通燃料的是负极,所以丙中,Fe是阴极,石墨是阳极,电解饱和氯化钠,在阴极上产生氢气,该极区域显示碱性,遇到酚酞显示红色,即电解一段时间Fe极附近呈红色,故答案为:Fe;
(4)燃料电池的负极上是燃料失电子的氧化反应:CH3OH-6e-+8OH-=CO32-+6H2O;若甲池消耗3.2g即0.1molCH3OH气体,则转移电子是0.6mol,
丙池中阳极上放出的氯气,根据2Cl--2e-=Cl2↑,转移0.6mol电子,产生氯气物质的量为0.3mol,故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;0.3mol;
(5)原电池中失电子的物质作负极,根据方程式知,铁作负极,比铁活泼性小的金属或导电的非金属作正极;铁失电子,发生氧化反应;正极上得电子,发生还原反应,根据方程式知,Fe3+得电子,生成Fe2+,电极反应式为:2Fe3++2e-=2Fe2+,电解质是反应物中可溶性的、得电子的物质,所以电解质是可溶性的铁盐,可用氯化铁作电解质,装置如下: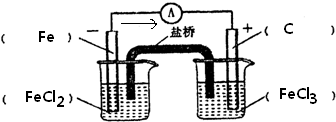 ,电子从负极流向正极,如图中箭头所示,故答案为:
,电子从负极流向正极,如图中箭头所示,故答案为: .
.
(2)乙池中A是阳极,B是阴极,利用乙池进行粗铜的电解精炼,金属铜为阴极,粗铜作阳极,活泼的金属在阳极上失电子得到金属阳离子,Fe以Fe2+的形式进入电解液中,不参与放电的Au、Ag形成阳极泥,故答案为:A;Au、Ag以单质的形式沉积在c(阳极)下方,Fe以Fe2+的形式进入电解液中;
(3),在甲池中,通氧气的电极是正极,通燃料的是负极,所以丙中,Fe是阴极,石墨是阳极,电解饱和氯化钠,在阴极上产生氢气,该极区域显示碱性,遇到酚酞显示红色,即电解一段时间Fe极附近呈红色,故答案为:Fe;
(4)燃料电池的负极上是燃料失电子的氧化反应:CH3OH-6e-+8OH-=CO32-+6H2O;若甲池消耗3.2g即0.1molCH3OH气体,则转移电子是0.6mol,
丙池中阳极上放出的氯气,根据2Cl--2e-=Cl2↑,转移0.6mol电子,产生氯气物质的量为0.3mol,故答案为:CH3OH-6e-+8OH-=CO32-+6H2O;0.3mol;
(5)原电池中失电子的物质作负极,根据方程式知,铁作负极,比铁活泼性小的金属或导电的非金属作正极;铁失电子,发生氧化反应;正极上得电子,发生还原反应,根据方程式知,Fe3+得电子,生成Fe2+,电极反应式为:2Fe3++2e-=2Fe2+,电解质是反应物中可溶性的、得电子的物质,所以电解质是可溶性的铁盐,可用氯化铁作电解质,装置如下:
 ,电子从负极流向正极,如图中箭头所示,故答案为:
,电子从负极流向正极,如图中箭头所示,故答案为: .
.
看了I.如图为相互串联的三个装置,...的网友还看了以下:
关于化学电池反应正负极我知道充电时是电解池,阳极氧化反应,放电时是原电池,负极是氧化反应所以放电负 2020-05-12 …
锂离子电池的应用很广,其正极材料可再生利用.某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙 2020-06-14 …
锂离子电池的应用很广,其正极材料可再生利用.某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙 2020-06-14 …
电解池电子从阳极流向阴极,那么电流流向为什么也从阳极流向阴极电解池电子从阳极流向阴极,可是阳极对应 2020-06-23 …
锂离子电池的应用很广,其正极材料可再生利用.某离子电池正极材料有钴酸锂(LiCoO2),导电剂乙炔黑 2020-11-01 …
锂离子电池的应用很广,其正极材料可再生利用.某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔 2020-11-01 …
锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(LiCoO2)、导电剂乙炔 2020-11-01 …
锂离子电池的应用广泛,其正极材料可再生利用.某锂离子电池正极材料有钴酸锂(LiCoO2)和铝箔等.现 2020-11-01 …
锂离子电池的应用很广,其正极材料可再生利用.某离子电池正极材料有钴酸锂(LiCoO2),导电剂乙炔黑 2020-11-01 …
4,熔融碳酸盐(如:熔融K2CO3)环境下电池总反应:CH4+2O2=CO2+2H2O.正极电极反应 2021-01-14 …