早教吧作业答案频道 -->化学-->
利用黄铜矿(CuFeS2)生产铜、绿矾的过程如下.根据题意完成下列各题:(1)CuFeS2中铜的化合价为+2价,则铁的化合价为.(2)要从溶液中得到绿矾,必须进行的实验操作是(按前后顺
题目详情
利用黄铜矿(CuFeS2)生产铜、绿矾的过程如下.根据题意完成下列各题:
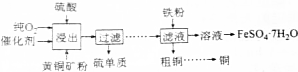
(1)CuFeS2中铜的化合价为+2价,则铁的化合价为___.
(2)要从溶液中得到绿矾,必须进行的实验操作是___(按前后顺序填写字母序号).
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)实验室中配制FeSO4溶液时常将绿矾溶于一定浓度的硫酸中,再加水稀释,这样操作的目的是___.
(4)绿矾产品的纯度可用滴定法进行测定,实验步骤如下:
步骤I.秤取6.000g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中.
步骤3:用硫酸酸化的0.0100mol/LKMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积
步骤4:重复步骤2、步骤3两次、三次评价消耗KMnO4溶液40.00ml.
①判断此滴定实验达到终点的现象是___
②写出滴定过程中发生反应的离子方程式___
③计算上述样品中FeSO4•7H2O的质量分数为___(保留四位有效值)

(1)CuFeS2中铜的化合价为+2价,则铁的化合价为___.
(2)要从溶液中得到绿矾,必须进行的实验操作是___(按前后顺序填写字母序号).
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)实验室中配制FeSO4溶液时常将绿矾溶于一定浓度的硫酸中,再加水稀释,这样操作的目的是___.
(4)绿矾产品的纯度可用滴定法进行测定,实验步骤如下:
步骤I.秤取6.000g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤2:从上述容量瓶中量取25.00mL待测溶液于锥形瓶中.
步骤3:用硫酸酸化的0.0100mol/LKMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积
步骤4:重复步骤2、步骤3两次、三次评价消耗KMnO4溶液40.00ml.
①判断此滴定实验达到终点的现象是___
②写出滴定过程中发生反应的离子方程式___
③计算上述样品中FeSO4•7H2O的质量分数为___(保留四位有效值)
▼优质解答
答案和解析
(1)CuFeS2中铜的化合价为+2价,硫为-2价,根据元素化合价代数和为零可和铁的化合价为+2价,
故答案为:+2;
(2)要从溶液中得到绿矾,可以通过蒸发浓缩,冷却结晶,过滤,洗涤,干燥等步骤,所以实验操作的序号为bcae,
故答案为:bcae;
(3)亚铁离子易水解,在配制硫酸亚铁溶液时要防止亚铁离子水解,所以将绿矾溶于一定浓度的硫酸中可以抑制亚铁离子水解,
故答案为:抑制亚铁离子水解;
(4)①根据题中实验步骤可知,滴定实验达到终点时,溶液中的高锰酸钾不完全褪色,溶液呈浅红色,所以判断滴定实验达到终点的现象是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
②酸性KMnO4被FeSO4还原时生成Mn2+,同时生成铁离子,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
③根据电子得失守恒有关系式MnO4-~5Fe2+,滴定中用去的高锰酸钾的物质的量为0.0100mol/L×0.04L=0.0004mol,所以6.000g绿矾产品中FeSO4•7H2O的物质的量为:
×5×0.0004mol=0.02mol,所以样品中FeSO4•7H2O的质量分数为:
×100%=92.67%,
故答案为:92.67%.
故答案为:+2;
(2)要从溶液中得到绿矾,可以通过蒸发浓缩,冷却结晶,过滤,洗涤,干燥等步骤,所以实验操作的序号为bcae,
故答案为:bcae;
(3)亚铁离子易水解,在配制硫酸亚铁溶液时要防止亚铁离子水解,所以将绿矾溶于一定浓度的硫酸中可以抑制亚铁离子水解,
故答案为:抑制亚铁离子水解;
(4)①根据题中实验步骤可知,滴定实验达到终点时,溶液中的高锰酸钾不完全褪色,溶液呈浅红色,所以判断滴定实验达到终点的现象是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
②酸性KMnO4被FeSO4还原时生成Mn2+,同时生成铁离子,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
③根据电子得失守恒有关系式MnO4-~5Fe2+,滴定中用去的高锰酸钾的物质的量为0.0100mol/L×0.04L=0.0004mol,所以6.000g绿矾产品中FeSO4•7H2O的物质的量为:
| 250 |
| 25 |
| 0.02×278 |
| 6.000 |
故答案为:92.67%.
看了利用黄铜矿(CuFeS2)生产...的网友还看了以下:
把下列各数填入相应集合中+2-30-32/1(这个是负的三有二分之一)-1.414-173/2负数 2020-04-25 …
怎样看化合价的大小下列物质中,硫元素的化合价最低的是?SH(2)SSO(2)H(2)SH(2)SO 2020-05-13 …
补写下列有关节日的两副对联。注意:①内容与节日相关,②可以不考虑平仄。小题1:端午上联:赛龙舟不忘 2020-05-13 …
醉落魄咏鹰古诗赏析1.这首词的上片主要是用什么手法来写鹰的,请做简要分析.2.结合下片的句醉落魄咏 2020-06-19 …
请问〔Mn(CO)4(μ2-Cl)〕2中,为什么不存在金属键?其中μ2中的下标2表示什么意思呢? 2020-07-07 …
CO和CO2的混合气体18g,完全燃烧后测得CO2体积为11.2L(标准状况)(1)混合气体中CO 2020-07-19 …
图1是一个正方形,分别连接这个正方形的对边中点,得到图2;分别连接图2中右下角的小正方形对边中点, 2020-07-30 …
补写下列有关节日的两副对联。注意:①内容与节日相关,②可以不考虑平仄。小题1:端午上联:赛龙舟不忘楚 2020-11-28 …
作为经济大省的江苏,城市化和工业化的进程都比较迅速。结合所给材料回答问题。(1)结合下图,分析江苏省 2020-12-09 …
英语资深达人或是英语老师的进!我是一名初一的学生.快上完新概念2了,但里面有些知识还没搞懂.学完之后 2020-12-29 …