早教吧作业答案频道 -->化学-->
利用黄铜矿(CuFeS2)生产铜、绿矾的过程如下.请回答:(1)CuFeS2中铜的化合价为+2价,则铁的化合价为.(2)要从溶液中得到绿矾,必须进行的实验操作是(按前后顺序填写字母序号
题目详情
利用黄铜矿(CuFeS2)生产铜、绿矾的过程如下.请回答:
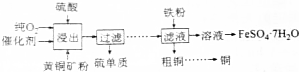
(1)CuFeS2中铜的化合价为+2价,则铁的化合价为___.
(2)要从溶液中得到绿矾,必须进行的实验操作是___(按前后顺序填写字母序号).
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)实验室中配制FeSO4溶液时常将绿矾溶于一定浓度的硫酸中国,再加水稀释,这样操作的目的是___.
(4)绿矾产品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取6.000g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤 2:从上述容量瓶中量取25.00mL待测液溶于锥形瓶中.
步骤3:用硫酸酸化的0.0100mol/LKMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积.
步骤4:重复步骤2、步骤3两次.三次平均消耗KMnO4溶液40.00mL.
①判断此滴定实验达到终点的现象是___.
②写出滴定过程中发生反应的离子方程式___.
③计算上述样品中FeSO4•7H2O的质量分数为___(保留四位有效数字).
(5)粗铜经过电解精炼可制得纯铜,电解精炼过程中阴极发生的电极反应式为___.

(1)CuFeS2中铜的化合价为+2价,则铁的化合价为___.
(2)要从溶液中得到绿矾,必须进行的实验操作是___(按前后顺序填写字母序号).
a.过滤洗涤 b.蒸发浓缩 c.冷却结晶 d.灼烧 e.干燥
(3)实验室中配制FeSO4溶液时常将绿矾溶于一定浓度的硫酸中国,再加水稀释,这样操作的目的是___.
(4)绿矾产品的纯度可用滴定法进行测定,实验步骤如下:
步骤1:称取6.000g绿矾产品,经溶解、定容等步骤准确配制250mL溶液.
步骤 2:从上述容量瓶中量取25.00mL待测液溶于锥形瓶中.
步骤3:用硫酸酸化的0.0100mol/LKMnO4溶液滴定至终点,记录消耗KMnO4溶液的体积.
步骤4:重复步骤2、步骤3两次.三次平均消耗KMnO4溶液40.00mL.
①判断此滴定实验达到终点的现象是___.
②写出滴定过程中发生反应的离子方程式___.
③计算上述样品中FeSO4•7H2O的质量分数为___(保留四位有效数字).
(5)粗铜经过电解精炼可制得纯铜,电解精炼过程中阴极发生的电极反应式为___.
▼优质解答
答案和解析
(1)CuFeS2中铜的化合价为+2价,硫为-2价,根据元素化合价代数和为零可和铁的化合价为+2价,
故答案为:+2;
(2)要从溶液中得到绿矾,可以通过蒸发浓缩,冷却结晶,过滤,洗涤,干燥等步骤,所以实验操作的序号为bcae,
故答案为:bcae;
(3)亚铁离子易水解,在配制硫酸亚铁溶液时要防止亚铁离子水解,所以将绿矾溶于一定浓度的硫酸中可以抑制亚铁离子水解,
故答案为:抑制亚铁离子水解;
(4)①根据题中实验步骤可知,滴定实验达到终点时,溶液中的高锰酸钾不完全褪色,溶液呈浅红色,所以判断滴定实验达到终点的现象是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
②酸性KMnO4被FeSO4还原时生成Mn2+,同时生成铁离子,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
③根据电子得失守恒有关系式MnO4-~5Fe2+,滴定中用去的高锰酸钾的物质的量为0.0100mol/L×0.04L=0.0004mol,所以6.000g绿矾产品中FeSO4•7H2O的物质的量为
×5×0.0004mol=0.02mol,所以样品中FeSO4•7H2O的质量分数为
×100%=92.67%,
故答案为:92.67%;
(5)粗铜电解精炼过程中阴极上是铜离子得电子生成铜单质,电极反应式为Cu2++2e-═Cu,
故答案为:Cu2++2e-═Cu.
故答案为:+2;
(2)要从溶液中得到绿矾,可以通过蒸发浓缩,冷却结晶,过滤,洗涤,干燥等步骤,所以实验操作的序号为bcae,
故答案为:bcae;
(3)亚铁离子易水解,在配制硫酸亚铁溶液时要防止亚铁离子水解,所以将绿矾溶于一定浓度的硫酸中可以抑制亚铁离子水解,
故答案为:抑制亚铁离子水解;
(4)①根据题中实验步骤可知,滴定实验达到终点时,溶液中的高锰酸钾不完全褪色,溶液呈浅红色,所以判断滴定实验达到终点的现象是滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色,
故答案为:滴加最后一滴KMnO4溶液时,溶液变成浅红色且半分钟内不褪色;
②酸性KMnO4被FeSO4还原时生成Mn2+,同时生成铁离子,反应的离子方程式为MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
③根据电子得失守恒有关系式MnO4-~5Fe2+,滴定中用去的高锰酸钾的物质的量为0.0100mol/L×0.04L=0.0004mol,所以6.000g绿矾产品中FeSO4•7H2O的物质的量为
| 250 |
| 25 |
| 0.02×278 |
| 6.000 |
故答案为:92.67%;
(5)粗铜电解精炼过程中阴极上是铜离子得电子生成铜单质,电极反应式为Cu2++2e-═Cu,
故答案为:Cu2++2e-═Cu.
看了利用黄铜矿(CuFeS2)生产...的网友还看了以下:
通过设置基准(枢轴)元素将待排序的序列划分为两个子序列,使得其一个子序列的元素均不大于基准元素,另一 2020-05-26 …
在Excel数据清单中,当以“姓名”字段作为关键字进行排序时,系统可以按“姓名”的()为序排列数据。 2020-05-31 …
任意改变某一个三位数的各位数字的顺序得到一个新数.试证新数与原数之和不能等于999. 2020-06-14 …
我们把壹元硬币有国徽的一面叫做正面,有币值的一面叫做反面.现依次抛出5枚一元硬币,按照抛出的顺序得 2020-06-21 …
1名世与苞同县,亦工为古文,苞为序其集,并逮下狱.2廉能之吏,遇秋籴值贱,得谷较多,应令详明别贮, 2020-06-21 …
/*请在程序的下划线处填入正确的内容并把下划线删除,使程序得出正确的结果.注意:不得增行或删行,也 2020-06-27 …
数据结构:用P表示入栈操作,D表示出栈操作,若元素入栈的顺序为1234,为了得到1342出栈顺序用 2020-06-28 …
=从一批机器零件的毛坯中取出10件,以每个毛坯200g为准,超过的质量为正,不足的为负,得到以下的 2020-07-03 …
二叉树序列中的“层序序列”是什么?在自考题中遇到:已知一颗二叉树的中序序列为“abcdefg",层 2020-07-15 …
书上说:由于三角函数不是单调的,为了得到它们的反函数,对这些函数限定在某个区间内.为什么必须把他们 2020-08-03 …