早教吧作业答案频道 -->化学-->
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如
题目详情
化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理.请回答下列问题:
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:
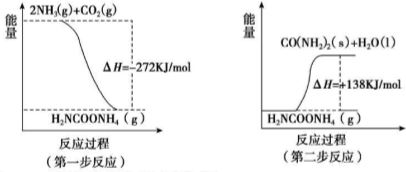
则NH3(g)与CO2(g)反应生成尿素的热化学方程式为___.
(2)已知可逆反应FeO(s)+CO(g)⇌Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表:
①写出该反应平衡常数的表达式___.
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,只改变下列一个条件:升高温度,混合气体的平均相对分子质量___(选填“增大”、“减小”、“不变”);充入氦气,混合气体的密度___(选填“增大”、“减小”、“不变”).
(2)常温下,浓度均为0.l mol•L-1的下列六种溶液的pH如下表:
①上述盐溶液中的阴离子,结合H+能力最强的是___
②根据表中数据判断,浓度均为0.0l mol•L-1的下列五种物质的溶液中,酸性最强的是___(填编号);将备溶液分别稀释100倍,pH变化最小的是___(填编号).
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是___(填编号).
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为___.
(1)工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

则NH3(g)与CO2(g)反应生成尿素的热化学方程式为___.
(2)已知可逆反应FeO(s)+CO(g)⇌Fe(s)+CO2(g)是炼铁工业中一个重要反应,其温度与平衡常数K的关系如表:
| T(K) | 938 | 1100 |
| K | 0.68 | 0.40 |
②若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,只改变下列一个条件:升高温度,混合气体的平均相对分子质量___(选填“增大”、“减小”、“不变”);充入氦气,混合气体的密度___(选填“增大”、“减小”、“不变”).
(2)常温下,浓度均为0.l mol•L-1的下列六种溶液的pH如下表:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
②根据表中数据判断,浓度均为0.0l mol•L-1的下列五种物质的溶液中,酸性最强的是___(填编号);将备溶液分别稀释100倍,pH变化最小的是___(填编号).
A.HCN B.HClO C.C6H5OH D.CH3COOH E.H2CO3
③据上表数据,请你判断下列反应不能成立的是___(填编号).
A.CH3COOH+Na2CO3=NaHCO3+CH3COONa
B.CH3COOH+NaCN=CH3COONa+HCN
C.CO2+H2O+2NaClO=Na2CO3+2HClO
D.CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为___.
▼优质解答
答案和解析
(1)第一步:2NH3(g)+CO2(g)⇌H2NCOONH4(l,氨基甲酸铵)△H1=-272KJ/mol,
第二步:H2NCOONH4(l)⇌H2O(l)+H2NCONH2(s)△H2=+138KJ/mol,
根据盖斯定律,两个过程相加得到NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)⇌H2O(l)+H2NCONH2(s)△H=-134kJ•mol-1;
故答案为:2NH3(g)+CO2(g)⇌H2O(l)+H2NCONH2(s)△H=-134kJ•mol-1;
(2)①根据反应方程式FeO(s)+CO(g)⇌Fe(s)+CO2(g)书写K,表达式为K=
,故答案为:K=
;
②根据表中数据可知,升高温度,K减小,说明平衡逆移,所以正反应为放热反应,因此升高温度平均相对分子质量减小;充入氦气,气体质量增大,体积不变,所以密度增大,故答案为:减小;增大;
(2)①对应酸的酸性越弱,其阴离子越易水解,其阴离子结合质子能力越强,根据表格中数据可知CO32-结合质子能力最强,故答案为:CO32-;
②对应酸的酸性越弱,其阴离子越易水解,其盐溶液碱性越强,所以PH最小的酸性最强,所以CH3COOH酸性最强,在稀释时酸性越弱PH变化越小,pH变化最小的是C6H5OH,故答案为:D;C;
③A.醋酸酸性大于碳酸,所以CH3COOH+Na2CO3=NaHCO3+CH3COONa能发生,故不选;
B.醋酸酸性大于氢氰酸,所以CH3COOH+NaCN=CH3COONa+HCN能发生,故不选;
C.次氯酸酸性小于碳酸而大于碳酸氢根离子,所以CO2+H2O+NaClO=NaHCO3+HClO能发生,故不选;
D.碳酸酸性大于苯酚,碳酸钠会和苯酚之间反应,所以CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH不能发生,故选;
故答案为:D;
④氯水中加入少量的碳酸钠溶液,碳酸钠会与溶液中H+反应,其反应方程为:H++HCO3-=H20+CO2↑,故答案为:H++HCO3-=H20+CO2↑.
第二步:H2NCOONH4(l)⇌H2O(l)+H2NCONH2(s)△H2=+138KJ/mol,
根据盖斯定律,两个过程相加得到NH3(g)与CO2(g)反应生成尿素的热化学方程式为2NH3(g)+CO2(g)⇌H2O(l)+H2NCONH2(s)△H=-134kJ•mol-1;
故答案为:2NH3(g)+CO2(g)⇌H2O(l)+H2NCONH2(s)△H=-134kJ•mol-1;
(2)①根据反应方程式FeO(s)+CO(g)⇌Fe(s)+CO2(g)书写K,表达式为K=
| c(CO2) |
| c(CO) |
| c(CO2) |
| c(CO) |
②根据表中数据可知,升高温度,K减小,说明平衡逆移,所以正反应为放热反应,因此升高温度平均相对分子质量减小;充入氦气,气体质量增大,体积不变,所以密度增大,故答案为:减小;增大;
(2)①对应酸的酸性越弱,其阴离子越易水解,其阴离子结合质子能力越强,根据表格中数据可知CO32-结合质子能力最强,故答案为:CO32-;
②对应酸的酸性越弱,其阴离子越易水解,其盐溶液碱性越强,所以PH最小的酸性最强,所以CH3COOH酸性最强,在稀释时酸性越弱PH变化越小,pH变化最小的是C6H5OH,故答案为:D;C;
③A.醋酸酸性大于碳酸,所以CH3COOH+Na2CO3=NaHCO3+CH3COONa能发生,故不选;
B.醋酸酸性大于氢氰酸,所以CH3COOH+NaCN=CH3COONa+HCN能发生,故不选;
C.次氯酸酸性小于碳酸而大于碳酸氢根离子,所以CO2+H2O+NaClO=NaHCO3+HClO能发生,故不选;
D.碳酸酸性大于苯酚,碳酸钠会和苯酚之间反应,所以CO2+H2O+2C6H5ONa=Na2CO3+2C6H5OH不能发生,故选;
故答案为:D;
④氯水中加入少量的碳酸钠溶液,碳酸钠会与溶液中H+反应,其反应方程为:H++HCO3-=H20+CO2↑,故答案为:H++HCO3-=H20+CO2↑.
看了化学学科中的化学平衡、电离平衡...的网友还看了以下:
气态PCl5的分解反应为2PCl5(g)⇌2PCl3(g)+2Cl2(g),在473K达到平衡时气 2020-04-07 …
如图所示的杠杆处于平衡,把A端所挂重物浸没在水中,杠杆将失去平衡,为使杠杆重新平衡应()A.将支点 2020-05-16 …
关于化学平衡及其移动的一些小疑惑,在可逆反应2SO2+O2=(可逆)=2SO3中,如果恒温恒容的情 2020-05-22 …
小刚用带有均匀刻度的杠杆和若干质量相同的钩码,验证杠杆的平衡条件.(1)杠杆组装后,如图甲所示.他 2020-06-20 …
下列事实中,不能用勒夏特列原理解释的是A.溴水中有下列平衡,当加入溶液后,溶液颜色变浅B.对平衡体 2020-06-26 …
下列对沉淀溶解平衡的描述正确的是()A.反应开始时,溶液中各离子浓度相等B.沉淀溶解达到平衡时,沉 2020-07-26 …
怎样使用天平天平有没有检查天平底座是否水平的装置?应怎样调平?衡量指针在什么位置时表示横梁平衡了?如 2020-11-02 …
放热反应CO(g)+H2O(g)CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H 2020-12-25 …
怎样使用天平天平有没有检查天平底座是否水平的装置?应怎样调平?衡量指针在什么位置时表示横梁平衡了?如 2021-01-01 …
已建立化学平衡的可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述中正确的是()A.生成 2021-01-22 …