早教吧作业答案频道 -->化学-->
图1是硫元素在自然界的循环情况.(1)有关叙述中不正确的是(填序号)a.自然界不存在游离态的硫b.部分硫元素由地壳到大气的过程发生了氧化反应c.图1显示大气中的二氧化硫最终
题目详情
图1是硫元素在自然界的循环情况.
(1)有关叙述中不正确的是___(填序号)
a.自然界不存在游离态的硫
b.部分硫元素由地壳到大气的过程发生了氧化反应
c.图1显示大气中的二氧化硫最终回到海洋并很快和其它矿物形成煤和石油
d.葡萄酒中含有二氧化硫可防止葡萄酒被氧化
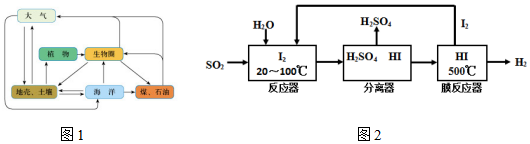
(2)硫铁矿(FeS2)燃烧产生的SO2通过下列碘循环工艺过程既能制H2SO4,又能制H2而获得清洁能源.
①该循环工艺过程的总反应方程式为___.
②FeS2可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式___
③用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是___.
④已知下列三个反应:
a Cl(g)+H(g)═HCl(g)△H1 b Br(g)+H(g)═HBr(g)△H2 c I(g)+H(g)═HI(g)△H3
则△H1、△H2、△H3由大到小的顺序为___,用原子结构解释原因___.
(3)工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.
表是不同压强、温度时SO2的转化率情况.
工业中SO2转化为SO3通常采用400℃~500℃、压强1.0MPa,而不选择更高的10MPa.其原因是___.
(4)下列事实能说明H2SO3的酸性强于H2CO3的是___
a.饱和H2SO3溶液的pH小于饱和H2CO3溶液的pH.
b.同温下,等浓度的NaHSO3和NaHCO3溶液,后者的pH值大.
c.H2SO3能使酸性高锰酸钾溶液褪色,而H2CO3不能.
d.将过量SO2气体通入NaHCO3溶液中,逸出的气体能使澄清石灰水变浑浊.

(1)有关叙述中不正确的是___(填序号)
a.自然界不存在游离态的硫
b.部分硫元素由地壳到大气的过程发生了氧化反应
c.图1显示大气中的二氧化硫最终回到海洋并很快和其它矿物形成煤和石油
d.葡萄酒中含有二氧化硫可防止葡萄酒被氧化
(2)硫铁矿(FeS2)燃烧产生的SO2通过下列碘循环工艺过程既能制H2SO4,又能制H2而获得清洁能源.
①该循环工艺过程的总反应方程式为___.
②FeS2可和盐酸发生复分解反应生成一种不稳定的液态化合物,该化合物的电子式___
③用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出H2的目的是___.
④已知下列三个反应:
a Cl(g)+H(g)═HCl(g)△H1 b Br(g)+H(g)═HBr(g)△H2 c I(g)+H(g)═HI(g)△H3
则△H1、△H2、△H3由大到小的顺序为___,用原子结构解释原因___.
(3)工业制硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤.
表是不同压强、温度时SO2的转化率情况.
压强 温度℃ | 0.2Mpa | 1.0Mp | 10Mpa |
| 400 | 97.2% | 99.5% | 99.7% |
| 500 | 91.5% | 96.9% | 97.8% |
| 600 | 72.6% | 85.8% | 89.5% |
(4)下列事实能说明H2SO3的酸性强于H2CO3的是___
a.饱和H2SO3溶液的pH小于饱和H2CO3溶液的pH.
b.同温下,等浓度的NaHSO3和NaHCO3溶液,后者的pH值大.
c.H2SO3能使酸性高锰酸钾溶液褪色,而H2CO3不能.
d.将过量SO2气体通入NaHCO3溶液中,逸出的气体能使澄清石灰水变浑浊.
▼优质解答
答案和解析
(1)a.自然界中存在游离态的硫,如火山口存在游离态的硫,故a错误;
b.硫单质和氧气反应生成二氧化硫,火山爆发时地壳中的硫和氧气反应生成二氧化硫,所以部分硫元素由地壳到大气的过程发生了氧化反应,故b正确;
c.形成煤和石油的过程是一个漫长过程,所以该说法错误,故c错误;
d.二氧化硫具有还原性,能被强氧化剂氧化,葡萄酒中含有二氧化硫被氧化,所以可防止葡萄酒被氧化,故d正确;
故选a c;
(2)①根据流程图知,碘在经过一系列的反应后又生成碘,只有二氧化硫和水参加反应,生成硫酸和氢气,反应方程式为SO2+2H2O=H2+H2SO4,故答案为:SO2+2H2O=H2+H2SO4;
②二者发生复分解反应生成氯化亚铁和H2S2,H2S2和双氧水分子结构相似,其电子式为 ,
,
故答案为: ;
;
③分离出氢气导致产物浓度减小,平衡正向移动,提高HI的分解率,
故答案为:减小生成物浓度,平衡正向移动,提高HI的分解率;
④Cl、Br、I都属于同一主族元素,其非金属性随着原子序数增大而减弱,其氢化物的稳定性随着原子序数增大而减弱,物质的能量越高,越不稳定,所以HI能量最高,I和H反应放出的能量最低,因为焓变小于0,所以△H3>△H2>△H1,
故答案为:△H3>△H2>△H1;
(3)根据表中数据知,同一压强下,升高温度二氧化硫的转化率降低,说明正反应是放热反应;同一温度下,压强增大10倍,转化率几乎不变,且对设备要求增大,从而降低经济效益,则压强选择1.0MPa,
故答案为:压强增大10倍,转化率几乎不变;
(4)a.饱和H2SO3溶液和饱和H2CO3溶液的浓度不同,所以不能根据这两种物质的饱和溶液pH大小判断酸性强弱,故错误;
b.同温下,酸的酸性越强,其相同浓度的酸式盐的pH越小,所以同温下,等浓度的NaHSO3和NaHCO3溶液,后者的pH值大,所以说明碳酸的酸性小于亚硫酸,故正确;
c.酸性高锰酸钾溶液具有强氧化性,能氧化还原性物质,该实验中说明亚硫酸具有还原性,碳酸没有还原性,所以不能比较亚硫酸和碳酸酸性强弱,故错误;
d.二氧化硫和二氧化碳都能使澄清石灰水变浑浊,因为该题中二氧化硫是过量的,澄清石灰水变浑浊不能说明是否产生二氧化碳,则不能说明酸性强弱,故错误;
故选b.
b.硫单质和氧气反应生成二氧化硫,火山爆发时地壳中的硫和氧气反应生成二氧化硫,所以部分硫元素由地壳到大气的过程发生了氧化反应,故b正确;
c.形成煤和石油的过程是一个漫长过程,所以该说法错误,故c错误;
d.二氧化硫具有还原性,能被强氧化剂氧化,葡萄酒中含有二氧化硫被氧化,所以可防止葡萄酒被氧化,故d正确;
故选a c;
(2)①根据流程图知,碘在经过一系列的反应后又生成碘,只有二氧化硫和水参加反应,生成硫酸和氢气,反应方程式为SO2+2H2O=H2+H2SO4,故答案为:SO2+2H2O=H2+H2SO4;
②二者发生复分解反应生成氯化亚铁和H2S2,H2S2和双氧水分子结构相似,其电子式为
 ,
,故答案为:
 ;
;③分离出氢气导致产物浓度减小,平衡正向移动,提高HI的分解率,
故答案为:减小生成物浓度,平衡正向移动,提高HI的分解率;
④Cl、Br、I都属于同一主族元素,其非金属性随着原子序数增大而减弱,其氢化物的稳定性随着原子序数增大而减弱,物质的能量越高,越不稳定,所以HI能量最高,I和H反应放出的能量最低,因为焓变小于0,所以△H3>△H2>△H1,
故答案为:△H3>△H2>△H1;
(3)根据表中数据知,同一压强下,升高温度二氧化硫的转化率降低,说明正反应是放热反应;同一温度下,压强增大10倍,转化率几乎不变,且对设备要求增大,从而降低经济效益,则压强选择1.0MPa,
故答案为:压强增大10倍,转化率几乎不变;
(4)a.饱和H2SO3溶液和饱和H2CO3溶液的浓度不同,所以不能根据这两种物质的饱和溶液pH大小判断酸性强弱,故错误;
b.同温下,酸的酸性越强,其相同浓度的酸式盐的pH越小,所以同温下,等浓度的NaHSO3和NaHCO3溶液,后者的pH值大,所以说明碳酸的酸性小于亚硫酸,故正确;
c.酸性高锰酸钾溶液具有强氧化性,能氧化还原性物质,该实验中说明亚硫酸具有还原性,碳酸没有还原性,所以不能比较亚硫酸和碳酸酸性强弱,故错误;
d.二氧化硫和二氧化碳都能使澄清石灰水变浑浊,因为该题中二氧化硫是过量的,澄清石灰水变浑浊不能说明是否产生二氧化碳,则不能说明酸性强弱,故错误;
故选b.
看了图1是硫元素在自然界的循环情况...的网友还看了以下:
读了元帅的马你从故事明白了什么道理?想一想,写出一句自己的格言 2020-06-08 …
1368年,推翻了元朝的统治,建立了明朝的农民起义领袖是()A、朱元璋B、李自成C、洪秀全D、李世 2020-06-09 …
元代堪称中国戏曲黄金时代,后人评价元曲“文而不晦”、“俗而不俚”、“明白如话”。这主要肯定了元曲的 2020-07-12 …
单位换算.元/克换成元/千克,元/千克就是元/(克*1000),就是元/克/1000.就是说元/克 2020-07-16 …
一道我见过的悖论题三个人去旅馆住店,每人交了10元钱.然后回到了各自的房间.老板说今天过节,于是退 2020-07-24 …
我们的班级多热闹!上学期我班举行了'我的学校我的家庆元旦主题班会",同学们拿出了各自的看家本领,精彩 2020-11-14 …
在思想品德课上,七(5)班的同学对如何正确认识自己发表了各自的看法:王建:“认识自己太容易了,自己都 2020-11-23 …
“不读书有权,不识字有钱,不晓事倒有人夸荐”,此例典型地说明了元曲的特征是①音节和用韵上比较自由②语 2020-11-28 …
人教版九年级化学的比较好的讲课顺序感觉教材安排多少有点问题,比如第三单元涉及到了元素的描述,但是第四 2020-11-28 …
《世说新语陈太丘与友期》中元方入门不顾,这是不是元方无礼的行为?《世说新语》之《陈太丘与友期》中,陈 2020-12-19 …