早教吧作业答案频道 -->化学-->
物质M是一种日常生活中不可缺少的调味品.已知C在D中燃烧发生苍白色火焰,M与其他物质的转化关系如图甲所示(部分产物已略去);(1)写出用惰性电极电解M溶液的离子方程式.(2)
题目详情
物质M是一种日常生活中不可缺少的调味品.已知C在D中燃烧发生苍白色火焰,M与其他物质的转化关系如图甲所示(部分产物已略去);
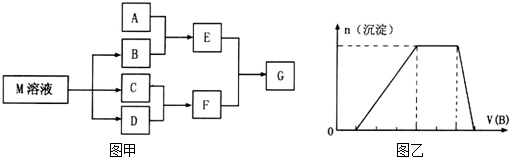
(1)写出用惰性电极电解M溶液的离子方程式___.
(2)比较B中各元素原子半径大小___(填元素符号).
(3)若A是一种酸性氧化物,且可用于制造玻璃,则G的化学式是___.
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是___.
(5)若A是一种溶液,只可能含有H+,NH4+,Mg2+,Fe3+,Al3+,CO32-,SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图乙所示.由此可知,该溶液中肯定含有的离子及其浓度之比为___.
(6)若E可用于检验葡萄糖的存在,写出G溶液充分蒸发灼烧后的产物与乙醇反应的化学方程式___.
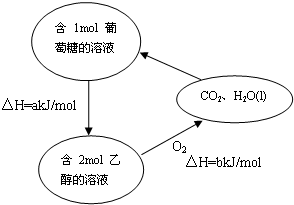
(7)根据下图,写出25℃时由CO2和H2O转化为葡萄糖溶液的化学方程式___.

(1)写出用惰性电极电解M溶液的离子方程式___.
(2)比较B中各元素原子半径大小___(填元素符号).
(3)若A是一种酸性氧化物,且可用于制造玻璃,则G的化学式是___.
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是___.
(5)若A是一种溶液,只可能含有H+,NH4+,Mg2+,Fe3+,Al3+,CO32-,SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图乙所示.由此可知,该溶液中肯定含有的离子及其浓度之比为___.
(6)若E可用于检验葡萄糖的存在,写出G溶液充分蒸发灼烧后的产物与乙醇反应的化学方程式___.
(7)根据下图,写出25℃时由CO2和H2O转化为葡萄糖溶液的化学方程式___.

▼优质解答
答案和解析
(1)C可在D中燃烧发出苍白色火焰,为氢气与氯气反应生成HCl,可推知C为H2、D为Cl2、F为HCl,M是日常生活中不可缺少的调味品,由转化关系可知,M的溶液电解生成氢气、氯气与B,可推知M为NaCl、B为NaOH,用惰性电极电解M溶液的离子方程式为2Cl-+2H2O
2OH-+H2↑+Cl2↑,
故答案为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;
(2)B为NaOH,根据原子电子层数越多半径越大,电子层数相同时则核电荷数越多,半径越小,所以NaOH中各元素原子半径大小为Na>O>H,
故答案为:Na>O>H;
(3)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2,E为Na2SiO3,与F溶液反应可以得到G为H2SiO3,
故答案为:H2SiO3;
(4)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+,一定没有CO32-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+,一定含有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则含有NH4+,由电荷守恒可知一定含有SO42-,
发生反应H++OH-=H2O,氢离子消耗NaOH溶液的体积为1积,
发生反应Al3++3OH-=Al(OH)3↓,铝离子消耗NaOH溶液的体积为3体积,
发生反应NH4++OH-=NH3•H2O,铵根消耗氢氧化钠为2体积,
则n(H+):n(Al3+):n(NH4+)=1:1:2,由电荷守恒可知,n(H+):n(Al3+):n(NH4+):n(SO42-)=1:1:2:3,故c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3,
故答案为:c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3;
(6)若E可用于检验葡萄糖的存在,则E为氢氧化铜,E和F生成G,则G为氯化铜,由于铜离子能水解,氯化把易挥发,所以氯化铜溶液充分蒸发灼烧后的产物为氧化铜,氧化铜与乙醇发生氧化还原反应生成铜和乙醛,反应方程式为2CH3CH2OH+CuO
2CH3CHO+Cu+2H2O,
故答案为:2CH3CH2OH+CuO
2CH3CHO+Cu+2H2O;
(7)根据图中各物质转化关系及元素守恒可写出由CO2和H2O转化为葡萄糖溶液的化学方程式为6CO2(g)+6H2O(l)
C6H12O6(aq)+2H2O(g),
故答案为:6CO2(g)+6H2O(l)
C6H12O6(aq)+2H2O(g).
| ||
故答案为:2Cl-+2H2O
| ||
(2)B为NaOH,根据原子电子层数越多半径越大,电子层数相同时则核电荷数越多,半径越小,所以NaOH中各元素原子半径大小为Na>O>H,
故答案为:Na>O>H;
(3)若A是一种常见的酸性氧化物,且可用于制造玻璃,则A为SiO2,E为Na2SiO3,与F溶液反应可以得到G为H2SiO3,
故答案为:H2SiO3;
(4)由图可知,开始加入NaOH没有沉淀和气体产生,则一定有H+,一定没有CO32-,后来有沉淀产生且最后消失,则一定没有Mg2+、Fe3+,一定含有Al3+;中间段沉淀的质量不变,应为NH4++OH-=NH3•H2O的反应,则含有NH4+,由电荷守恒可知一定含有SO42-,
发生反应H++OH-=H2O,氢离子消耗NaOH溶液的体积为1积,
发生反应Al3++3OH-=Al(OH)3↓,铝离子消耗NaOH溶液的体积为3体积,
发生反应NH4++OH-=NH3•H2O,铵根消耗氢氧化钠为2体积,
则n(H+):n(Al3+):n(NH4+)=1:1:2,由电荷守恒可知,n(H+):n(Al3+):n(NH4+):n(SO42-)=1:1:2:3,故c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3,
故答案为:c(H+):c(Al3+):c(NH4+):c(SO42-)=1:1:2:3;
(6)若E可用于检验葡萄糖的存在,则E为氢氧化铜,E和F生成G,则G为氯化铜,由于铜离子能水解,氯化把易挥发,所以氯化铜溶液充分蒸发灼烧后的产物为氧化铜,氧化铜与乙醇发生氧化还原反应生成铜和乙醛,反应方程式为2CH3CH2OH+CuO
| △ |
故答案为:2CH3CH2OH+CuO
| △ |
(7)根据图中各物质转化关系及元素守恒可写出由CO2和H2O转化为葡萄糖溶液的化学方程式为6CO2(g)+6H2O(l)
| △ |
故答案为:6CO2(g)+6H2O(l)
| △ |
看了物质M是一种日常生活中不可缺少...的网友还看了以下:
化学用语是学习化学的重要工具,请用化学用语回答下列问题:(1)红磷在空气中燃烧产物的化学式;(2) 2020-04-11 …
化学用语是国际通用的化学语言,是学习化学的重要工具,请用化学用语回答下列问题:(1)红磷在空气中燃 2020-05-02 …
文斗乡贺家湾正在建设液化气站,估计2016年底文斗集镇基本上可使用液化然气.用燃气灶烧水时,把2. 2020-05-13 …
纯碱、烧碱等是重要的化工原料.(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应.将A与 2020-05-14 …
(1)家用液化气的主要成分之一是丁烷(C4H10),当1kg丁烷完全燃烧生成二氧化碳和液态水时,放 2020-05-14 …
家用液化气中的主要成分之一是丁烷(大4H10).已知1mol液态水汽化时需要吸收44KJ热量.(1 2020-05-14 …
烧碱液是什么 有碱性还是酸性 还是都有啊 2020-05-16 …
纯碱溶于水的水溶液最好要用什么容器储存?可以用水泥糟直接储存或是在水槽表面上铺一层塑料袋?关于烧碱 2020-07-04 …
烧杯为什么会被烧炸?实验室的烧杯为什么在给溶液加热时会突然烧炸了?疑惑?石棉网垫了溶液就是配好的只要 2020-11-10 …
药厂废酒精浓度约70%,其中含有较强的硫酸味,点燃时酒精水溶液表面会起白雾和强酸味,加入烧碱能不能去 2020-11-30 …