早教吧作业答案频道 -->化学-->
低碳生活是一种时尚的生活理念,如何有效地开发利用碳资源以及降低大气中CO2的含量的研究显得更加紧迫.(1)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),
题目详情
低碳生活是一种时尚的生活理念,如何有效地开发利用碳资源以及降低大气中CO2的含量的研究显得更加紧迫.
(1)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生 成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
①请结合上表数据,写出NO与活性炭反应的化学方程式___.
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2.
Ⅰ.计算K1=___,
Ⅱ.根据上述信息判断,温度T1和T2的关系是(填序号)___.
a.T1>T2 b.T1<T2 c.无法比较
(2)CO2在实验室常用氢氧化钠来吸收,现有8.96L CO2(标态),若用200ml 3mol/LNaOH 溶液将其恰好完全吸收,反应的离子方程式为___,所得溶液中离子浓度由大到小的顺序为___.
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.现将浓度为2×10-4
mo1/L Na2CO3溶液与等体积的CaCl2溶液混合,则生成沉淀所需CaCl2溶液的最小浓度为___.
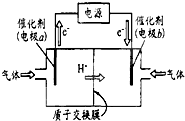
(4)若用如右图装置,以CO2和H2为原料制备甲醇,发生 反应为CO2+3H2
CH3OH+H2O,则b电极的电极反应为___.

(1)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生 成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
物质T/℃n/mol T/℃ | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2.
Ⅰ.计算K1=___,
Ⅱ.根据上述信息判断,温度T1和T2的关系是(填序号)___.
a.T1>T2 b.T1<T2 c.无法比较
(2)CO2在实验室常用氢氧化钠来吸收,现有8.96L CO2(标态),若用200ml 3mol/LNaOH 溶液将其恰好完全吸收,反应的离子方程式为___,所得溶液中离子浓度由大到小的顺序为___.
(3)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9.现将浓度为2×10-4
mo1/L Na2CO3溶液与等体积的CaCl2溶液混合,则生成沉淀所需CaCl2溶液的最小浓度为___.
(4)若用如右图装置,以CO2和H2为原料制备甲醇,发生 反应为CO2+3H2
| ||
▼优质解答
答案和解析
(1)①由表中数据可知,C、NO、E、F的化学计量数之比为0.03:0.06:0.03:0.03=1:2:1:1,反应中C被氧化,结合原子守恒可知,生成为N2与CO2,且该反应为可逆反应,故反应方程式为:C+2NO⇌N2+CO2,
故答案为:C+2NO⇌N2+CO2;
②Ⅰ、平衡时c(NO)=
=0.02mol/L,c(N2)=c(CO2)=
=0.015mol/L,故T1℃时该反应的平衡常数为K1=
=
,故答案为:
;
Ⅱ、由表中数据可知,温度由T1变为T2,平衡向逆反应移动,由于正反应是吸热,还是放热不确定,无法判断温度变化,故答案为:c;
(2)根据二氧化碳和氢氧化钠之间反应量的关系:按照1:1反应,产物是碳酸氢钠,按照1:2反应,产物是碳酸钠,标准状况下8.96L CO2是0.4mol,0.4molCO2和200mL 3mol/L NaOH溶液混合,二者的物质的量之比是2:3,所的溶液是碳酸钠和碳酸氢钠的混合物离子方程式为:2CO2+3OH-=HCO3-+CO32-+H2O;混合物显碱性c(OH-)>c(H+),碳酸根离子水解程度大与碳酸氢根离子的水解程度,所以c(CO32-)<c(HCO3-),即c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:2CO2+3OH-=HCO3-+CO32-+H2O;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
(3)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=
×2×10-4mol/L=1×10-4mol/L,根据Ksp=c(CO32-)•c(Ca2+)=2.8×10-9可知,c(Ca2+)=
mol/L=2.8×10-5mol/L,原溶液CaCl2溶液的最小浓度为混合溶液中c(Ca2+)的2倍,故原溶液CaCl2溶液的最小浓度为2×2.8×10-5mol/L=5.6×10-5mol/L.
故答案为:5.6×10-5mol/L;
(4)据电子移动方向分析,b为阴极,阴极发生还原反应,CO2在阴极发生还原反应,电极反应式为:CO2+6H++6e-=CH3OH+H2O,故答案为:CO2+6H++6e-=CH3OH+H2O.
故答案为:C+2NO⇌N2+CO2;
②Ⅰ、平衡时c(NO)=
| 0.04mol |
| 2L |
| 0.03mol |
| 2L |
| 0.015×0.015 |
| 0.022 |
| 9 |
| 16 |
| 9 |
| 16 |
Ⅱ、由表中数据可知,温度由T1变为T2,平衡向逆反应移动,由于正反应是吸热,还是放热不确定,无法判断温度变化,故答案为:c;
(2)根据二氧化碳和氢氧化钠之间反应量的关系:按照1:1反应,产物是碳酸氢钠,按照1:2反应,产物是碳酸钠,标准状况下8.96L CO2是0.4mol,0.4molCO2和200mL 3mol/L NaOH溶液混合,二者的物质的量之比是2:3,所的溶液是碳酸钠和碳酸氢钠的混合物离子方程式为:2CO2+3OH-=HCO3-+CO32-+H2O;混合物显碱性c(OH-)>c(H+),碳酸根离子水解程度大与碳酸氢根离子的水解程度,所以c(CO32-)<c(HCO3-),即c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:2CO2+3OH-=HCO3-+CO32-+H2O;c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
(3)Na2CO3溶液的浓度为2×10-4mol/L,等体积混合后溶液中c(CO32-)=
| 1 |
| 2 |
| 2.8×10-9 |
| 1×10-4 |
故答案为:5.6×10-5mol/L;
(4)据电子移动方向分析,b为阴极,阴极发生还原反应,CO2在阴极发生还原反应,电极反应式为:CO2+6H++6e-=CH3OH+H2O,故答案为:CO2+6H++6e-=CH3OH+H2O.
看了低碳生活是一种时尚的生活理念,...的网友还看了以下:
下列说法不正确的是()A.焦炭在高温下与水蒸气的反应是吸热反应B.吸热反应一定是反应物总能量低于生 2020-04-11 …
与液;/晶数码显示器相比,LED数码显示器具有亮度高且耗电量低的优点。( ) 2020-06-07 …
资料显示,我国拥有的淡水资源总量低于巴西、俄罗斯、加拿大、美国和印度尼西亚,居世界第6位。但由于人 2020-07-16 …
显微镜的低倍镜是哪个我们学校显微镜低倍镜高倍镜长一个样子,一样长,一个红的一个黄的,老师说对光用低 2020-07-23 …
硝酸铵溶于水,溶液温度显著降低是由于A硝酸铵溶于水只有扩散过程B硝酸铵溶解时,水合过程吸收的热量大 2020-07-29 …
3月22日是“世界水日”,有关水的认识正确的是()A.生活中用活性炭降低水的硬度B.将FeCl3、蔗 2020-11-02 …
焦炭和水蒸气高温反应吸热还是放热?如题.吸热反应一定是反应物总能量低于生成物总能量么? 2020-11-05 …
生活中的物理奇妙的电路在汽车的仪表盘上有一个油量表来显示油箱内汽油的余量,当汽油的余量低于一定值时, 2020-11-29 …
广东煤矿规模小,煤炭质量低,全省煤炭年产量仅800多万吨,在全省经济中所占份额很小,且大部分煤矿证照 2020-12-01 …
下列关于山西省煤炭资源开发条件的说法正确的是①煤炭资源丰富②市场广阔但交通落后③埋藏层浅④位置适中⑤ 2020-12-03 …