早教吧作业答案频道 -->化学-->
为了测定一份由纯碱、氢氧化钠和杂质(杂质不溶于水,不与其它物质反应)组成的固体样品中氢氧化钠的质量分数,某化学探究小组进行了如下实验:(1)发生中和反应的化学方程式是
题目详情
为了测定一份由纯碱、氢氧化钠和杂质(杂质不溶于水,不与其它物质反应)组成的固体样品中氢氧化钠的质量分数,某化学探究小组进行了如下实验:
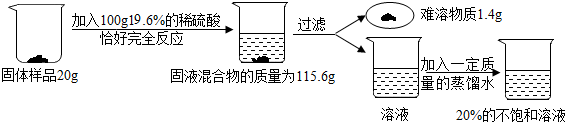
(1)发生中和反应的化学方程式是___;
(2)求解样品中生成气体的物质的质量 (X)的比例式为___;
(3)样品中烧碱的质量分数为___;
(4)(若实验在25℃时进行)向过滤后所得滤液中加入一定质量的蒸馏水,最终得到质量分数为20%的只含一种溶质的不饱和溶液,则加入水的体积为___mL (水的密度为1g/cm3);
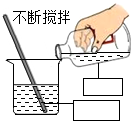
(5)若用98%的浓硫酸配制实验中所用的稀硫酸,在图中标出浓硫酸与蒸馏水的质量.


(1)发生中和反应的化学方程式是___;
(2)求解样品中生成气体的物质的质量 (X)的比例式为___;
(3)样品中烧碱的质量分数为___;
(4)(若实验在25℃时进行)向过滤后所得滤液中加入一定质量的蒸馏水,最终得到质量分数为20%的只含一种溶质的不饱和溶液,则加入水的体积为___mL (水的密度为1g/cm3);
(5)若用98%的浓硫酸配制实验中所用的稀硫酸,在图中标出浓硫酸与蒸馏水的质量.
▼优质解答
答案和解析
(1)氢氧化钠和硫酸反应生成硫酸钠和水,化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O;
(2)生成二氧化碳的质量为:100g+20g-115.6g=4.4g,
设参加反应的碳酸钠质量为x,生成硫酸钠质量为y,消耗硫酸质量为m
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 98 142 44
x m y 4.4g
=
=
=
x=10.6g
y=14.2g
m=9.8g
所以与氢氧化钠反应的硫酸质量为:100g-
=50g,
(3)所以样品中烧碱的质量分数为:
×100%=47%;
(4)设氢氧化钠和硫酸反应生成的硫酸钠为z
2NaOH+H2SO4=Na2SO4+2H2O
98 142
50g×19.6% z
=
z=14.2g
所以共生成硫酸钠质量为:14.2g×2=28.4g,
滤液的质量为:115.6g-1.4g=114.2g
设需要加水的质量为n
(114.2g+n)×20%=28.4g
n=27.8g
所以水的体积为:27.8mL;
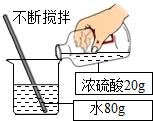
(5)需要浓硫酸的质量为:
=20g,需要水的质量为:100g-20g=80g
故答案为:(1)2NaOH+H2SO4=Na2SO4+2H2O;
(2)
=
;
(3)47%;
(4)27.8;
(5)

(2)生成二氧化碳的质量为:100g+20g-115.6g=4.4g,
设参加反应的碳酸钠质量为x,生成硫酸钠质量为y,消耗硫酸质量为m
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 98 142 44
x m y 4.4g
| 106 |
| x |
| 142 |
| y |
| 44 |
| 4.4g |
| 98 |
| m |
x=10.6g
y=14.2g
m=9.8g
所以与氢氧化钠反应的硫酸质量为:100g-
| 9.8g |
| 19.6% |
(3)所以样品中烧碱的质量分数为:
| 20g-10.6g |
| 20g |
(4)设氢氧化钠和硫酸反应生成的硫酸钠为z
2NaOH+H2SO4=Na2SO4+2H2O
98 142
50g×19.6% z
| 98 |
| 50g×19.6% |
| 142 |
| z |
z=14.2g
所以共生成硫酸钠质量为:14.2g×2=28.4g,
滤液的质量为:115.6g-1.4g=114.2g
设需要加水的质量为n
(114.2g+n)×20%=28.4g
n=27.8g
所以水的体积为:27.8mL;
(5)需要浓硫酸的质量为:
| 100g×19.6% |
| 98% |

故答案为:(1)2NaOH+H2SO4=Na2SO4+2H2O;
(2)
| 106 |
| x |
| 44 |
| 4.4g |
(3)47%;
(4)27.8;
(5)

看了 为了测定一份由纯碱、氢氧化钠...的网友还看了以下:
钾是活泼的碱金属,钾和氧有氧化钾、过氧化钾和超氧化钾等多种化合物.某过氧化钾样品中氧的质量分数(杂 2020-04-08 …
为了测定一份由纯碱、氢氧化钠和杂质(杂质不溶于水,不与其它物质反应)组成的固体样品中氢氧化钠的质量 2020-05-14 …
九年级化学计算题,在线等!有含杂质的氧化铜样品40g,加入稀硫酸完全反应后,共用去稀硫酸368g, 2020-05-16 …
有杂质的氧化铜样品40g,加入稀盐酸完全反映后,共用去368g,过滤的滤渣8g(杂质既不溶于水,也 2020-05-22 …
有含杂质的氧化铜样品40g,加入稀硫酸完全反应后,共用去稀硫酸368g.过滤得滤渣8g(杂质不溶水 2020-05-22 …
煅烧250t含杂质的石灰石(杂质不参与反应、不分解),完全分解后,剩余固体的质量变为162t,请计 2020-07-18 …
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2 2020-07-22 …
将55克含杂质铜的干燥氧化铜试样放入试管中,先通氢气(足量)后加热,将完全反应后冷却称得残留物45克 2020-11-01 …
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与H2S 2020-12-16 …
25g石灰石(有杂质)与100g稀盐酸恰好完全反应(杂质不溶解,也不参加反应),此时烧杯中物质的总质 2021-02-06 …