早教吧作业答案频道 -->化学-->
Al2O3、Al(OH)3都是重要化工原料.根据要求回答问题:Ⅰ、电解法制高品质Al(OH)3装置如图(中间用离子交换膜隔开):4Na[Al(OH)4]+2H2O通电
题目详情
Al2O3、Al(OH)3都是重要化工原料.根据要求回答问题:
Ⅰ、电解法制高品质Al(OH)3装置如图(中间用离子交换膜隔开):
4Na[Al(OH)4]+2H2O
4Al(OH)3↓+4NaOH+O2↑+2H2↑
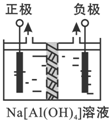
(1)产物Al(OH)3在___区(填“阴极”或“阳极”)沉积;
(2)电解中转移2mol e-时,将制得___mol的Al(OH)3.
Ⅱ、制取纳米Al2O3需要纯净的硫酸铝.现有0.05mol•L-1硫酸铝溶液,经检测,含有Fe2+、Fe3+.可按下述操作提纯:往溶液中加足量H2O2充分反应,再用试剂X调节溶液pH=3.5.(室温下,0.1mol•L-1的Fe2+、Al3+开始沉淀的pH分别为7.0和3.7,Fe3+完全沉淀的pH=3.2)
(3)纳米氧化铝分散在分散剂中将形成胶体.则纳米氧化铝的直径约为___m.
(4)检验硫酸铝溶液含有Fe3+时,所采用的试剂及现象是___.
(5)往溶液中加入H2O2的作用是___(用离子方程式表示).
(6)加入的X试剂(填选项编号)是___.
A.CuO B.Al(OH)3 C.NaOH D.NaHCO3
若调节后溶液的pH偏离3.5,可能带来的后果是___.
Ⅰ、电解法制高品质Al(OH)3装置如图(中间用离子交换膜隔开):
4Na[Al(OH)4]+2H2O
| ||

(1)产物Al(OH)3在___区(填“阴极”或“阳极”)沉积;
(2)电解中转移2mol e-时,将制得___mol的Al(OH)3.
Ⅱ、制取纳米Al2O3需要纯净的硫酸铝.现有0.05mol•L-1硫酸铝溶液,经检测,含有Fe2+、Fe3+.可按下述操作提纯:往溶液中加足量H2O2充分反应,再用试剂X调节溶液pH=3.5.(室温下,0.1mol•L-1的Fe2+、Al3+开始沉淀的pH分别为7.0和3.7,Fe3+完全沉淀的pH=3.2)
(3)纳米氧化铝分散在分散剂中将形成胶体.则纳米氧化铝的直径约为___m.
(4)检验硫酸铝溶液含有Fe3+时,所采用的试剂及现象是___.
(5)往溶液中加入H2O2的作用是___(用离子方程式表示).
(6)加入的X试剂(填选项编号)是___.
A.CuO B.Al(OH)3 C.NaOH D.NaHCO3
若调节后溶液的pH偏离3.5,可能带来的后果是___.
▼优质解答
答案和解析
(1)电解本质是电解水,阴极上水放电生成氢气与氢氧根离子,阳极上水放电生成生成氧气与氢离子,氢离子再与[Al(OH)4]-反应生成Al(OH)3,故产物Al(OH)3在阳极区沉积,故答案为:阳极;(2)根据电子转移守恒,...
看了 Al2O3、Al(OH)3都...的网友还看了以下:
下列溶液氯离子的物质的量浓度与50ml 1mol/L氯化铝溶液中氯离子的物质的量浓度相等的是a 1 2020-04-06 …
将同一植物细胞依次浸于蒸馏水、0.3mol/L的蔗糖溶液和0.5mol/L的尿素溶液,观察到原生质 2020-05-15 …
常温下,向20mL0.2mol·L-1H2A溶液中滴加0.2mol·L-1NaOH溶液.有关微粒的 2020-05-17 …
重络酸钾配制实验操作配制0.1mol/l的重络酸钾溶液1、配制1mol/l重络酸钾溶液2、稀释1溶 2020-05-22 …
超难单位换算问题如何将L/km化为kg/min算的是汽车耗油量,汽车官方网站都是用L/km作单位的 2020-06-09 …
向100mL0.1mol•L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol•L- 2020-06-12 …
反应:A═2B中,A、B的浓度变化如图所示.则2min以内的平均反应的速率为()A.vA=9mol 2020-06-12 …
种子萌发的过程干重和鲜重种子萌发过程中干重和鲜重如何变化.如何由干重的变化判断鲜重的变化以及判断呼 2020-06-26 …
在一根弹簧下端悬挂重物,改变并记录重物的质量.观察并记录弹簧长度的变化,探索它们的变化规律,如果弹 2020-07-21 …
(2011•湘潭)两个全等的直角三角形重叠放在直线l上,如图(1),AB=6cm,BC=8cm,∠A 2020-11-12 …