早教吧作业答案频道 -->化学-->
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等,回答下列问题:(1)铅与碳是同族元素,则下列说法正确的是.a.主要化合价为+2、+4b.同族的Si与Ge(锗)均为半导体材料,
题目详情
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等,回答下列问题:
(1)铅与碳是同族元素,则下列说法正确的是___.
a.主要化合价为+2、+4
b.同族的Si与Ge(锗)均为半导体材料,铅也为半导体材料.
c.铅的最高价氧化物对应水化物的酸性强于碳酸
d.与同族的Ge(锗)作比较:碱性Ge(OH)4<Pb(OH)4,则金属性Ge<Pb,周期表中位置Pb在Ge下面.
e.同族的Ge(锗)与盐酸不反应,Pb与盐酸能反应,则原子半径Ge>Pb
(2)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___.
(3)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g)△H=a kJ⋅mol-1
PbS(s)+2PbO(s)=3Pb(s)+SO2(g)△H=b kJ⋅mol-1
PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g)△H=c kJ⋅mol-1
反应3PbS(s)+6O2(g)=3PbSO4(s)△H=___kJ⋅mol-1(用含a,b,c的代数式表示).
(4)引爆导弹、核武器的工作电源通常Ca/PbSO4热电池,其装置如图1所示,该电池正极的电极反应式为___.
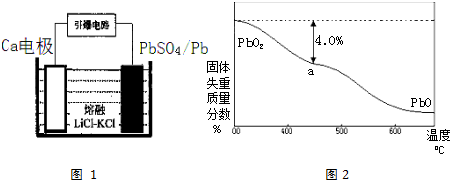
(5)PbO2在加热过程发生分解的失重曲线如图2所示,已知失重曲线上的a点为样品失重4.0%[即:(
×100%]的残留固体.若a点固体组成表示为PbOx或mPbO2•nPbO,列式计算x值___,和m:n值___.
(1)铅与碳是同族元素,则下列说法正确的是___.
a.主要化合价为+2、+4
b.同族的Si与Ge(锗)均为半导体材料,铅也为半导体材料.
c.铅的最高价氧化物对应水化物的酸性强于碳酸
d.与同族的Ge(锗)作比较:碱性Ge(OH)4<Pb(OH)4,则金属性Ge<Pb,周期表中位置Pb在Ge下面.
e.同族的Ge(锗)与盐酸不反应,Pb与盐酸能反应,则原子半径Ge>Pb
(2)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为___.
(3)瓦纽科夫法熔炼铅,其相关反应的热化学方程式如下:
2PbS(s)+3O2(g)=2PbO(s)+2SO2(g)△H=a kJ⋅mol-1
PbS(s)+2PbO(s)=3Pb(s)+SO2(g)△H=b kJ⋅mol-1
PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g)△H=c kJ⋅mol-1
反应3PbS(s)+6O2(g)=3PbSO4(s)△H=___kJ⋅mol-1(用含a,b,c的代数式表示).
(4)引爆导弹、核武器的工作电源通常Ca/PbSO4热电池,其装置如图1所示,该电池正极的电极反应式为___.

(5)PbO2在加热过程发生分解的失重曲线如图2所示,已知失重曲线上的a点为样品失重4.0%[即:(
| 样品起始质量-a点固体质量 |
| 样品起始质量 |
▼优质解答
答案和解析
(1)a.铅与碳是同族元素,最外层电子数为4,主要化合价为+2、+4,故a正确;
b.同族的Si与Ge(锗)均为半导体材料,铅是金属不是半导体材料,故b错误;
c.同主族最高价氧化物对应水化物形成的酸性减弱,铅的最高价氧化物对应水化物的酸性弱于碳酸,故c错误;
d.同主族从上到下金属性增强,形成最高价氢氧化物的碱性增强,与同族的Ge(锗)作比较:碱性Ge(OH)44,则金属性Gee.同族的Ge(锗)与盐酸反应,Pb与盐酸能反应,则原子半径Ge故答案为:ad;
(2)PbO和次氯酸钠反应生成二氧化铅和氯化钠,离子方程式为PbO+ClO-=PbO2+Cl-,故答案为:PbO+ClO-=PbO2+Cl-;
(3)已知:①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g)△H=a kJ•mol-1
②PbS(s)+2PbO(s)=3Pb(s)+SO2(g)△H=b kJ•mol-1
③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g)△H=c kJ•mol-1
将①×2+②×2-③×3可得反应3PbS(s)+6O2(g)=3PbSO4(s)
根据盖斯定律△H=2△H1+2△H2-3△H3=(2a+2b-3c)kJ•mol-1
故答案为:2a+2b-3c;
(4)根据装置图,判断正极为PbSO4发生还原反应,故答案为PbSO4+2e-=SO42-+Pb,故答案为:PbSO4+2e-=SO42-+Pb;
(5)若a点固体组成表示为PbOx,根据PbO2
PbOx+
O2↑,
×32=239×4.0%,x=1.4;
若组成为mPbO2•nPbO,根据原子守恒得,O原子和Pb原子的比值=x=
=1.4,得m:n=2:3,
故答案为:1.4;2:3;
b.同族的Si与Ge(锗)均为半导体材料,铅是金属不是半导体材料,故b错误;
c.同主族最高价氧化物对应水化物形成的酸性减弱,铅的最高价氧化物对应水化物的酸性弱于碳酸,故c错误;
d.同主族从上到下金属性增强,形成最高价氢氧化物的碱性增强,与同族的Ge(锗)作比较:碱性Ge(OH)4
(2)PbO和次氯酸钠反应生成二氧化铅和氯化钠,离子方程式为PbO+ClO-=PbO2+Cl-,故答案为:PbO+ClO-=PbO2+Cl-;
(3)已知:①2PbS(s)+3O2(g)=2PbO(s)+2SO2(g)△H=a kJ•mol-1
②PbS(s)+2PbO(s)=3Pb(s)+SO2(g)△H=b kJ•mol-1
③PbS(s)+PbSO4(s)=2Pb(s)+2SO2(g)△H=c kJ•mol-1
将①×2+②×2-③×3可得反应3PbS(s)+6O2(g)=3PbSO4(s)
根据盖斯定律△H=2△H1+2△H2-3△H3=(2a+2b-3c)kJ•mol-1
故答案为:2a+2b-3c;
(4)根据装置图,判断正极为PbSO4发生还原反应,故答案为PbSO4+2e-=SO42-+Pb,故答案为:PbSO4+2e-=SO42-+Pb;
(5)若a点固体组成表示为PbOx,根据PbO2
| ||
| 2-x |
| 2 |
| 2-x |
| 2 |
若组成为mPbO2•nPbO,根据原子守恒得,O原子和Pb原子的比值=x=
| 2m+n |
| m+n |
故答案为:1.4;2:3;
看了铅及其化合物可用于蓄电池、耐酸...的网友还看了以下:
已知硫酸对应的非金属氧化物是三氧化硫二氧化碳对应的算是亚硫酸那么亚硫酸对情的非金属氧化物是———H 2020-05-02 …
硫酸,盐酸,硝酸名多大浓度为浓酸,能引起铁铝钝化的酸是什么酸 2020-05-16 …
酸和碱的反应时中和反应,这里的酸是指酸性的溶液还是酸的溶液还有这里碱是指碱性的溶液还是碱的溶液.碱 2020-05-16 …
回答下列与常见的酸有关的问题.(1)胃液中有助于消化的酸是.(2)浓硫酸常用作某些气体的干燥剂,主 2020-05-17 …
实验室制取二氧化碳的酸是什么酸是盐酸、硼酸、碳酸还是醋酸 2020-05-24 …
如何比较硅酸钠和碳酸钠碱性强弱?碳酸根对应的酸是碳酸氢根而硅酸根对应的酸是什么? 2020-06-07 …
最强的酸是甚么?别告诉我是王水,魔酸,高氯酸,氢碘酸.要原理! 2020-06-27 …
心里一酸的酸是什么意思?寒酸小气的酸是什么意思?A酸味B疼痛C难受D不大方 2020-07-02 …
除去暖水瓶中的水垢,下列最适宜的酸是()A.浓硫酸B.稀硫酸C.碳酸D.稀盐酸 2020-07-15 …
酸碱质子理论认为,酸给出质子后变成碱,碱接受质子后变成酸,酸=碱+质子,此式中右边的碱是左边的酸的 2020-07-15 …