早教吧作业答案频道 -->化学-->
某中药主要含二硫化亚铁(FeS2),某学习小组欲用图1所示装置进行实验,测定其铁、硫元素的质量分数.(1)装置中,A为高温灼烧装置,B为气体吸收装置,C为检测尾气中是否含有SO2的传
题目详情
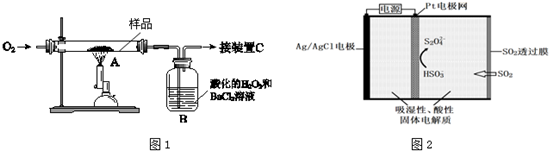
某中药主要含二硫化亚铁(FeS2),某学习小组欲用图1所示装置进行实验,测定其铁、硫元素的质量分数.
(1)装置中,A为高温灼烧装置,B为气体吸收装置,C为检测尾气中是否含有SO2的传感器.取m g该中药样品于装置A中,经充分反应,使硫元素全部转化为SO2和SO3,在B中得到白色沉淀,传感器(装置C)未检测到SO2.
①装置B中的H2O2反应时表现出了___性.
②欲计算硫元素的质量分数,需测量的数据是___.
③传感器的工作原理如图2所示.
传感器中阴极的电极反应式是___.
(2)为测定铁元素的质量分数,继续实验.
a.将A装置中的剩余固体用足量盐酸酸浸,有少量H2产生.充分反应后过滤,得到黄色滤液;
b.向滤液中滴加TiCl3溶液,至恰好完全反应,TiCl3被氧化为TiO2+;
c.用滴定法测定Fe2+的量,消耗v mL n mol/LK2Cr2O7溶液.
①a中滤液含有的金属阳离子是___.
②b中反应的离子方程式是___.
③c中K2Cr2O7被还原为Cr3+,样品中铁元素质量分数的数学表示式是___.
(1)装置中,A为高温灼烧装置,B为气体吸收装置,C为检测尾气中是否含有SO2的传感器.取m g该中药样品于装置A中,经充分反应,使硫元素全部转化为SO2和SO3,在B中得到白色沉淀,传感器(装置C)未检测到SO2.

①装置B中的H2O2反应时表现出了___性.
②欲计算硫元素的质量分数,需测量的数据是___.
③传感器的工作原理如图2所示.
传感器中阴极的电极反应式是___.
(2)为测定铁元素的质量分数,继续实验.
a.将A装置中的剩余固体用足量盐酸酸浸,有少量H2产生.充分反应后过滤,得到黄色滤液;
b.向滤液中滴加TiCl3溶液,至恰好完全反应,TiCl3被氧化为TiO2+;
c.用滴定法测定Fe2+的量,消耗v mL n mol/LK2Cr2O7溶液.
①a中滤液含有的金属阳离子是___.
②b中反应的离子方程式是___.
③c中K2Cr2O7被还原为Cr3+,样品中铁元素质量分数的数学表示式是___.
▼优质解答
答案和解析
(1)①取m g该中药样品于装置A中,经充分反应,FeS2燃烧生成二氧化硫和氧化铁,二氧化硫通入酸化的过氧化氢和氯化钡溶液中,使硫元素全部转化为SO2和SO3,在B中得到白色沉淀,发生氧化还原反应生成硫酸钡沉淀;过氧化氢的主要作用是氧化剂氧化+4价硫为+6价硫酸根离子,装置B中的H2O2反应时表现出了氧化性,
故答案为:氧化;
②欲计算硫元素的质量分数,需要测定B中沉淀质量计算硫元素物质的量,所以测量的数据是B中沉淀的质量,
故答案为:B中沉淀的质量;
③阴极发生还原反应,酸溶液中亚硫酸氢根离子得到电子生成S2O42-,电极反应为2HSO3-+2H++2e-=S2O42-+2H2O,
故答案为:2HSO3-+2H++2e-=S2O42-+2H2O;
(2)①将A装置中的剩余固体用足量盐酸酸浸,有少量H2产生证明含有铁,充分反应后过滤,得到黄色滤液,说明含有氧化铁,所以盐酸溶解后得到溶液中含有阳离子为:Fe3+、Fe2+,
故答案为:Fe3+、Fe2+;
②向滤液中滴加TiCl3溶液,至恰好完全反应,TiCl3被铁离子氧化为TiO2+,反应的离子方程式为:Fe3++Ti3++H2O=Fe2++TiO2++2H+;
故答案为:Fe3++Ti3++H2O=Fe2++TiO2++2H+;
③用滴定法测定Fe2+的量,消耗v mL n mol/LK2Cr2O7溶液,则
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
6 1
n(Fe2+) v×10-3L×n mol/L
n=6vn×10-3mol
样品中铁元素质量分数=
×100%=
vn×100%=
×100%=
%,
故答案为:
%.
故答案为:氧化;
②欲计算硫元素的质量分数,需要测定B中沉淀质量计算硫元素物质的量,所以测量的数据是B中沉淀的质量,
故答案为:B中沉淀的质量;
③阴极发生还原反应,酸溶液中亚硫酸氢根离子得到电子生成S2O42-,电极反应为2HSO3-+2H++2e-=S2O42-+2H2O,
故答案为:2HSO3-+2H++2e-=S2O42-+2H2O;
(2)①将A装置中的剩余固体用足量盐酸酸浸,有少量H2产生证明含有铁,充分反应后过滤,得到黄色滤液,说明含有氧化铁,所以盐酸溶解后得到溶液中含有阳离子为:Fe3+、Fe2+,
故答案为:Fe3+、Fe2+;
②向滤液中滴加TiCl3溶液,至恰好完全反应,TiCl3被铁离子氧化为TiO2+,反应的离子方程式为:Fe3++Ti3++H2O=Fe2++TiO2++2H+;
故答案为:Fe3++Ti3++H2O=Fe2++TiO2++2H+;
③用滴定法测定Fe2+的量,消耗v mL n mol/LK2Cr2O7溶液,则
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
6 1
n(Fe2+) v×10-3L×n mol/L
n=6vn×10-3mol
样品中铁元素质量分数=
| 6vn×10-3mol×56g/mol |
| mg |
| 0.336 |
| m |
| 0.336vn |
| m |
| 33.6nv |
| m |
故答案为:
| 33.6nv |
| m |
看了某中药主要含二硫化亚铁(FeS...的网友还看了以下:
工业上用铝土矿(主要成分为Al203,还有少量的Fe203、Si02等杂质)提取氧化铝,操作过程如 2020-06-09 …
为落实“五水共治”,某工厂拟综合处理含NH4+废水和工业废气(主要含N2,CO2,SO2,NO,C 2020-06-21 …
(2013•平顶山一模)下表为某校食堂某天午餐部分食谱:主食荤菜素菜米饭红烧牛肉炒胡萝卜、炒黄瓜( 2020-06-28 …
下表为某校食堂某天午餐部分食谱:主食荤菜素菜米饭红烧牛肉炒胡萝卜、炒黄瓜(1)食谱中富含蛋白质的是 2020-06-28 …
(2013•浦东新区二模)工业上生产硫酸的原料,一种是黄铁矿,其主要成分为FeS2(S为-1价); 2020-06-29 …
xx钙咀嚼片规格:2.5g/片含钙量:0.5g/片主要成分:碳酸钙(1)每片xx钙咀嚼片规格:2. 2020-07-04 …
某铝合金(硬铝)中含有镁、铜、硅,为了测定该合金中铝的含量,有人设计如下实验:(1)取样品ag,称 2020-07-06 …
人类使用的燃料大多来自化石燃料.(1)煤主要含有碳元素,将煤作为燃料,主要是利用碳元素与氧反应所放 2020-07-29 …
(l)食谱中的米饭主要含(填“淀粉”或“纤维素”).(2)从营养均衡及学生身体发育需要的角度考虑,你 2020-12-02 …
近代形而上学唯物主为什么近代形而上学唯物主义具有形而上学(2者有何区别),还有历史观上的唯心主义(都 2020-12-08 …