早教吧作业答案频道 -->化学-->
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如图所示装置(略去部分加持仪器)模拟生成过程.(C装置中盛装Na2S和Na2SO3混合溶液)烧瓶C中发生反应如下:Na2S+H2O+SO2=Na2SO3+H2S(Ⅰ)
题目详情
工业上常利用含硫废水生产Na2S2O3•5H2O,实验室可用如图所示装置(略去部分加持仪器)模拟生成过程.(C装置中盛装Na2S和Na2SO3混合溶液)
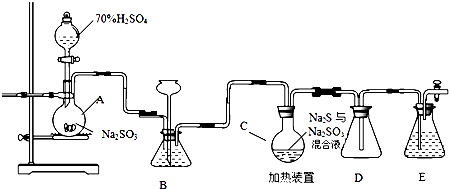
烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (Ⅰ)
2H2S+SO2=3S↓+2H2O (Ⅱ)
S+Na2SO3
Na2S2O (Ⅲ)
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若___,则整个装置气密性良好.
(2)装置D的作用是___,装置E中为___溶液.
(3)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为___.
(4)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___.
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(5)已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是___.
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:___.
已知Na2S2O3•5H2O遇酸易分 S2O32‾+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.

烧瓶C中发生反应如下:
Na2S+H2O+SO2=Na2SO3+H2S (Ⅰ)
2H2S+SO2=3S↓+2H2O (Ⅱ)
S+Na2SO3
| ||
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液注,若___,则整个装置气密性良好.
(2)装置D的作用是___,装置E中为___溶液.
(3)为提高产品纯度,应使烧瓶C中Na2S和Na2SO3恰好完全反应,则烧瓶C中Na2S和Na2SO3物质的量之比为___.
(4)装置B的作用之一是观察SO2的生成速率,其中的液体最好选择___.
a.蒸馏水 b.饱和Na2SO3溶液
c.饱和NaHSO3溶液 d.饱和NaHCO3溶液
(5)已知反应(Ⅲ)相对较慢,则烧瓶C中反应达到终点的现象是___.
(6)反应终止后,烧瓶C中的溶液经蒸发浓缩即可析出Na2S2O3•5H2O,其中可能含有Na2SO3、Na2SO4等杂质.利用所给试剂设计实验,检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论:___.
已知Na2S2O3•5H2O遇酸易分 S2O32‾+2H+=S↓+SO2↑+H2O
供选择的试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、AgNO3溶液.
▼优质解答
答案和解析
(1)仪器组装完成后,关闭两端活塞,向装置B中的长颈漏斗内注入液体至形成一段液柱,若液柱高度保持不变,则气密性良好,故答案为:液柱高度保持不变;(2)D中左侧为短导管,为安全瓶,防止倒吸;装置E起到吸收尾...
看了工业上常利用含硫废水生产Na2...的网友还看了以下:
80摄是度时,饱和硫酸铜溶液310克,加热蒸发掉100克水,再冷却到30摄是度,可析出多少克硫酸铜 2020-05-13 …
用a吨硫铁矿(FeS2)制硫酸,若S的损失率为20%,则硫铁矿的损失率为多少?S的总损失啊!你用和 2020-05-20 …
在体积为2L的恒容容器中发生如下反应2NaSO4(s)+4H2(g)-----Na2S(s)+4H 2020-05-23 …
可逆反应Na2so4(s)十4H2(g)=Na2S(s)十4H2O(g)TV一定时向体系中加入少量 2020-05-23 …
求Na2SO4(s)+4H2(g)↔Na2S(s)+4H2O(g)平衡常数在某温度达到平衡后,测得 2020-05-23 …
细胞受到冰冻时,蛋白质分子相互靠近,当接近到一定程度时,蛋白质分子中相邻近的巯基(-SH)氧化形成 2020-06-22 …
已知S6、S8的结构如图所示.下列说法中错误的是()A.硫单质S原子间都以σ键结合B.S6、S8分 2020-06-30 …
把下面的式子的两边弄成相等的1.FeCl3(aq)+KOH(aq)-->Fe(OH)3(s)+KC 2020-07-09 …
书写下列反应的文字表达式(或用化学式表示反应):(1)硫单质在空气中燃烧硫+氧气点燃二氧化硫(或S 2020-07-13 …
书写下列反应的文字表达式(或用化学式表示反应):(1)硫单质在空气中燃烧硫+氧气点燃二氧化硫(或S 2020-07-13 …