早教吧作业答案频道 -->化学-->
氨基甲酸铵(NH2COONH4)是一种白色固体,可用做肥料、灭火剂、洗涤剂等.制备氨基甲酸铵的化学方程式如下:2NH3(g)+CO2(g)═NH2COONH4(s)△H<0,已知氨基甲酸铵有以下性质:a.常温
题目详情
氨基甲酸铵(NH2COONH4)是一种白色固体,可用做肥料、灭火剂、洗涤剂等.制备氨基甲酸铵的化学方程式如下:2NH3(g)+CO2(g)═NH2COONH4(s)△H<0,
已知氨基甲酸铵有以下性质:
a.常温下在干燥的空气中稳定,遇水生成碳酸铵或碳酸氢铵;
b.59℃则可分解成NH3和CO2气体;
用如图1装置制备干燥的氨气,图Ⅱ装置制备氨基甲酸铵,把制备的干燥的氨气和二氧化碳通入四氯化碳中不断搅拌混合,当生成的氨基甲酸铵晶体悬浮在四氯化碳中较多时停止制备(注:四氯化碳与液体石蜡均为惰性介质).
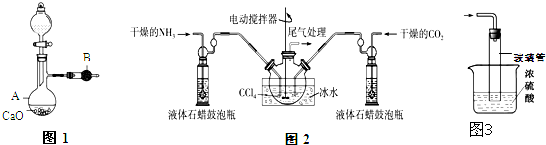
请回答下列问题:
(1)图1中,仪器B的名称___,A中的化学反应方程式是___;
(2)图2装置中使用冰水的原因是___;
(3)图2中液体石蜡鼓泡瓶的作用是___;
(4)从图2反应后的混合物中分离出产品的方法是___;
A.蒸馏 B.过滤 C.分液 D.结晶
(5)图2装置中,尾气处理装置如图3所示,玻璃管的作用___,浓硫酸的作用是___和防止空气中水蒸气进入反应器使氨基甲酸铵水解;
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品7.82g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为10.0g,则样品中氨基甲酸铵的质量分数为___(计算结果精确至0.1%)
已知氨基甲酸铵有以下性质:
a.常温下在干燥的空气中稳定,遇水生成碳酸铵或碳酸氢铵;
b.59℃则可分解成NH3和CO2气体;
用如图1装置制备干燥的氨气,图Ⅱ装置制备氨基甲酸铵,把制备的干燥的氨气和二氧化碳通入四氯化碳中不断搅拌混合,当生成的氨基甲酸铵晶体悬浮在四氯化碳中较多时停止制备(注:四氯化碳与液体石蜡均为惰性介质).

请回答下列问题:
(1)图1中,仪器B的名称___,A中的化学反应方程式是___;
(2)图2装置中使用冰水的原因是___;
(3)图2中液体石蜡鼓泡瓶的作用是___;
(4)从图2反应后的混合物中分离出产品的方法是___;
A.蒸馏 B.过滤 C.分液 D.结晶
(5)图2装置中,尾气处理装置如图3所示,玻璃管的作用___,浓硫酸的作用是___和防止空气中水蒸气进入反应器使氨基甲酸铵水解;
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品7.82g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为10.0g,则样品中氨基甲酸铵的质量分数为___(计算结果精确至0.1%)
▼优质解答
答案和解析
(1)装置1中仪器B的名称是干燥管;把浓氨水滴入到固体氧化钙,在溶解过程中放热使浓氨水分解生成氨气,则反应方程式为CaO+NH3•H2O=Ca(OH)2+NH3↑,
故答案为:干燥管;CaO+NH3•H2O=Ca(OH)2+NH3↑;
(2)反应2NH3(g)+CO2(g)⇌NH2COONH4(s)+Q,是放热反应,降温平衡正向进行,温度升高;发生器用冰水冷却提高反应物质转化率,防止生成物温度过高分解,
故答案为:降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解);
(3)液体石蜡鼓泡瓶的作用是控制反应进行程度,控制气体流速和原料气体的配比,故答案为:通过观察气泡,调节NH3与CO2通入比例;
(4)制备氨基甲酸铵的装置如图3所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,分离产品的实验方法利用过滤得到,故选:B;
(5)双通玻璃管的作用是防止液体倒吸;浓硫酸起到吸收多余的氨气,同时防止空气中水蒸气进入反应器使氨基甲酸铵水解,
故答案为:防止倒吸;吸收多余氨气;
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品7.82g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为10.0g.物质的量为
=0.1mol,设样品中氨基甲酸铵物质的量为x,碳酸氢铵物质的量为y,由碳元素守恒可知,
x+y=0.1
78x+79y=7.82
解得x=0.08mol
y=0.02mol
则样品中氨基甲酸铵的质量分数=
×100%=79.8%,故答案为:79.8%.
故答案为:干燥管;CaO+NH3•H2O=Ca(OH)2+NH3↑;
(2)反应2NH3(g)+CO2(g)⇌NH2COONH4(s)+Q,是放热反应,降温平衡正向进行,温度升高;发生器用冰水冷却提高反应物质转化率,防止生成物温度过高分解,
故答案为:降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解);
(3)液体石蜡鼓泡瓶的作用是控制反应进行程度,控制气体流速和原料气体的配比,故答案为:通过观察气泡,调节NH3与CO2通入比例;
(4)制备氨基甲酸铵的装置如图3所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,分离产品的实验方法利用过滤得到,故选:B;
(5)双通玻璃管的作用是防止液体倒吸;浓硫酸起到吸收多余的氨气,同时防止空气中水蒸气进入反应器使氨基甲酸铵水解,
故答案为:防止倒吸;吸收多余氨气;
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品7.82g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为10.0g.物质的量为
| 10g |
| 100g/mol |
x+y=0.1
78x+79y=7.82
解得x=0.08mol
y=0.02mol
则样品中氨基甲酸铵的质量分数=
| 0.08mol×78g/mol |
| 7.82g |
看了 氨基甲酸铵(NH2COONH...的网友还看了以下:
下列既用了二氧化碳的物理性质,又用了二氧化碳的化学性质的是()A.用于灭火B.参与光合作用C.用于 2020-05-13 …
下列二氧化碳的用途中,既跟它的物理性质有关,又跟它的化学性质有关的是()A.用来灭火B.制化肥C. 2020-05-13 …
(1999•安徽)实验桌上因酒精灯打翻而着火时,最简单、最好的扑灭方法是()A.用水冲灭B.用手扑 2020-06-16 …
在进行实验时,若不小心弄倒了酒精灯而引起着火,应采用的最简单的扑灭方法是()A.用水浇灭B.用手捂 2020-07-28 …
因酒精灯打翻而使酒精在桌上燃烧起来时,最简捷的灭火方法是()A.用泥沙扑灭B.用湿抹布扑灭C.用水扑 2020-10-30 …
下列说法错误的是()A.用水灭火,是为了降低可燃物的着火点B.利用洗洁精的乳化作用可以洗去餐具上的油 2020-11-05 …
实验时不小心碰翻了酒精灯,酒精在桌上燃烧起来,这时最简便的灭火方法是()A.用湿抹布盖灭B.用水去冲 2021-01-14 …
实验桌上的酒精灯被打翻时,最简单的灭火方法是()A.用水扑灭B.用泡沫灭火器灭火C.用湿抹布盖灭D. 2021-01-14 …
实验时不小心打翻酒精灯着火了,最简便合理的灭火方法是A用水浇灭B用嘴吹灭C用湿抹布盖灭D用灭火器朴灭 2021-01-14 …
下列情况所采取的灭火方法,不恰当的是()A.用泡沫灭火器扑灭木材场的大火B.酒精灯不慎失火,用湿抹布 2021-01-14 …