早教吧作业答案频道 -->化学-->
随着不断向化工、石油、电力、海水淡化、建筑、日常生活用品等行业推广,钛金属日益被人们重视,被誉为“现代金属”和“战略金属”,是提高国防装备水平不可或缺的重要战略物资.
题目详情
随着不断向化工、石油、电力、海水淡化、建筑、日常生活用品等行业推广,钛金属日益被人们重视,被誉为“现代金属”和“战略金属”,是提高国防装备水平不可或缺的重要战略物资.工业主要以二氧化钛为原料冶炼金属钛.
(1)Ⅰ.二氧化钛可由以下两种方法制备:
方法1:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:
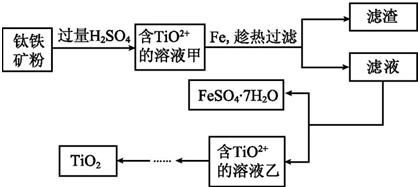
(1)由滤液获得绿矾晶体的操作过程是___.
(2)甲溶液中除含TiO2+之外还含有的金属阳离子有___.
(3)已知10 kg该钛铁矿中铁元素的质量分数为33.6%,能够得到绿矾晶体22.24 kg,试计算最少加入铁粉的质量.
方法2:TiCl4水解生成TiO2•xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛.
(4)①TiCl4水解生成TiO2•xH2O的化学方程式为___;
②检验TiO2•xH2O中Cl-是否被除净的方法是___.
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及的步骤如下:TiO2
TiCl4
Ti
反应②的化学方程式是___,该反应成功需要的其他条件及原因是___.
(1)Ⅰ.二氧化钛可由以下两种方法制备:
方法1:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:

(1)由滤液获得绿矾晶体的操作过程是___.
(2)甲溶液中除含TiO2+之外还含有的金属阳离子有___.
(3)已知10 kg该钛铁矿中铁元素的质量分数为33.6%,能够得到绿矾晶体22.24 kg,试计算最少加入铁粉的质量.
方法2:TiCl4水解生成TiO2•xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛.
(4)①TiCl4水解生成TiO2•xH2O的化学方程式为___;
②检验TiO2•xH2O中Cl-是否被除净的方法是___.
Ⅱ.二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及的步骤如下:TiO2
| ① |
| |
| ② |
| |
| Mg800℃ |
反应②的化学方程式是___,该反应成功需要的其他条件及原因是___.
▼优质解答
答案和解析
钛铁矿和过量稀硫酸混合,FeTiO3和稀硫酸反应生成Fe2+、TiO2+,氧化铁和稀硫酸反应生成Fe3+,所以溶液甲中含有Fe2+、TiO2+、Fe3+,然后向溶液中加入Fe,Fe将Fe3+氧化生成Fe2+,然后过滤得到滤渣和滤液,滤液中含有硫酸亚铁,将滤液蒸发浓缩、冷却结晶得到绿矾和含有TiO2+溶液乙,通过一系列反应得到TiO2;
(1)从溶液中获得绿矾晶体,应该采用蒸发浓缩、冷却结晶、过滤的方法,所以由滤液获得绿矾晶体的操作过程是蒸发、冷却、结晶、过滤,故答案为:蒸发、冷却、结晶、过滤;
(2)FeTiO3和稀硫酸反应生成Fe2+、TiO2+,氧化铁和稀硫酸反应生成Fe3+,所以甲中阳离子为Fe2+、TiO2+、Fe3+,
故答案为:Fe2+、Fe3+;
(3)10 kg该钛铁矿中铁元素的质量分数为33.6%,该钛铁矿中Fe元素质量=10kg×33.6%=3.36kg,
绿矾晶体中Fe元素质量=
×56g/mol=4.48×103g=4.48kg,根据Fe元素守恒得需要加入Fe的质量=4.48kg-3.36kg=1.12kg,
答:最少加入Fe的质量为1.12kg;
(4)①TiCl4水解生成TiO2•xH2O,同时生成HCl,反应方程式为TiCl4+(x+2)H2O(过量)⇌TiO2•xH2O↓+4HCl,
故答案为:TiCl4+(x+2)H2O(过量)⇌TiO2•xH2O↓+4HCl;
②氯离子用硝酸酸化的硝酸银溶液检验,如果有白色沉淀说明含有氯离子,所以检验TiO2•xH2O中Cl-是否被除净的方法是取最后一次洗涤液少量,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净,
故答案为:取最后一次洗涤液少量,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净;
Ⅱ.在800℃条件下,四氯化钛和镁反应生成氯化镁和钛,Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气,防止Mg和空气中物质反应.
(5)反应②的化学方程式是TiCl4+2Mg
2MgCl2+Ti,稀有气体保护,防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用,所以该反应成功需要的其他条件及原因稀有气体保护,防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用,
故答案为:TiCl4+2Mg
2MgCl2+Ti;稀有气体保护,防止高温下Mg(Ti)与空气中的O2(或CO2、N2)作用.
(1)从溶液中获得绿矾晶体,应该采用蒸发浓缩、冷却结晶、过滤的方法,所以由滤液获得绿矾晶体的操作过程是蒸发、冷却、结晶、过滤,故答案为:蒸发、冷却、结晶、过滤;
(2)FeTiO3和稀硫酸反应生成Fe2+、TiO2+,氧化铁和稀硫酸反应生成Fe3+,所以甲中阳离子为Fe2+、TiO2+、Fe3+,
故答案为:Fe2+、Fe3+;
(3)10 kg该钛铁矿中铁元素的质量分数为33.6%,该钛铁矿中Fe元素质量=10kg×33.6%=3.36kg,
绿矾晶体中Fe元素质量=
| 22.24×103g |
| 278g/mol |
答:最少加入Fe的质量为1.12kg;
(4)①TiCl4水解生成TiO2•xH2O,同时生成HCl,反应方程式为TiCl4+(x+2)H2O(过量)⇌TiO2•xH2O↓+4HCl,
故答案为:TiCl4+(x+2)H2O(过量)⇌TiO2•xH2O↓+4HCl;
②氯离子用硝酸酸化的硝酸银溶液检验,如果有白色沉淀说明含有氯离子,所以检验TiO2•xH2O中Cl-是否被除净的方法是取最后一次洗涤液少量,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净,
故答案为:取最后一次洗涤液少量,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已除净;
Ⅱ.在800℃条件下,四氯化钛和镁反应生成氯化镁和钛,Mg是活泼金属,能与空气中多种物质反应,因此可得出Ar气作用为保护气,防止Mg和空气中物质反应.
(5)反应②的化学方程式是TiCl4+2Mg
| ||
故答案为:TiCl4+2Mg
| ||
看了随着不断向化工、石油、电力、海...的网友还看了以下:
醋酸、柠檬酸等是食品加工中常用的酸,它们在水中都能电离生成A.OH-B.H+C.Cl-D.SO42 2020-06-28 …
跪求一篇关于旅游必备品的作文!急!最好带翻译旅游时必备的物品,比如地图、相机、mp3等至少最重要的 2020-07-26 …
现代生活离不开电池.电子表、移动电话、汽车等许多电子产品,都需要配备各式各样的电池.锂电池是目前相同 2020-11-01 …
食醋、食盐、碱面、蔗糖、花生油、大米、矿泉水都是厨房常备物品.请选择物质填空:(1)市场上食盐的品种 2020-11-22 …
科学、实用、安全、经济、美观、新颖等是产品设计评价的基本原则,一般来说,对某种产品设计进行评价时应综 2020-11-28 …
食醋、食盐、纯碱、蔗糖、花生油、大米、矿泉水都是厨房常备物品。请选择物质填空:(1)市场上食盐的品种 2020-12-02 …
英语翻译萃取一车间萃取二车间预处理车间沉淀灼烧车间生产辅料仓备品仓饭堂宿舍成品仓中控分析室清洁用品室 2020-12-10 …
食醋(CH3COOH)、食盐、纯碱、蔗糖、花生油、大米、矿泉水都是厨房常备物品.请选择物质填空:(1 2021-01-12 …
食醋(CH3COOH)、食盐、纯碱、蔗糖、花生油、大米、矿泉水都是厨房常备物品.请选择物质填空:(1 2021-01-12 …
(2009•朝阳区一模)食醋、食盐、碱面、蔗糖、花生油、大米、矿泉水都是厨房常备物品.请选择物质填空 2021-01-12 …