早教吧作业答案频道 -->化学-->
如图所示是用铅蓄电池为电源,模拟氯碱工业中电解饱和食盐水的装置图(C、D均为石墨电极).已知铅蓄电池在放电时发生下列电极反应.负极:Pb+SO42--2e-═PbSO4正极:PbO2+4H++SO42-+2e-=PbSO4+2H
题目详情
如图所示是用铅蓄电池为电源,模拟氯碱工业中电解饱和食盐水的装置图(C、D均为石墨电极).已知铅蓄电池在放电时发生下列电极反应.
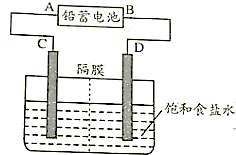
负极:Pb+SO42--2e-═PbSO4
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
(1)若在电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色,说明该铅蓄电池的A极为___极
(2)用铅蓄电池电解2L饱和食盐水(食盐水足量,密度为1.15g/cm3)时:
①若收集到11.2L(标准状况下)氯气,则至少转移电子___mol.
②若该电池消耗0.02molH2SO4,则可收集到H2的体积为___(标准状况下)L.电解后除去隔膜,所得溶液在常温下的pH为___(假定氯气全部排出,电解过程中溶液体积的变化忽略不计).

负极:Pb+SO42--2e-═PbSO4
正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O
(1)若在电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色,说明该铅蓄电池的A极为___极
(2)用铅蓄电池电解2L饱和食盐水(食盐水足量,密度为1.15g/cm3)时:
①若收集到11.2L(标准状况下)氯气,则至少转移电子___mol.
②若该电池消耗0.02molH2SO4,则可收集到H2的体积为___(标准状况下)L.电解后除去隔膜,所得溶液在常温下的pH为___(假定氯气全部排出,电解过程中溶液体积的变化忽略不计).
▼优质解答
答案和解析
(1)电解池中C极一侧滴2滴酚酞试液、电解一段时间后,未呈红色说明C电极为阳极,D为阴极,电源A为正极,
故答案为:正极;
(2)①电解饱和食盐水生成氯气的电极反应为:2Cl--2e-=Cl2↑,收集到11.2L(标准状况下)氯气物质的量为:
=0.5mol,转移电子物质的量为:0.5mol×2=1mol,
故答案为:1;
②蓄电池消耗H2SO4 0.02mol,依据电极反应PbO2+4H++SO42-+2e-=PbSO4+2H2O,消耗0.02mol硫酸电子转移0.02mol,电解食盐水阴极电极反应为2H++2e-=H2↑,则转移0.02mol电子生成氢气的物质的量为0.01mol,标准状况体积为:22.4L/mol×0.01mol=0.224;
根据反应2NaCl+2H2O
2NaOH+Cl2↑+H2↑可知生成0.01mol氢气时会同时生成0.02molNaOH,氢氧根离子的浓度为:
=0.01mol/L,则所得溶液的pH=12,
故答案为:0.224L;12.
故答案为:正极;
(2)①电解饱和食盐水生成氯气的电极反应为:2Cl--2e-=Cl2↑,收集到11.2L(标准状况下)氯气物质的量为:
| 11.2L |
| 22.4L/mol |
故答案为:1;
②蓄电池消耗H2SO4 0.02mol,依据电极反应PbO2+4H++SO42-+2e-=PbSO4+2H2O,消耗0.02mol硫酸电子转移0.02mol,电解食盐水阴极电极反应为2H++2e-=H2↑,则转移0.02mol电子生成氢气的物质的量为0.01mol,标准状况体积为:22.4L/mol×0.01mol=0.224;
根据反应2NaCl+2H2O
| ||
| 0.02mol |
| 2L |
故答案为:0.224L;12.
看了 如图所示是用铅蓄电池为电源,...的网友还看了以下:
牧童吕岩草铺横野六七里,笛弄晚风三四声。归来饱饭黄昏后,不脱蓑衣卧月明。15.《牧童》一诗,向我们 2020-05-13 …
微雨登城二首,为什么虚实结合?《微雨登城二首》雨映寒空半有无,重楼闲上倚城隅.浅深山色高低树,一片 2020-06-10 …
谁首诗怎么解?半窗幽梦轻似雾,枕畔风摇绿户.晓风疏雨动槛竹.浸染疏棂,无声水墨图.我叫孙雨浓... 2020-07-03 …
ClO2是一种广谱、高效的杀菌消毒剂,熔点为-59℃,沸点为11.0℃,不稳定,易溶于水.某研究小组 2020-11-22 …
阅读下面两首诗歌,完成小题。(4分)牧童吕岩草铺横野六七里,笛弄晚风三四声。归来饱饭黄昏后,不脱蓑衣 2020-12-24 …
阅读下面的诗词,回答下面的问题。登城刘敞雨映寒空半有无,重楼闲上倚城隅。浅深山色高低树,一片江南水墨 2021-01-01 …
阅读下面的诗歌,完成下题。登城刘敞雨映寒空半有无,重楼闲上倚城隅。浅深山色高低树,一片江南水墨图。望 2021-01-01 …
麻烦老师解答:阅读下面两首宋诗,完阅读下面两首宋诗,完成后面的题目.登城[宋]刘敞雨映寒空半有无,重 2021-01-01 …
阅读下面两首宋诗,完成后面的题目。登城[宋]刘敞雨映寒空半有无,重楼闲上倚城隅。浅深山色高低树,一片 2021-01-01 …
阅读下面两首宋诗,完成后面的题目。登城刘敞雨映寒空半有无,重楼闲上倚城隅。浅深山色高低树,一片江南水 2021-01-06 …