早教吧作业答案频道 -->化学-->
工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-.为除去杂质离子,部分操作流程如下:请回答问题:(1)用稀硫酸浸泡某矿石后的溶液中,
题目详情
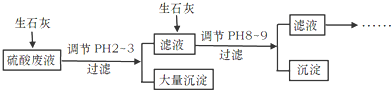
工厂中用稀硫酸浸泡某矿石后的溶液中,除了含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-.为除去杂质离子,部分操作流程如下:
请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9g•L-1,则该溶液中的pH约为___.
(2)NH4+在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在.现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH4+)恰好是NH4Cl溶液中c(NH4+)的2倍,则c[(NH4)2SO4]___c(NH4Cl)(填:<、=或>).
(3)随着向废液中投入生石灰(忽略溶液温度的变化),溶液中
___(填“增大”、“减小”或“不变”).
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],提纯CaSO4•2H2O的主要操作步骤:向沉淀中加入过量___,充分反应后,过滤、洗涤、___.
(5)25℃,H3AsO4电离常数为K1=5.6×10-3,K2=1.7×10-7,K3=4.0×10-12.当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2.
①pH调节到8左右Ca3(AsO4)2才开始沉淀的原因是___.
②Na3AsO4第一步水解的平衡常数数值为:___.
③已知:AsO43-+2I-+2H+=AsO33-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+.上述两个反应中还原性最强的微粒是___.

请回答问题:
(1)用稀硫酸浸泡某矿石后的溶液中,硫酸的浓度为4.9g•L-1,则该溶液中的pH约为___.
(2)NH4+在用稀硫酸浸泡某矿石后的溶液中以(NH4)2SO4和NH4Cl形式存在.现有一份(NH4)2SO4溶液,一份NH4Cl溶液,(NH4)2SO4溶液中c(NH4+)恰好是NH4Cl溶液中c(NH4+)的2倍,则c[(NH4)2SO4]___c(NH4Cl)(填:<、=或>).
(3)随着向废液中投入生石灰(忽略溶液温度的变化),溶液中
| [NH3•H2O] |
| [OH-] |
(4)投入生石灰调节pH到2~3时,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],提纯CaSO4•2H2O的主要操作步骤:向沉淀中加入过量___,充分反应后,过滤、洗涤、___.
(5)25℃,H3AsO4电离常数为K1=5.6×10-3,K2=1.7×10-7,K3=4.0×10-12.当溶液中pH调节到8~9时,沉淀主要成分为Ca3(AsO4)2.
①pH调节到8左右Ca3(AsO4)2才开始沉淀的原因是___.
②Na3AsO4第一步水解的平衡常数数值为:___.
③已知:AsO43-+2I-+2H+=AsO33-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+.上述两个反应中还原性最强的微粒是___.
▼优质解答
答案和解析
硫酸废液中含有大量硫酸外,还含有少量NH4+、Fe3+、AsO43-、Cl-,加入生石灰,调节pH2~3,大量沉淀主要成分为CaSO4•2H2O[含有少量Fe(OH)3],滤液加入生石灰调节pH8~9,生成Ca3(AsO4)2沉淀,滤液主要含有(NH4)2SO4和NH4Cl,
(1)硫酸的浓度为4.9g•L-1,c(H2SO4)=
=0.05mol/L,c(H+)=0.1mol/L,pH=-lg0.1=1,故答案为:1;
(2)如c[(NH4)2SO4]=c(NH4Cl),则(NH4)2SO4溶液中c(NH4+)较大,因c(NH4+)越大,NH4+水解程度越小,则(NH4)2SO4溶液中c(NH4+)大于是NH4Cl溶液中c(NH4+)的2倍,如等于2倍,则c(NH4Cl)应较大,
故答案为:<;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小,则溶液中
减小,故答案为:减小;
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,且防止CaSO4•2H2O的溶解,过滤后洗涤、干燥,
故答案为:稀硫酸;晾干或干燥;
(5)①H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀,
故答案为:H3AsO4是弱酸,当溶液中pH调节到8左右,c(AsO43-)增大,Ca3(AsO4)2开始沉淀;
②Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O⇌HAsO42-+OH-,该步水解的平衡常数Kh=
=
=
=
=2.5×10-3,
故答案为:2.5×10-3;
③已知:AsO43-+2I-+2H+=AsO33-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+.还原剂还原性大于还原产物的还原性,则还原性SO2>I->AsO33-,两个反应中还原性最强的微粒是SO2,
故答案为:SO2.
(1)硫酸的浓度为4.9g•L-1,c(H2SO4)=
| ||
| 1L |
(2)如c[(NH4)2SO4]=c(NH4Cl),则(NH4)2SO4溶液中c(NH4+)较大,因c(NH4+)越大,NH4+水解程度越小,则(NH4)2SO4溶液中c(NH4+)大于是NH4Cl溶液中c(NH4+)的2倍,如等于2倍,则c(NH4Cl)应较大,
故答案为:<;
(3)随着向废液中投入生石灰,c(OH-)增大,c(NH3•H2O)减小,则溶液中
| [NH3•H2O] |
| [OH-] |
(4)提纯CaSO4•2H2O,可加入稀硫酸溶解Fe(OH)3,且防止CaSO4•2H2O的溶解,过滤后洗涤、干燥,
故答案为:稀硫酸;晾干或干燥;
(5)①H3AsO4是弱酸电离出来的AsO43-较少,所以酸性条件下不易形成Ca3(AsO4)2沉淀,当溶液中pH调节到8左右时AsO43-浓度增大,Ca3(AsO4)2开始沉淀,
故答案为:H3AsO4是弱酸,当溶液中pH调节到8左右,c(AsO43-)增大,Ca3(AsO4)2开始沉淀;
②Na3AsO4的第一步水解的离子方程式为:AsO43-+H2O⇌HAsO42-+OH-,该步水解的平衡常数Kh=
| c(HAsO42-)•c(OH-) |
| c(AsO43-) |
| c(HAsO42-)•c(OH-)•c(H+) |
| c(AsO43-)•c(H+) |
| Kw |
| K3 |
| 10-14 |
| 4.0×10-12 |
故答案为:2.5×10-3;
③已知:AsO43-+2I-+2H+=AsO33-+I2+H2O,SO2+I2+2H2O=SO42-+2I-+4H+.还原剂还原性大于还原产物的还原性,则还原性SO2>I->AsO33-,两个反应中还原性最强的微粒是SO2,
故答案为:SO2.
看了工厂中用稀硫酸浸泡某矿石后的溶...的网友还看了以下:
请问有含量85%的铅矿石吗?铅含量85% 2020-04-25 …
(共16分)下图为我国华北地区某乡驻地及周边部分辖区示意图,经勘探,发现图示区域有含量丰富的大煤田 2020-05-01 …
某合金的主要成分有锌、铜、碳等物质.为测定合金的某些含量做如下实验:向50.3g合金粉末中逐次滴加 2020-05-24 …
古文中:然然然然是一句话有一定的意思的我一个女的朋友问我的含义应该是有点意思的或者好玩的大家尽量猜 2020-07-03 …
粉煤灰是燃煤电厂排出的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为42.6%,还有含量 2020-07-12 …
英语翻译如果达不到买方质量要求,按照质量给予买方折价赔偿.(意思是客户给我们了质量要求,比如要求某 2020-07-15 …
碱面(主要成分是)中常含有杂质,某厂生产的碱面包装袋上标有“含量>=96%”字样。为了判断该碱面中的 2020-11-07 …
碱面(主要成分是)中常含有杂质,某厂生产的碱面包装袋上标有“含量>=96%”字样。为了判断该碱面中的 2020-11-07 …
葡萄中有含量丰富的白藜芦醇(化学式为C14H12O3),它能抗癌细胞的增生.试计算:(1)一个白藜芦 2020-11-22 …
粉煤灰是燃煤电厂的工业废渣,其中含莫来石(Al6Si2O13)的质量分数为38%,还有含量较多的Si 2020-11-30 …