若用AG表示溶液的酸度,表达式为:AG=lgc(H+)c(OH-).室温下,用0.1mol•L-1的NaOH溶液滴定10mL0.1mol•L-1HA溶液,滴定曲线如图所示.下列说法错误的是()A.室温下,该HA的电离平衡常数约为
若用AG表示溶液的酸度,表达式为:AG=lg
.室温下,用0.1mol•L-1的NaOH溶液滴定10mL 0.1mol•L-1HA溶液,滴定曲线如图所示.下列说法错误的是( )c(H+) c(OH-) 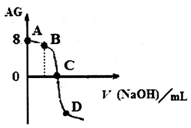
A. 室温下,该HA的电离平衡常数约为10-5
B. C点时加入NaOH溶液的体积为10mL
C. 滴定过程中从A到D点溶液中水的电离程度先增大后减小
D. 若B点加入的NaOH溶液体积为5mL,所得溶液中c(A-)+2c(OH-)═c(HA)+2 c(H+)
| c(H+) |
| c(OH-) |
| C(H+) |
| C(OH-) |
| C(A-)C(H+) |
| C(HA) |
B.C点的AG=lg
| c(H+) |
| c(OH-) |
| C(H+) |
| C(OH-) |
C.从A到D过程中,溶液中的溶质由酸、酸和盐、盐变为盐和碱,酸或碱抑制水电离,含有弱离子的盐促进水电离,故滴定过程中从A到D点溶液中水的电离程度先增大后减小,故C正确;
D.B点溶液中溶质为等浓度的HA和NaA,溶液中电荷守恒为c(OH-)+c(A-)=c(Na+)+c(H+),物料守恒为2c(Na+)=c(A-)+c(HA),所以B点溶液中:c(A-)+2c(OH)-=c(HA)+2c(H+),故D正确,
故选B.
利用水滴下落可以测量重力加速度g,调节水龙头,让水一滴一滴地流出.在水龙头的正下方放一个盘子,调整 2020-05-17 …
下列电池中不能充电的:A.镍镉电池B.银锌电池C.普通干电池D.铅蓄电池下列电池中不能充电的:A. 2020-05-22 …
问一道高一物理题屋檐定时滴出水滴,当第5滴正欲滴下时,第1滴已刚好到达地面,而第3滴与第2滴正分别 2020-06-20 …
1只电烙铁的额定电压是220v,在额定电压下工作时的电阻是1210,它的额定功率有多大?在额定电压 2020-06-29 …
屋檐定时滴出水滴,当第五滴正欲滴下时,第一滴已刚好到达地面,而第三滴与第二滴正分别位于高1m的窗户 2020-07-02 …
(2013•辽宁一模)如图所示的两个平行板电容器水平放置,A板用导线与M板相连,B板和N板都接地.让 2020-10-31 …
某同学站在一平房边观察从屋檐边缘滴下的水滴,发现屋檐的滴水是等时的,且第5滴正欲滴下时,第1滴刚好到 2020-12-10 …
雨滴自房檐由静止滴下,每隔0.2秒滴下一滴,第一滴落地时第六滴恰欲滴下,此时测得第1,2,3,4滴之 2020-12-10 …
如图所示,将滴有酚酞试液的滤纸放入试管中,试管口塞上一团脱脂棉.(1)用胶头滴管吸取浓氨水,滴在脱脂 2020-12-31 …
如图所示,将滴有酚酞试液的滤纸放入试管中,试管口塞上小团脱脂棉.(1)用胶头滴管吸取浓氨水,滴在脱脂 2020-12-31 …