早教吧作业答案频道 -->化学-->
水是生命的源泉,工业的血液、城市的命脉,要保护好河流,河水是重要的饮用水源,污染物通过用水直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请问答下列问题:(1)25℃
题目详情
水是生命的源泉,工业的血液、城市的命脉,要保护好河流,河水是重要的饮用水源,污染物通过用水直接毒害人体,也可通过食物链和灌溉农田间接危及健康.请问答下列问题:
(1)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为___,由水电离出c(OH-)=___mol•L-1.
(2)纯水在100℃时,pH=6,该温度下1mol.L-1的NaOH溶液中,由水电离出的c(OH-)=___mol•l-1
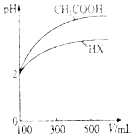
(3)体积均为100mL、pH均为2的CH3COOH溶液与一元酸HX溶液,加水稀释过程中pH与体积的关系如图所示,则HX的电离平衡常数___(填“大于”“小于”或“等于”)CH3COOH的电离平衡常数.
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理置.己知:
①25℃时,有等浓度的NaCN容液、Ma2CO3溶液和CH3COONa溶液,三种溶液的pH由大到小的顺序为___.
②向NaCN溶液中通入少量的CO2,发生反应化学方程式为___.
(5)25℃时,在CH3COOH与CH3COONa的混合洛液中,若测得pH=6,则溶液中CH3COO-)•c(Na+)=___(填精确值)mol•L-1.

(1)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为___,由水电离出c(OH-)=___mol•L-1.
(2)纯水在100℃时,pH=6,该温度下1mol.L-1的NaOH溶液中,由水电离出的c(OH-)=___mol•l-1
(3)体积均为100mL、pH均为2的CH3COOH溶液与一元酸HX溶液,加水稀释过程中pH与体积的关系如图所示,则HX的电离平衡常数___(填“大于”“小于”或“等于”)CH3COOH的电离平衡常数.
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理置.己知:
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3x10-7,K2=5.6×10-11 |
②向NaCN溶液中通入少量的CO2,发生反应化学方程式为___.
(5)25℃时,在CH3COOH与CH3COONa的混合洛液中,若测得pH=6,则溶液中CH3COO-)•c(Na+)=___(填精确值)mol•L-1.
▼优质解答
答案和解析
(1)碳酸钠溶液中因碳酸根离子水解导致溶液显碱性,碳酸根水解的离子方程式为CO32-+H2O⇌HCO3-+OH-、HCO3-+H2O⇌H2CO3+OH-,其pH=11,则c(OH-)=0.001mol/L,全部由水电离产生,故答案为:CO32-+H2O⇌HCO3-+OH-、HCO3-+H2O⇌H2CO3+OH-,0.001;
(2)纯水在100℃时,pH=6,Kw=10-12,该温度下1mol.L-1的NaOH溶液中,由水电离出的c(OH-)=c(H+)=10-12mol/L,
故答案为:10-12;
(3)据图分析,加水稀释的过程中,HX的pH变化比较慢,说明HX的酸性比醋酸弱,HX的电离平衡常数比醋酸小,
故答案为:小于;
(4)①根据图表数据分析,电离常数:醋酸>HCN>碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,故溶液的pH为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,
故答案为:Na2CO3溶液>NaCN溶液>CH3COONa溶液;
②根据电离平衡常数大小可知酸性:H2CO3>HCN>HCO3-,向NaCN溶液中通入少量CO2,反应生成HCN和碳酸氢钠,不能生成二氧化碳,反应的化学方程式为:NaCN+H2O+CO2=HCN+NaHCO3,
故答案为:NaCN+H2O+CO2=HCN+NaHCO3;
(5)25℃时,CH3COOH和CH3COONa的混合溶液,若测得混合液的PH=6,即C(H+)=10-6mol/L,由于水的离子积为10-14,故C(OH-)=10-8mol/L.
根据电荷守恒可知:C(CH3COO-)+C(OH-)=C(Na+)+C(H+),故C(CH3COO-)-C(Na+)=C(H+)-C(OH-)=10-6mol/L-10-8mol/L=9.9×10-7mol/L,
故答案为:9.9×10-7.
(2)纯水在100℃时,pH=6,Kw=10-12,该温度下1mol.L-1的NaOH溶液中,由水电离出的c(OH-)=c(H+)=10-12mol/L,
故答案为:10-12;
(3)据图分析,加水稀释的过程中,HX的pH变化比较慢,说明HX的酸性比醋酸弱,HX的电离平衡常数比醋酸小,
故答案为:小于;
(4)①根据图表数据分析,电离常数:醋酸>HCN>碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,故溶液的pH为:Na2CO3溶液>NaCN溶液>CH3COONa溶液,
故答案为:Na2CO3溶液>NaCN溶液>CH3COONa溶液;
②根据电离平衡常数大小可知酸性:H2CO3>HCN>HCO3-,向NaCN溶液中通入少量CO2,反应生成HCN和碳酸氢钠,不能生成二氧化碳,反应的化学方程式为:NaCN+H2O+CO2=HCN+NaHCO3,
故答案为:NaCN+H2O+CO2=HCN+NaHCO3;
(5)25℃时,CH3COOH和CH3COONa的混合溶液,若测得混合液的PH=6,即C(H+)=10-6mol/L,由于水的离子积为10-14,故C(OH-)=10-8mol/L.
根据电荷守恒可知:C(CH3COO-)+C(OH-)=C(Na+)+C(H+),故C(CH3COO-)-C(Na+)=C(H+)-C(OH-)=10-6mol/L-10-8mol/L=9.9×10-7mol/L,
故答案为:9.9×10-7.
看了水是生命的源泉,工业的血液、城...的网友还看了以下:
下列关于利用细菌净化污水的原理说法错误的是()A.污水中的有机物可以作为细菌的食物B.污水中的无机 2020-06-14 …
下列说法中不正确的是()A.硬水软化后才可做锅炉用水B.煮沸水可以降低水的硬度C.开水瓶中水垢是水 2020-07-10 …
下列物质中按混合物、氧化物、单质的顺序排列的是()A.冰水混合物、水银、食醋B.清新的空气、氖气、 2020-07-22 …
植物细胞可以吸水和失水,下列情况可以使植物细胞吸水的是()A.盐水腌萝卜B.晾晒青菜C.糖拌番茄D 2020-07-24 …
某有机物的结构简式如图所示:下列有关该有机物的叙述正确的是()A.该有机物的分子式为C11H14O 2020-07-29 …
下列关于水的说法不正确的是A水能与酒精互溶,所以水也是有机化合物B水可以溶解许多物质C水既可作为反 2020-07-29 …
下列各组物质只用水便可鉴别的是()A浓HNO3,食盐水,浓盐酸,浓硫酸BCUSO4,CUSO4.5下 2020-11-03 …
按要求回答下列各题.(1)明矾可用于净水,是因为明矾溶于水生成的胶状物可以悬浮于水中的杂质,使杂质从 2020-11-03 …
回答下列问题:(1)图1是家用净水器桶及其滤芯实物图,滤芯中的白色物质为软化剂,其主要作用是降低水中 2020-11-05 …
下列有关植物体内水的吸收与运输之叙述,何者正确A.泌溢作用(溢水作用)可直接帮助植物体运输水分B.高 2020-12-14 …