早教吧作业答案频道 -->化学-->
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸
题目详情
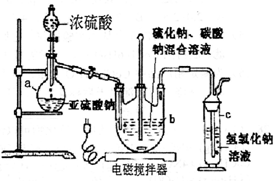
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”.它易溶于水,难溶于乙醇,加热易分解.工业上常用亚硫酸钠法、硫化碱法等制备.某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图:实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节螺旋夹,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电磁搅拌器搅动.
②至析出的硫不再消失,控制溶液的pH接近7时,停止通入
SO2气体.
③抽滤所得的滤液,转移至蒸发皿中,水浴加热浓缩,直到溶液表面出现晶膜.
④冷却结晶、抽滤、洗涤.
⑤将晶体放入烘箱中,在40~45℃左右干燥50~60min,称量.
请回答以下问题:
(l)仪器a的名称是___;
(2)步骤②中若控制pH值小于7,则产率会下降,请用离子方程式解释原因:___.
(3)步骤③中不能将溶液蒸发至干的原因是___;晶膜通常在溶液表面出现的原因是___.
(4)步骤④中洗涤硫代硫酸钠晶体所用试剂的结构式是___.
(5)为检验制得的产品的纯度,该实验小组称取5,0克的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.0lmol•L-1KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+═3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-═2I-+S4O62-,当蓝色褪去H半分钟不变色时到达滴定终点.实验数据如下表:
则该产品的纯度是___,间接碘量法滴定过程中可能造成实验结果偏低的是___.
A.滴定管末用Na2S2O3溶液润洗 B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗 D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡.
①开启分液漏斗,使硫酸慢慢滴下,适当调节螺旋夹,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电磁搅拌器搅动.
②至析出的硫不再消失,控制溶液的pH接近7时,停止通入
SO2气体.
③抽滤所得的滤液,转移至蒸发皿中,水浴加热浓缩,直到溶液表面出现晶膜.
④冷却结晶、抽滤、洗涤.
⑤将晶体放入烘箱中,在40~45℃左右干燥50~60min,称量.
请回答以下问题:
(l)仪器a的名称是___;
(2)步骤②中若控制pH值小于7,则产率会下降,请用离子方程式解释原因:___.
(3)步骤③中不能将溶液蒸发至干的原因是___;晶膜通常在溶液表面出现的原因是___.
(4)步骤④中洗涤硫代硫酸钠晶体所用试剂的结构式是___.
(5)为检验制得的产品的纯度,该实验小组称取5,0克的产品配制成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:在锥形瓶中加入25mL 0.0lmol•L-1KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+═3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-═2I-+S4O62-,当蓝色褪去H半分钟不变色时到达滴定终点.实验数据如下表:
| 实验序号 | 1 | 2 | 3 |
| N2aS2O3溶液体积(mL) | 19.8 | 20.02 | 21.18 |
A.滴定管末用Na2S2O3溶液润洗 B.滴定终点时仰视读数
C.锥形瓶用蒸馏水润洗 D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡.

▼优质解答
答案和解析
(1)由装置图可知a装置为蒸馏烧瓶;故答案为:蒸馏烧瓶;
(2)Na2S2O3在酸性条件下会生成S和二氧化硫,所以产率会下降,其反应的离子方程式为:S2O32-+2H+=S↓+H2O+SO2↑;
故答案为:S2O32-+2H+=S↓+H2O+SO2↑;
(3)已知硫代硫酸钠晶体加热易分解,故蒸干会使硫代硫酸钠脱水并分解,所以从硫代硫酸钠溶液中分离溶质时不能将溶液蒸发至干;加热浓缩硫代硫酸钠溶液,当温度较低时会析出晶体,在冷却时,溶液表面温度较低,先析出晶体;
故答案为:蒸干会使硫代硫酸钠脱水并分解;因为溶液表面温度较低;
(4)硫代硫酸钠易溶于水,难溶于乙醇,在洗涤硫代硫酸钠晶体时,为了减少晶体的溶解,用乙醇来洗涤,乙醇的结构式为: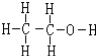 ;
;
故答案为: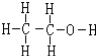 ;
;
(5)在锥形瓶中加入25mL 0.0lmol•L-1KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+═3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-═2I-+S4O62-,
则可得关系式:IO3-~6S2O32-,
1mol 6mol
0.025L×0.0lmol•L-1 n(S2O32-)
则n(S2O32-)=0.0015mol,
第三次实验的数据误差较大,舍去,
所以250mL硫代硫酸钠溶液中硫代硫酸钠的物质的量为0.0015mol×
=0.01875mol,
则硫代硫酸钠的质量为0.01875mol×248g/mol=4.65g,
则该产品的纯度是
×100%=93%;
A.滴定管末用Na2S2O3溶液润洗,则Na2S2O3溶液会被稀释,所以测出硫代硫酸钠的质量偏小,故纯度偏小,故A选;
B.滴定终点时仰视读数,使Na2S2O3溶液体积偏大,计算出的硫代硫酸钠的质量偏小,故纯度偏小,故B选;
C.锥形瓶用蒸馏水润洗,对实验结果没影响,纯度不变,故C不选;
D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡,使读出的Na2S2O3的体积变小,计算出原溶液中的硫代硫酸钠的质量偏大,则纯度偏大,故D不选.
故答案为:93%;AB.
(2)Na2S2O3在酸性条件下会生成S和二氧化硫,所以产率会下降,其反应的离子方程式为:S2O32-+2H+=S↓+H2O+SO2↑;
故答案为:S2O32-+2H+=S↓+H2O+SO2↑;
(3)已知硫代硫酸钠晶体加热易分解,故蒸干会使硫代硫酸钠脱水并分解,所以从硫代硫酸钠溶液中分离溶质时不能将溶液蒸发至干;加热浓缩硫代硫酸钠溶液,当温度较低时会析出晶体,在冷却时,溶液表面温度较低,先析出晶体;
故答案为:蒸干会使硫代硫酸钠脱水并分解;因为溶液表面温度较低;
(4)硫代硫酸钠易溶于水,难溶于乙醇,在洗涤硫代硫酸钠晶体时,为了减少晶体的溶解,用乙醇来洗涤,乙醇的结构式为:
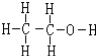 ;
;故答案为:
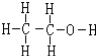 ;
;(5)在锥形瓶中加入25mL 0.0lmol•L-1KIO3溶液,并加入过量的KI并酸化,发生下列反应:5I-+IO3-+6H+═3I2+3H2O,再加入几滴淀粉溶液,立即用所配Na2S2O3溶液滴定,发生反应:I2+2S2O32-═2I-+S4O62-,
则可得关系式:IO3-~6S2O32-,
1mol 6mol
0.025L×0.0lmol•L-1 n(S2O32-)
则n(S2O32-)=0.0015mol,
第三次实验的数据误差较大,舍去,
所以250mL硫代硫酸钠溶液中硫代硫酸钠的物质的量为0.0015mol×
| 250 | ||
(19.98+20.02)×
|
则硫代硫酸钠的质量为0.01875mol×248g/mol=4.65g,
则该产品的纯度是
| ,4.65 |
| 5 |
A.滴定管末用Na2S2O3溶液润洗,则Na2S2O3溶液会被稀释,所以测出硫代硫酸钠的质量偏小,故纯度偏小,故A选;
B.滴定终点时仰视读数,使Na2S2O3溶液体积偏大,计算出的硫代硫酸钠的质量偏小,故纯度偏小,故B选;
C.锥形瓶用蒸馏水润洗,对实验结果没影响,纯度不变,故C不选;
D.滴定管尖嘴处滴定前无气泡,滴定终点发现气泡,使读出的Na2S2O3的体积变小,计算出原溶液中的硫代硫酸钠的质量偏大,则纯度偏大,故D不选.
故答案为:93%;AB.
看了硫代硫酸钠(Na2S2O3•5...的网友还看了以下:
我国北方农村农民常在菜窖里储存几桶水,是因为?A水比热容大,气温升高时放出的热量较多,使储存的蔬菜 2020-07-06 …
下列有关实验说法正确的是()A.在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒 2020-11-24 …
下列说法不正确的是()A.在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒进行搅 2020-11-24 …
下列有关实验说法正确的是A.在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、普通玻璃棒进行 2020-11-24 …
“封管实验”具有简易、方便、节约、绿色等优点,观察下面四个“封管实验”(夹持装置未画出),判断下列说 2020-12-19 …
金属的下列性质中,与自由电子无关的是()A.易导热B.容易导电C.延展性好D.密度大小 2020-12-24 …
金属的下列性质中,与自由电子无关的是()A.易导热B.容易导电C.延展性好D.密度大小 2020-12-24 …
金属的下列性质中,与自由电子无关的是()A.易导热B.容易导电C.延展性好D.密度大小 2020-12-24 …
在光的色散实验中,小明在测量不同色光区域的温度时,他将温度计的玻璃泡涂黑,可以使温度计更加灵敏,这是 2020-12-25 …
下列关于探究“防止食物腐败的方法”的实验,叙述错误的是()A.实验时用到的肉汤必须加热煮沸,目的是消 2020-12-29 …