早教吧作业答案频道 -->化学-->
目前,新能源不断被利用到现代的汽车中,高铁电池技术就是科研机构着力研究的一个方向.(1)高铁酸钾-锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是(填化学
题目详情
目前,新能源不断被利用到现代的汽车中,高铁电池技术就是科研机构着力研究的一个方向.
(1)高铁酸钾-锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是___(填化学式).
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定.反应原理为
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4↓+3NaCl+6NaNO3+5H2O.
Ⅱ.Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH═K2FeO4+2NaOH.
主要的生产流程如图1:
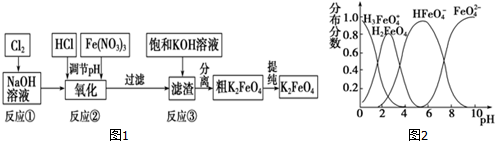
①写出反应①的离子方程式:___.
②流程图中反应③是在某低温下进行的,且此温度无NaOH析出,说明此温度下
Ksp(K2FeO4)___Ksp(Na2FeO4)(填“>”、“<”或“=”).
(3)已知K2FeO4在水溶液中可以发生:4FeO
+10H2O⇌4Fe(OH)3↓+8OH-+3O2↑,则K2FeO4在水处理中的作用是___.
(4)FeO
在水溶液中的存在形态如图2所示.
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO
的分布分数的变化情况是___.
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,___转化为___(填化学式).
(1)高铁酸钾-锌电池(碱性介质)是一种典型的高铁电池,则该种电池负极材料是___(填化学式).
(2)工业上常采用NaClO氧化法生产高铁酸钾(K2FeO4),K2FeO4在碱性环境中稳定,在中性和酸性条件下不稳定.反应原理为
Ⅰ.在碱性条件下,利用NaClO氧化Fe(NO3)3制得Na2FeO4:3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4↓+3NaCl+6NaNO3+5H2O.
Ⅱ.Na2FeO4与KOH反应生成K2FeO4:Na2FeO4+2KOH═K2FeO4+2NaOH.
主要的生产流程如图1:

①写出反应①的离子方程式:___.
②流程图中反应③是在某低温下进行的,且此温度无NaOH析出,说明此温度下
Ksp(K2FeO4)___Ksp(Na2FeO4)(填“>”、“<”或“=”).
(3)已知K2FeO4在水溶液中可以发生:4FeO
| 2- 4 |
(4)FeO
| 2- 4 |
①若向pH=10的这种溶液中加硫酸至pH=2,HFeO
| - 4 |
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,___转化为___(填化学式).
▼优质解答
答案和解析
(1)高铁酸钾-锌电池(碱性介质)中,高铁酸钾是氧化剂在正极反应,锌易失电子是还原剂发生氧化反应而作负极,故答案为:Zn;(2)①氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水,离子反应方程式为:Cl2+2OH-=Cl-+...
看了目前,新能源不断被利用到现代的...的网友还看了以下:
如图是玉米种子纵剖面结构示意图,请据图回答问题:(“[]”内填写图中标号,“”上填写相关的内容)( 2020-05-13 …
(2011•宝山区一模)物理知识在生产和生活中有着广泛应用,用吸管吸饮料利用的是的知识;液体密度计 2020-06-23 …
如图是显微镜结构图,请据图回答:([]内填数字,横线上填名称)(1)取送显微镜时,右手握,左手托. 2020-06-27 …
屈肘运动时,起杠杆作用的是肱骨和桡骨等,作为支点的是(填“肘关节”或“肩关节”),处于收缩状态并起 2020-06-28 …
金属材料应用广泛.(1)在空气中(填“铝”或“铁”)制品更耐腐蚀.(2)人们大量使用的是合金而不是 2020-07-07 …
回顾《呼风唤雨的世纪》一课,想想它们用的是什么说明方法,将序号填在括号内。A.打比方B.作比较C� 2020-07-16 …
图1中A、B、C分别表示绿色植物的某些生理过程,图2是绿色植物叶片横切面结构示意图.请回答:(横线 2020-07-31 …
一道英语填空题It'sOKtohavenothinginyourpocket,butit'llbe 2020-08-01 …
英语填空Whatdidyoumakeit?Milkandeggs.填什么介词合适可是答案用的是wit 2020-11-03 …
(9分)下图为显微镜构造示意图,请据图回答问题。(在[]里填图中数字、短线上填文字;示例:[10]镜 2020-11-26 …