早教吧作业答案频道 -->化学-->
酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素.Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓
题目详情
酸性KMnO4溶液能与草酸(H2C2O4)溶液反应.某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素.
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的离子方程式为___.
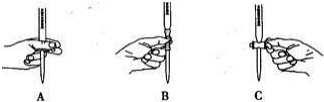
(2)滴定过程中操作滴定管的图示正确的是___.
(3)若配制酸性KMnO4标准溶液时,俯视容量瓶的刻度线,会使测得的草酸溶液浓度___(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
(4)表中实验目的a的内容是___
(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
分析上述数据后得出“当其它条件相同时,酸性高锰酸钾溶液的浓度越小,褪色时间就越短,即反应速率就越快”的结论.某同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到了错误的实验结论,请简述改进的实验方案___.
(6)该实验中使用的催化剂应选择MnSO4并非MnCl2,原因为___(离子方程式表示).
Ⅰ.实验前首先用浓度为0.1000mol•L-1酸性KMnO4标准溶液滴定未知浓度的草酸.
(1)写出滴定过程中发生反应的离子方程式为___.
(2)滴定过程中操作滴定管的图示正确的是___.

(3)若配制酸性KMnO4标准溶液时,俯视容量瓶的刻度线,会使测得的草酸溶液浓度___(填“偏高”、“偏低”、或“不变”).
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol•L-1.用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL).
| 实验编号 | 温度(℃) | 催化剂用量(g) | 酸性高锰酸钾溶液 | 实验目的 a.实验1和2是…. b.实验1 和3 探究反应物浓度对该反应速率的影响; c.实验1 和4探究催化剂对该反应速率的影响. | |
| 体积(mL) | 浓度 (mol•L-1) | ||||
| 1 | 25 | 0.5 | 4 | 0.1000 | |
| 2 | 50 | 0.5 | 4 | 0.1000 | |
| 3 | 25 | 0.5 | 4 | 0.0100 | |
| 4 | 25 | 0 | 4 | 0.1000 | |
(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| 实验编号 | 溶液褪色所需时间(min) | ||
| 第1 次 | 第2 次 | 第3 次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 3 | 6.5 | 6.7 | 6.8 |
(6)该实验中使用的催化剂应选择MnSO4并非MnCl2,原因为___(离子方程式表示).
▼优质解答
答案和解析
Ⅰ.(1)高锰酸钾具有强氧化性,把草酸中的C从+3价氧化成+4价的二氧化碳,Mn元素从+7价变化到+2价的锰离子,由于草酸分子中有2个C原子,根据得失电子守恒,高锰酸钾与草酸的反应比例为 5:2,故反应的方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(2)根据滴定管的使用规则,滴定时,左手包住滴定管的活塞控制液滴的滴出,防止活塞被意外打开,即如图A所示操作,
故答案为:A;
(3)配置酸性KMnO4标准溶液时,俯视容量瓶的刻度线,溶液的体积偏小,配制的溶液的浓度偏大,滴定时消耗的高锰酸钾溶液的体积偏小,则消耗的高锰酸钾的物质的量偏小,由2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O可知,测定的草酸的物质的量偏小,即测得的草酸溶液浓度偏低,
故答案为:偏低;
Ⅱ.(4)实验1、2反应物用量完全相同,只有温度不同,目的就在于探究温度不同对反应速率的影响,
故答案为;探究温度不同对反应速率的影响;
(5)因根据表格中的褪色时间长短来判断浓度大小与反应速率的关系,需满足高锰酸钾的物质的量相同,浓度不同的草酸溶液,
故答案为:其它条件相同时,利用等量且少量的高锰酸钾与等体积不同浓度的足量草酸溶液反应,测量溶液褪色时间;
(6)酸性条件下,高锰酸根离子能将氯离子氧化成氯气,自身被还原成二价锰离子,反应方程式为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O,
故答案为:2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
故答案为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O;
(2)根据滴定管的使用规则,滴定时,左手包住滴定管的活塞控制液滴的滴出,防止活塞被意外打开,即如图A所示操作,
故答案为:A;
(3)配置酸性KMnO4标准溶液时,俯视容量瓶的刻度线,溶液的体积偏小,配制的溶液的浓度偏大,滴定时消耗的高锰酸钾溶液的体积偏小,则消耗的高锰酸钾的物质的量偏小,由2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O可知,测定的草酸的物质的量偏小,即测得的草酸溶液浓度偏低,
故答案为:偏低;
Ⅱ.(4)实验1、2反应物用量完全相同,只有温度不同,目的就在于探究温度不同对反应速率的影响,
故答案为;探究温度不同对反应速率的影响;
(5)因根据表格中的褪色时间长短来判断浓度大小与反应速率的关系,需满足高锰酸钾的物质的量相同,浓度不同的草酸溶液,
故答案为:其它条件相同时,利用等量且少量的高锰酸钾与等体积不同浓度的足量草酸溶液反应,测量溶液褪色时间;
(6)酸性条件下,高锰酸根离子能将氯离子氧化成氯气,自身被还原成二价锰离子,反应方程式为2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O,
故答案为:2MnO4-+10Cl-+16H+=5Cl2↑+2Mn2++8H2O.
看了酸性KMnO4溶液能与草酸(H...的网友还看了以下:
草酸麻黄碱和氯化钙反应式草酸盐麻黄碱和氯化钙溶液反应,反应式啥样子?反应后生成的盐酸盐麻黄碱易溶于 2020-05-16 …
如图所示,在载玻片上滴三种液体,甲为高浓度的盐水,乙为草履虫及其培养液,丙是清水.用解剖针先将甲乙 2020-05-17 …
草甘膦(化学式为C3H8NO5P)是一种有机磷除草剂,白色结晶,易溶于水、乙醇等.计算:(1)草甘 2020-06-16 …
实验室制备溴苯的实验步骤如下:步骤1:在a中加入苯和少量铁屑,将b中液溴慢慢加入到a中,充分反应; 2020-07-04 …
(1)草酸(H2C2O4,其中H的化合价为+1,O的化合价为-2)能使高锰酸钾溶液褪色,其反应的离 2020-07-05 …
已知25℃时,Ksp(CaSO4)=7.10×10-5.在1L0.1mol·L-1CaCl2溶液中 2020-07-22 …
草酸是二元中强酸,测得0.01mol·L-1的草酸氢钠溶液显酸性。常温下,向10mL0.01mol 2020-07-25 …
如何从只含硫酸铜废液中提取铜和硫酸亚铁原题为:CuSO4+A物质=固体1+液体1﹑固体1+B物质=C 2020-11-03 …
(2010•揭阳模拟)草酸(H2C2O4)是一种有机二元酸,水溶液中草酸的存在形态有三种,各形态的浓 2020-11-12 …
如图所示,在载玻片上滴三种液体,甲为高浓度的盐水,乙为草履虫及其培养液,丙是清水.用解剖针先将甲乙两 2021-01-14 …