研究离子晶体,常考查1个离子为中心时其周围不同距离的离子对它的吸引和排斥的静电作用力。设NaCl晶体中Na+与离它最近的Cl-之间的距离为d以其中1个Na+为中心,其他离子可看
(1)第二层离子是____________离子,有____________个,离中心离子的距离为___________。
(2)纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的根本原因。假设某氯化钠纳米颗粒的大小和形状恰好和NaCl晶胞的相同,求这种纳米颗粒的表面原子占总原子数的百分比。
(3)假设某氯化钠颗粒也是立方体,但其边长为NaCl晶胞边长的10倍,试估算表面原子占总原子数的百分比。
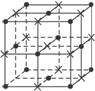
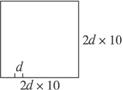
解析:解本题时,要弄清NaCl晶体的排列规则,如图所示,●为Cl - ,×为Na + ,Na + 处于立方体的中心和12条棱的中心,Cl - 处于立方体的顶点和面心。离中心Na + 最近的是6个处于面心的Cl - (第一层),其次近的是12个Na + (第二层)。将Na + 和Cl - 均看成小球,它们的间距为d,则在1个NaCl晶胞中共有小球3×3×3=27个,其中只有1个处于体心,另外26个都在表面上,所以表面原子占原子总数的百分比很容易得出。假设将晶胞的立方体边长扩大为原来的10倍,从其表面图可以看出,晶体的边长为20d,可放2×10+1=21个小球,所以共有21 3 =9 261个小球;其中,顶点8个,棱心:21-2=19个,面心:19 2 =361个。所以,表面球为8+19×12+19 2 ×6=2 402个。由此得到答案为 ![]() ×100%=26%。
×100%=26%。
答案:(1)Na + 12 ![]() d
d
(2) ![]() ×100%=96%
×100%=96%
(3) ![]() ×100%=26%
×100%=26%
谜语:1.它就像一只鸟,但没有羽毛。它就像一只蜻蜓,但没有腿。它可以在天上飞,而且又可以在2.什么 2020-06-08 …
如果人生是.那么家是.它可以.它可以. 2020-06-14 …
有一只兔子挖了一百个罗卜方在一起、它要把这些罗卜背回家、它家离那里有五十米远.它每次最多可以背五十 2020-06-15 …
英语怎么说:收件地址是错误的,所以它可能在路上多耽误了一天 2020-06-18 …
1一种新型材料B4C,具有很高的熔沸点和硬度,它可以用于制作切削工具,高温变换器,关于B4C说法正 2020-06-24 …
这句句是不是拟人?哪里拟人了?仿写的话应该前半句拟人还是后半句?绳子可以断木,它是在告诉我们做事应持 2020-11-26 …
仿写句子,100分我可以使它度过一个有意义的人生,也可以使它荒废,庸碌一生仿写:我可以也可以,.谢谢 2020-11-28 …
中微子是一种质量几乎为零,伴随着β衰变和其他一些物理过程而产生的微小粒子.由于它是如此之小,所以它可 2020-12-17 …
有没有办法让一颗人造卫星固定在地球的北极或者南极上空?地球同步卫星的公转周期跟地球的自转周期一样,所 2020-12-21 …
cellpreparations是什么意思?preparation还有制剂的意思,所以它可能有细胞制 2021-01-08 …