早教吧作业答案频道 -->化学-->
某科研单位利用石油裂解的副产物CH4来制取CO和H2,其生产流程如图1:(1)该流程第Ⅰ步反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图2.
题目详情
某科研单位利用石油裂解的副产物CH4来制取CO和H2,其生产流程如图1:
(1)该流程第Ⅰ步反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图2.则P1___P2.(填“<”、“>”或“=”).该反应的平衡常数的表达式K=___.
(2)此流程的第Ⅱ步反应的平衡常数随温度的变化如表:
①从上表分析推断,该反应是△H___0(填“<”、“>”或“=”).
②在500℃时,设起始时CO和H2O的起始浓度均为0.010mol/L-1,在该条件下,反应达到平衡时,CO的转化率为___.
③如图3表示该反应在t1时刻达到平衡,在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件可能是___(写出两种).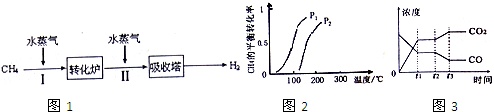
(1)该流程第Ⅰ步反应为:CH4(g)+H2O(g)⇌CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图2.则P1___P2.(填“<”、“>”或“=”).该反应的平衡常数的表达式K=___.
(2)此流程的第Ⅱ步反应的平衡常数随温度的变化如表:
| 温度/℃ | 300 | 500 | 830 |
| 平衡常数K | 12 | 9 | 1 |
②在500℃时,设起始时CO和H2O的起始浓度均为0.010mol/L-1,在该条件下,反应达到平衡时,CO的转化率为___.
③如图3表示该反应在t1时刻达到平衡,在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件可能是___(写出两种).

▼优质解答
答案和解析
(1)由图可知温度相同时,到达平衡时,压强为P1的CH4转化率高,平衡向正反应方向移动,反应为气体体积增大的反应,增大压强平衡向体积减小的方向移动,即P12;平衡常数K=
,故答案为:<;
;
(2)①分析图表数据可知平衡常数随温度升高减小,说明平衡逆向进行,正反应是放热反应,△H<0,故答案为:<;
②设一氧化碳浓度的变化为x,则
CO(g)+H2O(g)⇌H2(g)+CO2(g),
初起量(mol/L-1):0.010 0.010 0 0
变化量(mol/L-1):x x x x
平衡量(mol/L-1):0.01-x 0.01-x x x
在500℃时达平衡,
=9,解之得:x=
,所以CO的转化率为
×100%=75%,故答案为:75%;
③反应是气体体积不变的放热反应,在t2时刻因改变某个条件浓度发生变化的情况是二氧化碳浓度增大,一氧化碳浓度减小,说明平衡正向进行,降低温度,或增加水蒸气的量或减少氢气的量均可以实现,
故答案为:降低温度,或增加水蒸汽的量,或减少氢气的量.
| c(CO)c3(H2) |
| c(CH4)c(H2O) |
| c(CO)c3(H2) |
| c(CH4)c(H2O) |
(2)①分析图表数据可知平衡常数随温度升高减小,说明平衡逆向进行,正反应是放热反应,△H<0,故答案为:<;
②设一氧化碳浓度的变化为x,则
CO(g)+H2O(g)⇌H2(g)+CO2(g),
初起量(mol/L-1):0.010 0.010 0 0
变化量(mol/L-1):x x x x
平衡量(mol/L-1):0.01-x 0.01-x x x
在500℃时达平衡,
| x2 |
| (0.01-x)2 |
| 0.03 |
| 4 |
| ||
| 0.01 |
③反应是气体体积不变的放热反应,在t2时刻因改变某个条件浓度发生变化的情况是二氧化碳浓度增大,一氧化碳浓度减小,说明平衡正向进行,降低温度,或增加水蒸气的量或减少氢气的量均可以实现,
故答案为:降低温度,或增加水蒸汽的量,或减少氢气的量.
看了某科研单位利用石油裂解的副产物...的网友还看了以下:
介质材料中的“谐振频率温度系数”和Qf是什么概念,或者哪些书上有的呢介质材料有三个主要性能,“介电 2020-05-13 …
化学反应速率中的化学反应速率之比等于反应方程式的计量数之比,该怎样去理解?以N2+3H2=2NH3 2020-05-16 …
关于反应2NH3(g)=N2(g)+3H2(g)的平衡移动..反应2NH3(g)=N2(g)+3H 2020-05-17 …
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下,在密闭容器中用H2还原WO 2020-06-12 …
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO 2020-06-19 …
金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下密闭容器中用H2还原WO3可 2020-06-19 …
反应2NH3(g)=N2(g)+3H2(g),恒温恒容,达到平衡后充入等温的NH3气体,平衡向哪移 2020-06-23 …
下丘脑中的热敏神经元在温度上升时冲动频率增加,冷敏神经元在温度下降时冲动频率增加,引起机体的散热和 2020-07-08 …
下丘脑中的热敏神经元在温度上升时冲动频率增加,冷敏神经元在温度下降时冲动频率增加,引起机体的散热和产 2020-11-23 …
(2014•雅安模拟)我省有着丰富的天然气资源,许多化肥厂用天然气在高温、催化剂作用下与水蒸气反应来 2021-02-19 …