早教吧作业答案频道 -->化学-->
过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至350℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2,过氧化钙可用于改善水质、处
题目详情
过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至350℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2,过氧化钙可用于改善水质、处理含重金属粒子废水和治理赤潮,也可用于应急供氧等,是一种重要化工试剂.
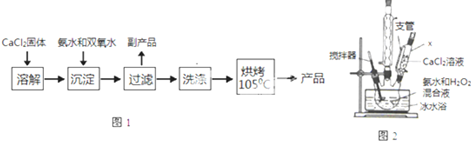
(Ⅰ)CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl实验步骤如图1,反应装置如图2所示,请回答下列问题:
(1)仪器x的名称为___
(2)用平衡移动原理解释加入氨水的作用是___.
(3)沉淀反应时常用冰水浴控制温度在0℃左右,其可能原因是___、___(写出两种)
(4)过滤后洗涤沉淀的试剂最好用___
A.热水 B.冷水 C.乙醇 D.乙醚
(Ⅱ)CaO2纯度检测,将一定量CaO2溶于稀硫酸,用标准KMnO4溶于滴定生成的H2O2(KMnO4反应后生成Mn2+)计算确定CaO2的含量.
(5)现每次称取0.4000g样品溶解后,用0.1000mol/L的KMnO4溶液滴定所得数据如表所示,则CaO2样品的纯度___
(6)测得CaO2纯度偏低的原因可能是___
A.烘烤时间不足
B.在洁净干燥的酸式滴定管中未润洗即装标准液
C.滴定前尖嘴处有气泡.滴定后消失
D.配置KMnO4标准溶液定容时俯视容量瓶标线.

(Ⅰ)CaO2的制备原理:CaCl2+H2O2+2NH3•H2O+6H2O═CaO2•8H2O↓+2NH4Cl实验步骤如图1,反应装置如图2所示,请回答下列问题:
(1)仪器x的名称为___
(2)用平衡移动原理解释加入氨水的作用是___.
(3)沉淀反应时常用冰水浴控制温度在0℃左右,其可能原因是___、___(写出两种)
(4)过滤后洗涤沉淀的试剂最好用___
A.热水 B.冷水 C.乙醇 D.乙醚
(Ⅱ)CaO2纯度检测,将一定量CaO2溶于稀硫酸,用标准KMnO4溶于滴定生成的H2O2(KMnO4反应后生成Mn2+)计算确定CaO2的含量.
(5)现每次称取0.4000g样品溶解后,用0.1000mol/L的KMnO4溶液滴定所得数据如表所示,则CaO2样品的纯度___
| 实验序号 | 第1次 | 第2次 | 第3次 | 第4次 |
| 消耗KMnO4体积/mL | 19.98 | 20.02 | 20.20 | 20.00 |
A.烘烤时间不足
B.在洁净干燥的酸式滴定管中未润洗即装标准液
C.滴定前尖嘴处有气泡.滴定后消失
D.配置KMnO4标准溶液定容时俯视容量瓶标线.
▼优质解答
答案和解析
(Ⅰ)(1)图2中仪器X为恒压滴液漏斗(或恒压分液漏斗,起到冷凝作用,
故答案为:恒压滴液漏斗(或恒压分液漏斗);
(2)氯化钙与双氧水的反应方程式为:CaCl2+H2O2⇌CaO2+2HCl,加入氨水可以与氯化氢发生中和反应,使该可逆反应向着生成过氧化钙的方向移动,提高的过氧化钙的产率,
故答案为:中和反应生成的HCl,使CaCl2+H2O2⇌CaO2+2HCl向右进行;
(3)由于温度较高时双氧水容易分解,会导致过氧化钙产率下降,且温度降低时过氧化钙的溶解度减小,有利于过氧化钙的析出,所以沉淀反应时常用冰水浴控制温度在0℃左右,
故答案为:减少双氧水受热分解;降低产物溶解度便于析出(或该反应放热);
(4)A.热水:过氧化钙在热水中溶解度较大,降低了过氧化钙的产率,故A错误;
B.冷水:过氧化钙极微溶于水,且杂质都易溶于水,可用冷水洗涤过氧化钙,故B正确;
C.乙醇:过氧化钙不溶于乙醇,但是杂质不溶于乙醇,且提高了成本,故C错误;
D.乙醚:过氧化钙不溶于乙醚,但杂质也不溶于乙醚,且乙醚成本较高,故D错误;
故答案为:B;
(Ⅱ)、(5)根据表中消耗高锰酸钾溶液的体积数据可知,第三次数据与其它三组误差较大,应该舍弃;则滴定中消耗酸性高锰酸钾的平均体积为:
mL=20.00mL,每次滴定消耗的高锰酸钾的物质的量为:n(KMnO4)=0.1000mol/L×0.02L=0.002mol,
KMnO4反应后生成Mn2+,化合价降低7-2)=5价,CaO2被氧化成氧气,化合价从-1升高到0价,至少升高:[0-(-1)]×2=2,根据化合价升降相等可得反应的关系式:2KMnO4~5CaO2,则每次称取0.4000g样品中含有的过氧化钙的物质的量为:n(CaO2)=
×n(KMnO4)=0.002mol×
=0.005mol,
所以该样品中过氧化钙的纯度为:
×100%=90.00%,
故答案为:90.00%;
(6)A.烘烤时间不足,样品中含有杂质水分,导致样品中过氧化钙的纯度偏小,故A正确;
B.在洁净干燥的酸式滴定管中未润洗即装标准液,标准液被蒸馏水稀释,滴定时消耗的标准液体积偏大,计算出的过氧化钙的纯度偏大,故B错误;
C.滴定前尖嘴处有气泡,滴定后消失,导致消耗的标准液体积偏大,根据关系式计算出的过氧化钙的质量偏大,过氧化钙的纯度偏高,故C错误;
D.配制KMnO4标准溶液定容时俯视容量瓶标线,导致标准液浓度偏高,滴定过程中营养样品中过氧化钙的物质的量不变,则消耗的标准液体积偏小,测定的过氧化钙的纯度偏小,故D正确;
故答案为:AD.
故答案为:恒压滴液漏斗(或恒压分液漏斗);
(2)氯化钙与双氧水的反应方程式为:CaCl2+H2O2⇌CaO2+2HCl,加入氨水可以与氯化氢发生中和反应,使该可逆反应向着生成过氧化钙的方向移动,提高的过氧化钙的产率,
故答案为:中和反应生成的HCl,使CaCl2+H2O2⇌CaO2+2HCl向右进行;
(3)由于温度较高时双氧水容易分解,会导致过氧化钙产率下降,且温度降低时过氧化钙的溶解度减小,有利于过氧化钙的析出,所以沉淀反应时常用冰水浴控制温度在0℃左右,
故答案为:减少双氧水受热分解;降低产物溶解度便于析出(或该反应放热);
(4)A.热水:过氧化钙在热水中溶解度较大,降低了过氧化钙的产率,故A错误;
B.冷水:过氧化钙极微溶于水,且杂质都易溶于水,可用冷水洗涤过氧化钙,故B正确;
C.乙醇:过氧化钙不溶于乙醇,但是杂质不溶于乙醇,且提高了成本,故C错误;
D.乙醚:过氧化钙不溶于乙醚,但杂质也不溶于乙醚,且乙醚成本较高,故D错误;
故答案为:B;
(Ⅱ)、(5)根据表中消耗高锰酸钾溶液的体积数据可知,第三次数据与其它三组误差较大,应该舍弃;则滴定中消耗酸性高锰酸钾的平均体积为:
| 19.98+20.02+20.00 |
| 3 |
KMnO4反应后生成Mn2+,化合价降低7-2)=5价,CaO2被氧化成氧气,化合价从-1升高到0价,至少升高:[0-(-1)]×2=2,根据化合价升降相等可得反应的关系式:2KMnO4~5CaO2,则每次称取0.4000g样品中含有的过氧化钙的物质的量为:n(CaO2)=
| 5 |
| 2 |
| 5 |
| 2 |
所以该样品中过氧化钙的纯度为:
| 0.005mol×72g/mol |
| 0.4000g |
故答案为:90.00%;
(6)A.烘烤时间不足,样品中含有杂质水分,导致样品中过氧化钙的纯度偏小,故A正确;
B.在洁净干燥的酸式滴定管中未润洗即装标准液,标准液被蒸馏水稀释,滴定时消耗的标准液体积偏大,计算出的过氧化钙的纯度偏大,故B错误;
C.滴定前尖嘴处有气泡,滴定后消失,导致消耗的标准液体积偏大,根据关系式计算出的过氧化钙的质量偏大,过氧化钙的纯度偏高,故C错误;
D.配制KMnO4标准溶液定容时俯视容量瓶标线,导致标准液浓度偏高,滴定过程中营养样品中过氧化钙的物质的量不变,则消耗的标准液体积偏小,测定的过氧化钙的纯度偏小,故D正确;
故答案为:AD.
看了过氧化钙(CaO2)是一种白色...的网友还看了以下:
根据资料部分列出的“20℃时部分酸、碱、盐的溶解性表”,完成以下任务:OH-Cl-CO32-SO4 2020-04-11 …
1、为什么化学反应大多数都是在溶液中才能进行啊?2、硫酸钙是微溶物吧,亚硫酸钙好像也是微溶物吧,那 2020-04-26 …
硫酸钠溶液与氯化钙溶液混合 会反应吗若反应 生成的硫酸钙是微溶的 算沉淀吗是不是所有的微溶物质都能 2020-05-16 …
微溶于水的盐有哪些?碳酸氢钠、碳酸氢钙、碳酸氢铵、硫酸氢钠、硫酸钙是微溶还是难溶? 2020-07-05 …
酸碱盐溶解性表是学习化学的重要工具,下表列出了部分酸碱盐在20℃的溶解性.你能利用下表完成下列任务 2020-07-11 …
(2010•新乡一模)酸、碱盐溶解性表示学习化学的重要工具.下表列出了部分酸、碱、盐在20℃时的溶 2020-07-11 …
酸、碱、盐溶解性表是学习化学的重要工具.你表列出m“部分酸、碱、盐在40℃时的溶解性.”O0ˉNO 2020-07-11 …
根据表格回答:部分酸、碱和盐在水中的溶解性(20℃)部分酸、碱和盐在水中的溶解性(20℃)阴离子阳 2020-07-16 …
海藻酸钠能配成10%的溶度吗?怎样配?海藻酸钠是微溶的,在水中不加任何助溶剂和不加热的情况下最高大概 2020-12-12 …
硫酸钙碳酸镁硫酸银是微溶,常温下他们的溶解度大不大.常温下是是为溶还是不溶 2021-01-12 …