早教吧作业答案频道 -->化学-->
铁合金及铁的化合物在生产、生活中有着重要的用途.(1)已知铁是26号元素,写出Fe2+的电子排布式.(2)已知三氯化铁固体在300℃以上可升华成含二聚三氯化铁(Fe2Cl6)分子的气体,
题目详情
铁合金及铁的化合物在生产、生活中有着重要的用途.
(1)已知铁是26号元素,写出Fe2+的电子排布式___.
(2)已知三氯化铁固体在300℃以上可升华成含二聚三氯化铁(Fe2Cl6)分子的气体,该分子中所有原子均满足最外层8电子的稳定结构,则该分子的结构式为___,你认为该分子是否为平面形分子?___(填“是”或“否”).
(3)六氰合亚铁酸钾K4[Fe(CN)6]俗称黄血盐,它可用做显影剂,该化合物中存在的微粒间相互作用类型有___(从下列选项中选填代号).
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(4)黄血盐在溶液中可电离出极少量的CN-,CN-与___(填一种即可)互为等电子体.CN-还可与H+结合形成一种弱酸--氢氰酸(HCN),HCN分子中碳原子的杂化轨道类型是___,该分子的σ键和π键数目分别为___.
(5)黄血盐溶液与Fe3+反应可生成一种蓝色沉淀,该物质最早由1704年英国普鲁士的一家染料厂的工人发现,因此取名为普鲁士蓝,化学式可表示为K4[Fe(CN)6].研究表明它的晶体的结构特征是Fe2+、Fe3+分别占据立方体的顶点,且自身互不相邻,而CN-位于立方体的棱上与Fe2+、Fe3+配位,K+填充在上述微粒形成的部分空隙中.忽略K+,该晶体的结构示意图如下四幅图所示:
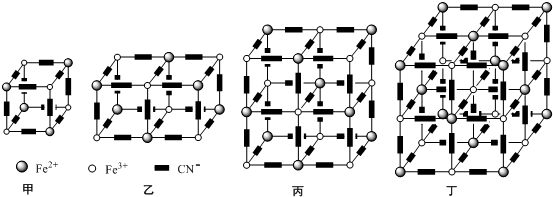
根据图可得普鲁士蓝的化学式为___,忽略K+,上述四幅晶体结构图中,图___是普鲁士蓝的晶胞.
(1)已知铁是26号元素,写出Fe2+的电子排布式___.
(2)已知三氯化铁固体在300℃以上可升华成含二聚三氯化铁(Fe2Cl6)分子的气体,该分子中所有原子均满足最外层8电子的稳定结构,则该分子的结构式为___,你认为该分子是否为平面形分子?___(填“是”或“否”).
(3)六氰合亚铁酸钾K4[Fe(CN)6]俗称黄血盐,它可用做显影剂,该化合物中存在的微粒间相互作用类型有___(从下列选项中选填代号).
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(4)黄血盐在溶液中可电离出极少量的CN-,CN-与___(填一种即可)互为等电子体.CN-还可与H+结合形成一种弱酸--氢氰酸(HCN),HCN分子中碳原子的杂化轨道类型是___,该分子的σ键和π键数目分别为___.
(5)黄血盐溶液与Fe3+反应可生成一种蓝色沉淀,该物质最早由1704年英国普鲁士的一家染料厂的工人发现,因此取名为普鲁士蓝,化学式可表示为K4[Fe(CN)6].研究表明它的晶体的结构特征是Fe2+、Fe3+分别占据立方体的顶点,且自身互不相邻,而CN-位于立方体的棱上与Fe2+、Fe3+配位,K+填充在上述微粒形成的部分空隙中.忽略K+,该晶体的结构示意图如下四幅图所示:

根据图可得普鲁士蓝的化学式为___,忽略K+,上述四幅晶体结构图中,图___是普鲁士蓝的晶胞.
▼优质解答
答案和解析
(1)铁是26号元素,核外电子排布式为1s22s22p63s23p63d64s2,失去4s能级2个电子形成Fe2+,Fe2+离子的核外电子排布式为:1s22s22p63s23p63d6,
故答案为:1s22s22p63s23p63d6;
(2)二聚三氯化铁(Fe2Cl6)分子的气体,该分子中所有原子均满足最外层8电子的稳定结构,Fe与氯原子之间形成4个共价键,有2个Cl原子形成分别与2个Fe原子之间形成2个共价键,存在配位键,所以其结构式为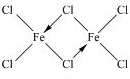 ;
;
该分子中每个铁原子生成四个共价键,则铁原子和四个氯原子形成四面体结构,则该分子不是平面形结构,
故答案为 ;否;
;否;
(3)K4[Fe(CN)6]中阴阳离子之间存在离子键,Fe3+和CN-之间存在配位键,CN-内原子之间形成共价键,
故答案为:ABD;
(4)原子数目相等、价电子总数相等的微粒互为电子,CN-与CO、N2等互为等电子体;等电子体结构相似,可知HCN的结构式为H-C≡N,C原子杂化轨道数目为2,所以碳原子为sp杂化,单键为σ键,三键含有1个σ键、2个π键,分子中含有22个σ键、2个π键,
故答案为:CO;sp;2,2;
(5)立方体结构中Fe3+离子的个数为:4×
=
,Fe2+离子的个数为:4×
=
,CN-离子的个数为:12×
=3,
根据电荷守恒:N(K+)+N(Fe3+)×3+N(Fe2+)×2=N(CN-),得N(K+)=
,
普鲁士蓝中 n(K+):n(Fe3+):n(Fe2+):n(CN-)=1:1:1:6,则其化学式为KFe2(CN)6;
晶胞为其最小重复单位,一般情况下,晶胞都是平行六面体.整块晶体可以看成是无数晶胞无隙并置而成的,要求晶胞的立方体八个顶点微粒相同,图象中丁符合,
故答案为:KFe2(CN)6;丁.
故答案为:1s22s22p63s23p63d6;
(2)二聚三氯化铁(Fe2Cl6)分子的气体,该分子中所有原子均满足最外层8电子的稳定结构,Fe与氯原子之间形成4个共价键,有2个Cl原子形成分别与2个Fe原子之间形成2个共价键,存在配位键,所以其结构式为
 ;
;该分子中每个铁原子生成四个共价键,则铁原子和四个氯原子形成四面体结构,则该分子不是平面形结构,
故答案为
 ;否;
;否;(3)K4[Fe(CN)6]中阴阳离子之间存在离子键,Fe3+和CN-之间存在配位键,CN-内原子之间形成共价键,
故答案为:ABD;
(4)原子数目相等、价电子总数相等的微粒互为电子,CN-与CO、N2等互为等电子体;等电子体结构相似,可知HCN的结构式为H-C≡N,C原子杂化轨道数目为2,所以碳原子为sp杂化,单键为σ键,三键含有1个σ键、2个π键,分子中含有22个σ键、2个π键,
故答案为:CO;sp;2,2;
(5)立方体结构中Fe3+离子的个数为:4×
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
根据电荷守恒:N(K+)+N(Fe3+)×3+N(Fe2+)×2=N(CN-),得N(K+)=
| 1 |
| 2 |
普鲁士蓝中 n(K+):n(Fe3+):n(Fe2+):n(CN-)=1:1:1:6,则其化学式为KFe2(CN)6;
晶胞为其最小重复单位,一般情况下,晶胞都是平行六面体.整块晶体可以看成是无数晶胞无隙并置而成的,要求晶胞的立方体八个顶点微粒相同,图象中丁符合,
故答案为:KFe2(CN)6;丁.
看了铁合金及铁的化合物在生产、生活...的网友还看了以下:
有两块合金,第一块合金中铜和锌的比是2:3,第二块合金中铜和锌的比是4:5,并且两块合金中含铜都是 2020-05-13 …
二元一次方程~就2道题~~急~~~~1.有两种合金,第一种合金含金90%,第二种合金含金80%,这 2020-06-06 …
我认为教材上二元一次方程组的定义,有些模糊。如果方程组中含有两个未知数,且含未知数的项的次数都是一 2020-07-01 …
有两块合金,第一块合金含金270克,含铜30克;第二块合金含金400克,含铜100克,要配置含金0 2020-07-09 …
顺铂(化学名称为二氯二氨合铂).化学式为PtCl2(NH3)2是一种用于治疗癌症的药物,一片顺铂药片 2020-11-01 …
以工业碳酸钙(含少量Na+、Fe3+、Al3+等)为原料可以生产医用二水合氯化钙,其工艺流程如下:已 2020-11-03 …
氨是重要的化工原料,用途广泛.(1)合成氨工厂常用醋酸二氨合铜(由[Cu(NH3)2]+和CH3CO 2020-11-24 …
医用氯化钙可用于补钙、抗过敏和消炎等,以工业碳酸钙(含少量Na+、Al3+、Fe3+等杂质)生产医用 2020-12-13 …
初三化学题急求!医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少.医用二水合氯化 2020-12-13 …
(2014•海陵区一模)医用二水合氯化钙可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3 2021-01-08 …