早教吧作业答案频道 -->化学-->
氨气和NO可在催化剂作用下转化为氮气和水,用如图所示装置可实现反应并测定NO的转化率已知FeSO4溶液能吸收NO生成可溶性的Fe(NO)SO4(棕色),请回答下列问题:(1)实验室制备氨气的化
题目详情
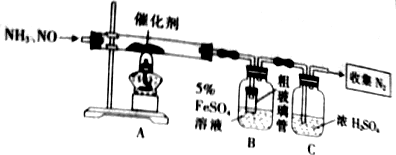
氨气和NO可在催化剂作用下转化为氮气和水,用如图所示装置可实现反应并测定NO的转化率
已知FeSO4溶液能吸收NO生成可溶性的Fe(NO)SO4(棕色),请回答下列问题:
(1)实验室制备氨气的化学方程式为___
(2)配制5%FeSO4溶液使用的仪器除天平、药匙、量筒、烧杯外,还需要___
(3)装置B中粗玻璃管的作用是___,装置C的作用是___
(4)反应开始后发现装置B的广口瓶中有白色沉淀生成,写生成该沉淀的离子方程式:___
(5)若参加反应的NO为2.688L(标准状况,下同),氨气过量,最先收集到2.016LN2,则装置A中NO的转化率为___.

已知FeSO4溶液能吸收NO生成可溶性的Fe(NO)SO4(棕色),请回答下列问题:
(1)实验室制备氨气的化学方程式为___
(2)配制5%FeSO4溶液使用的仪器除天平、药匙、量筒、烧杯外,还需要___
(3)装置B中粗玻璃管的作用是___,装置C的作用是___
(4)反应开始后发现装置B的广口瓶中有白色沉淀生成,写生成该沉淀的离子方程式:___
(5)若参加反应的NO为2.688L(标准状况,下同),氨气过量,最先收集到2.016LN2,则装置A中NO的转化率为___.
▼优质解答
答案和解析
(1)实验室制取氨气是用氯化铵和氢氧化钙固体加热生成氨气和氯化钙、水,其化学方程式是:2NH4Cl+Ca(OH)2
2NH3↑+CaCl2+2H2O;
故答案为:2NH4Cl+Ca(OH)2
2NH3↑+CaCl2+2H2O;
(2)配制5%FeSO4溶液在溶解固体时,需要用到玻璃棒搅拌,所以还缺少的仪器:玻璃棒;
(3)氨气易溶于水,导管直接插入硫酸亚铁溶液中容易发生倒吸,所以装置B中粗玻璃管的作用是防止氨气易溶于水发生倒吸;
生成的氮气中含有水蒸气,通过盛有浓硫酸的洗气瓶可以吸收氮气中的水蒸气;
故答案为:防止氨气易溶于水发生倒吸;干燥;
(4)硫酸亚铁与一水合氨反应生成氢氧化亚铁白色沉淀和铵根离子,离子方程式:Fe2++2NH3•H2O=Fe(OH)2↓+2NH4+;
故答案为:Fe2++2NH3•H2O=Fe(OH)2↓+2NH4+;
(5)氨气与一氧化氮反应的化学方程式6NO+4NH3=5N2+6H2O,
则:6NO+4NH3=5N2+6H2O
6 5
V 2.016L
解得V=2.4129L;
则装置A中NO的转化率为:
×100%=90%;
故答案为:90%.
| ||
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)配制5%FeSO4溶液在溶解固体时,需要用到玻璃棒搅拌,所以还缺少的仪器:玻璃棒;
(3)氨气易溶于水,导管直接插入硫酸亚铁溶液中容易发生倒吸,所以装置B中粗玻璃管的作用是防止氨气易溶于水发生倒吸;
生成的氮气中含有水蒸气,通过盛有浓硫酸的洗气瓶可以吸收氮气中的水蒸气;
故答案为:防止氨气易溶于水发生倒吸;干燥;
(4)硫酸亚铁与一水合氨反应生成氢氧化亚铁白色沉淀和铵根离子,离子方程式:Fe2++2NH3•H2O=Fe(OH)2↓+2NH4+;
故答案为:Fe2++2NH3•H2O=Fe(OH)2↓+2NH4+;
(5)氨气与一氧化氮反应的化学方程式6NO+4NH3=5N2+6H2O,
则:6NO+4NH3=5N2+6H2O
6 5
V 2.016L
解得V=2.4129L;
则装置A中NO的转化率为:
| 2.4129L |
| 2.688L |
故答案为:90%.
看了氨气和NO可在催化剂作用下转化...的网友还看了以下:
关于氧气用途的说法不正确的是()A.氧气可用来炼钢B.氧气可用来灭火C.氧气可用于登山或飞行D.氧 2020-04-11 …
下列物质的用途中,利用其物理性质的是()A.氧气用于气焊气割B.氮气用于食品防腐C.活性炭用于制糖 2020-04-11 …
下列物质的用途中,是利用物质物理性质的是()A.氧气用于炼钢、气焊B.稀有气体用于保护气C.氮气用 2020-04-11 …
汽车气缸容量和马力怎么换算?各位大侠好,请问一下您们一个问题,气缸容量和马力和千瓦时怎么换算.比如 2020-05-16 …
夺命深渊中最后主人公的氧气用完了,利用岩壁上的气泡呼吸,请问这可能么?夺命深渊中最后主人公的氧气用 2020-06-19 …
据图中信息回答下列问题:(1)食品充氮防腐的原因是(2)氧气用于金属切割是因为氧气具有(3)稀有气 2020-06-30 …
划线提问天气用什么问我就是想问Todayissunny划sunny怎么做%> 2020-07-14 …
物理热力学问题·气体膨胀体积增大气体是对外界做功,对气体来说是做正功.气体收缩体积减小是外界对气体做 2020-11-04 …
关于煤气罐的化学爆炸问题请问煤气的成分主要是甲烷吗?不是说化学爆炸必须具备三个条件一是煤气二是空气三 2020-12-18 …
把1Kg25摄式度的水烧开,烧前烧后煤气表的示数分别为456.163立方米,456.178立方米.( 2020-12-24 …