早教吧作业答案频道 -->化学-->
回答下列问题:(1)写出铬(Cr)原子基态核外电子排布式.(2)写出乙酸分子中碳原子的杂化方式,1mol乙酸分子中含有的σ键数目为.(3)运用价层电子对互斥模型判断下列微粒
题目详情
回答下列问题:
(1)写出铬(Cr)原子基态核外电子排布式___.
(2)写出乙酸分子中碳原子的杂化方式___,1mol 乙酸分子中含有的σ键数目为___.
(3)运用价层电子对互斥模型判断下列微粒的立体结构:BF3___、SO42-___.
(4)观察下列四种物质的晶胞,其中有关说法正确的是___.
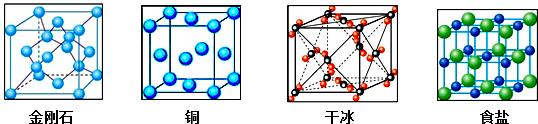
A.金刚石中存在六元碳环
B.铜中原子堆积方式是ABABAB…
C.干冰中有多种取向不同的二氧化碳分子
D.若把食盐晶胞中Na+替换为Cs+,相应得到CsCl的晶胞
E.四种晶体中微粒的配位数分别是4、12、12、6.
(1)写出铬(Cr)原子基态核外电子排布式___.
(2)写出乙酸分子中碳原子的杂化方式___,1mol 乙酸分子中含有的σ键数目为___.
(3)运用价层电子对互斥模型判断下列微粒的立体结构:BF3___、SO42-___.
(4)观察下列四种物质的晶胞,其中有关说法正确的是___.

A.金刚石中存在六元碳环
B.铜中原子堆积方式是ABABAB…
C.干冰中有多种取向不同的二氧化碳分子
D.若把食盐晶胞中Na+替换为Cs+,相应得到CsCl的晶胞
E.四种晶体中微粒的配位数分别是4、12、12、6.
▼优质解答
答案和解析
(1)Cr的原子序数为24,共4个电子层,最外层电子数为1,基态核外电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1,
故答案为:1s22s22p63s23p63d54s1或[Ar]3d54s1;
(2)乙酸为CH3COOH,甲基中C形成4个共价单键,-COOH中C形成1个双键和2个单键,则C的杂化方式分别为sp3、sp2,单键均为σ键,双键中有1个σ键,则1mol 乙酸分子中含有的σ键数目为7 mol,故答案为:sp3、sp2;
(3)BF3分子中心B原子孤电子对数=
=0,价层电子对数=3+0=3,故B原子采取sp2杂化,VSEPR构型为平面三角形,分子的立体构型为平面三角形,
SO42-中含孤电子对为
=0,价层电子对个数都是4,所以空间构型都是正四面体结构,
故答案为:平面正三角形;正四面体;
(4)A.由图可知,金刚石晶体中每个C原子处于其他4个C原子构成的正四面体的内部,向周围无限延伸形成空间立体网状结构,最小的环是立体六元环,故A正确;
B.六方最密堆积按ABABAB…的方式堆积,面心立方堆积按ABCABC…的方式堆积,故B错误;
C.由图可知,面心和顶点分子取向不同,则干冰中有多种取向不同的二氧化碳分子,故C正确;
D.NaCl中阴阳离子配位数是6、CsCl中阴阳离子配位数是8,则二者结构不同,故D错误;
E.金刚石中与C相连的C有4个,铜、干冰均为面心立方结构,氯化钠中钠离子周围有6个氯离子,则四种晶体中微粒的配位数分别是4、12、12、6,故E正确;
故答案为:ACE.
故答案为:1s22s22p63s23p63d54s1或[Ar]3d54s1;
(2)乙酸为CH3COOH,甲基中C形成4个共价单键,-COOH中C形成1个双键和2个单键,则C的杂化方式分别为sp3、sp2,单键均为σ键,双键中有1个σ键,则1mol 乙酸分子中含有的σ键数目为7 mol,故答案为:sp3、sp2;
(3)BF3分子中心B原子孤电子对数=
| 3-3×1 |
| 2 |
SO42-中含孤电子对为
| 6+2-2×4 |
| 2 |
故答案为:平面正三角形;正四面体;
(4)A.由图可知,金刚石晶体中每个C原子处于其他4个C原子构成的正四面体的内部,向周围无限延伸形成空间立体网状结构,最小的环是立体六元环,故A正确;
B.六方最密堆积按ABABAB…的方式堆积,面心立方堆积按ABCABC…的方式堆积,故B错误;
C.由图可知,面心和顶点分子取向不同,则干冰中有多种取向不同的二氧化碳分子,故C正确;
D.NaCl中阴阳离子配位数是6、CsCl中阴阳离子配位数是8,则二者结构不同,故D错误;
E.金刚石中与C相连的C有4个,铜、干冰均为面心立方结构,氯化钠中钠离子周围有6个氯离子,则四种晶体中微粒的配位数分别是4、12、12、6,故E正确;
故答案为:ACE.
看了回答下列问题:(1)写出铬(C...的网友还看了以下:
道尔顿说:“一切物质都是由数量巨大的、极微小的粒子——原子构成的,这些粒子间通过引力互相结合.我们不 2020-03-30 …
纯种甜玉米和纯种非甜玉米间行种植,收获时发现甜玉米果穗有非甜玉米籽粒,而非甜玉米果穗上无甜玉米籽粒 2020-06-14 …
纯种甜玉米和纯种非甜玉米间行种植,收获时发现甜玉米果穗有非甜玉米籽粒,而非甜玉米果穗上无甜玉米籽粒 2020-06-26 …
纯种甜玉米和纯种非甜玉米间行种植,收获时发现甜玉米果穗有非甜玉米籽粒,而非甜玉米果穗上无甜玉米籽粒 2020-06-26 …
A,B,C,三人各有豆若干粒,要求互相赠送.先由A给B,C,所给的豆数等于B,C原来各有的.依相同 2020-07-05 …
A,B,C三人各有豆若干粒,要求互相赠送,先由A给B、C,所给的豆数等于B、C原来各有的豆数,依同 2020-07-05 …
近代著名化学家道尔顿在著作中说:“一切物质都是由数量巨大的、极微小的粒子(原子)构成的,这些粒子间通 2020-11-06 …
A,B,C三人各有糖若干粒,要求互相赠送,先由A给B,C,所给的糖数等于B,C原来各有的糖数,依同法 2020-12-05 …
近代著名化学家道尔顿在著作中说“一切物质都是由数量巨大的、极微小的粒子(原子)构成的,这些粒子间通过 2020-12-07 …
道尔顿在其著作中写道:“一切物质都是由数量巨大的、极微小的粒子(原子)构成的,这些粒子间通过引力互相 2020-12-07 …