早教吧作业答案频道 -->化学-->
稳定的ClO2易溶于水,熔点为一59.5℃,沸点为11℃,能在碱性条件下与H2O2反应,生成ClO2.它是国际公认的新一代高效、广谱、安全杀菌保鲜剂.但液态二氧化氯不稳定,易爆炸,在生产、包
题目详情
稳定的ClO2易溶于水,熔点为一59.5℃,沸点为11℃,能在碱性条件下与H2O2反应,生成ClO2.它是国际公认的新一代高效、广谱、安全杀菌保鲜剂.但液态二氧化氯不稳定,易爆炸,在生产、包装、运输方面不便.固载二氧化氯是用化学方法固化在载体上,使用时再释放出来.工业上NaClO2是制备稳定型固载ClO2的主要原料,采用H2O2、NaClO3和NaOH等制备NaClO2的工艺装置如图: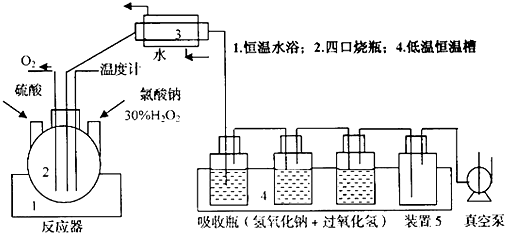
(1)反应器发生的化学反应方程式为___
(2)装置3的名称为___
A.离心机 B.冷凝器 C.安全器 D.电热器
(3)吸收瓶中发生的化学方程式为:___,为什么恒温槽要选择低温:___,还可以选择什么条件促进吸收:___
(4)装置5的作用是:___
(5)工业上可用如下方法对NaClO2纯度进行测定:
a称量约mg亚氯酸钠,配成500.00mL溶液
b.量取25.00mL试液,置于预先加有碘化钾溶液的碘量瓶中,并加入人适量稀硫酸溶液,摇匀,并于暗处放置10min
c.加100mL水,加人淀粉指示液,用浓度为c mol/L硫代硫酸钠标准溶液滴定至溶液蓝色消失即为终点,记下消耗的硫代硫酸钠标准溶液的体积为v mL,同时做空白试验,记下消耗的硫代硫酸钠标准溶液的体积为V0mL.滴定发生的方程式:2Na2S2O3+I2=2NaI+Na2S4O6 4I-+ClO2-+4H+=2I2+Cl-+3H2O
利用上述数据写出NaClO2质量分数的计算式(不用化简)___
(6)工业上可用RS(kesting法,原理为:2NaClO3+4HCl=2ClO2+Cl2↑+2NaCl+2H2O)制ClO2,相比R5法,过氧化氢法有什么优点___.

(1)反应器发生的化学反应方程式为___
(2)装置3的名称为___
A.离心机 B.冷凝器 C.安全器 D.电热器
(3)吸收瓶中发生的化学方程式为:___,为什么恒温槽要选择低温:___,还可以选择什么条件促进吸收:___
(4)装置5的作用是:___
(5)工业上可用如下方法对NaClO2纯度进行测定:
a称量约mg亚氯酸钠,配成500.00mL溶液
b.量取25.00mL试液,置于预先加有碘化钾溶液的碘量瓶中,并加入人适量稀硫酸溶液,摇匀,并于暗处放置10min
c.加100mL水,加人淀粉指示液,用浓度为c mol/L硫代硫酸钠标准溶液滴定至溶液蓝色消失即为终点,记下消耗的硫代硫酸钠标准溶液的体积为v mL,同时做空白试验,记下消耗的硫代硫酸钠标准溶液的体积为V0mL.滴定发生的方程式:2Na2S2O3+I2=2NaI+Na2S4O6 4I-+ClO2-+4H+=2I2+Cl-+3H2O
利用上述数据写出NaClO2质量分数的计算式(不用化简)___
(6)工业上可用RS(kesting法,原理为:2NaClO3+4HCl=2ClO2+Cl2↑+2NaCl+2H2O)制ClO2,相比R5法,过氧化氢法有什么优点___.
▼优质解答
答案和解析
(1)根据工艺装置图中物质的信息可知,反应物为H2O2、H2SO4和NaClO3,生成物为ClO2,氯的化合价降低,过氧化氢中-1价的氧化合价升高,所以产物中有氧气,根据得失电子守恒和原子守恒,反应方程式为:2NaClO3+H2O2+H2SO4=2ClO2+O2↑+Na2SO4+2H2O,
故答案为:2NaClO3+H2O2+H2SO4=2ClO2+O2↑+Na2SO4+2H2O;
(2)装置3从下向上进水,ClO2易溶于水,熔点为-59.5℃,沸点为11℃,所以装置3为冷凝装置,
故答案为:B;
(3)吸收瓶中二氧化氯和过氧化氢在碱性条件下反应:2ClO2+H2O2+2NaOH=2NaClO2+2H2O+O2,温度过高,过氧化氢会分解,所以选择低温条件,也可选择增大反应物氢氧化钠的浓度促进吸收,
故答案为:2ClO2+H2O2+2NaOH=2NaClO2+2H2O+O2;温度过高,过氧化氢会分解;增大氢氧化钠的浓度;
(4)装置5处在吸收瓶和真空泵之间,起缓冲作用,防止吸收液直接进入真空泵,
故答案为:缓冲,防止吸收液直接进入真空泵;
(5)根据c步骤.滴定发生的方程式:2Na2S2O3+I2=2NaI+Na2S4O6,2Na2S2O3~I2反应生成的碘单质的物质的量为:n(I2)=
n(Na2S2O3)=
×C×(V-V0)×10-3mol/L,
由4I++ClO2-+4H+=2I2+Cl-+3H2O可知ClO2-~2I2,步骤a.称量约mg亚氯酸钠,配成500.00mL溶液,n(NaClO2)=
n(I2)=
×C×
×(V-V0)×10-3mol/L,
所以NaClO2的质量为:m(NaClO2)=nM=
×C×
×(V-V0)×10-3mol/L×90.5g/mol═
×C×
×(V-V0)×10-3×90.5g,所以NaClO2的质量分数为:
×100%,
故答案为:
×100%;
(6)制备NaClO2的工艺未使用易挥发的酸,没有易挥发的污染物,而用R5(kesting法,原理为:2NaClO3+4HCl=2ClO2+Cl2↑+2NaCl+2H2O)制ClO2,氯气、氯化氢有毒且易挥发,对环境污染大,所以相比R5法,过氧化氢对环境污染小,
故答案为:对环境污染小.
故答案为:2NaClO3+H2O2+H2SO4=2ClO2+O2↑+Na2SO4+2H2O;
(2)装置3从下向上进水,ClO2易溶于水,熔点为-59.5℃,沸点为11℃,所以装置3为冷凝装置,
故答案为:B;
(3)吸收瓶中二氧化氯和过氧化氢在碱性条件下反应:2ClO2+H2O2+2NaOH=2NaClO2+2H2O+O2,温度过高,过氧化氢会分解,所以选择低温条件,也可选择增大反应物氢氧化钠的浓度促进吸收,
故答案为:2ClO2+H2O2+2NaOH=2NaClO2+2H2O+O2;温度过高,过氧化氢会分解;增大氢氧化钠的浓度;
(4)装置5处在吸收瓶和真空泵之间,起缓冲作用,防止吸收液直接进入真空泵,
故答案为:缓冲,防止吸收液直接进入真空泵;
(5)根据c步骤.滴定发生的方程式:2Na2S2O3+I2=2NaI+Na2S4O6,2Na2S2O3~I2反应生成的碘单质的物质的量为:n(I2)=
| 1 |
| 2 |
| 1 |
| 2 |
由4I++ClO2-+4H+=2I2+Cl-+3H2O可知ClO2-~2I2,步骤a.称量约mg亚氯酸钠,配成500.00mL溶液,n(NaClO2)=
| 1 |
| 2 |
| 1 |
| 4 |
| 500 |
| 25 |
所以NaClO2的质量为:m(NaClO2)=nM=
| 1 |
| 4 |
| 500 |
| 25 |
| 1 |
| 4 |
| 500 |
| 25 |
(V-V0)×C×
| ||
m×
|
故答案为:
(V-V0)×C×
| ||
m×
|
(6)制备NaClO2的工艺未使用易挥发的酸,没有易挥发的污染物,而用R5(kesting法,原理为:2NaClO3+4HCl=2ClO2+Cl2↑+2NaCl+2H2O)制ClO2,氯气、氯化氢有毒且易挥发,对环境污染大,所以相比R5法,过氧化氢对环境污染小,
故答案为:对环境污染小.
看了稳定的ClO2易溶于水,熔点为...的网友还看了以下:
国务院关于特准经金瓶掣签认定的坚赞诺布继任为第十一世班禅额尔德尼的批复颁布单位:国务院颁布日期:1 2020-06-29 …
去年5月1日美国特种部队将基地恐怖组织头目本•拉登击毙。事后根据相关资料进行尸体认定,你认为下列方 2020-07-16 …
图5是“我国2006年以来人口数、人口自然增长率及出生人口性别比的变化曲线图”。出生性别比为每出生百 2020-11-02 …
国家出台促进中小企业发展的税收优惠政策有以下规定:(1)国家级高新技术开发区内的企业,经认定为高新技 2020-11-27 …
2010年12月9日,国务院决定修改工伤保险条例,扩大了工伤认定的范围。上下班途中非机动车及地铁事故 2020-11-28 …
求助,翻译成英语,谢谢!中译英:国家以自主研发和创新为核心来认定高新技术企业,对参加认定企业的经营业 2020-12-04 …
材料一2010年3月15日美国130位国会议员联名致信美国财政部长盖特纳和商务部长骆家辉,要求将中国 2020-12-06 …
(18分)叙利亚局势危机,牵动全球的神经材料一叙利亚爆发内战以来,多次发生化学武器袭击,危机不断升级 2020-12-28 …
爱国情感与爱国认识的关系是[]A.情感是在认识的基础上产生的B.认识越深厚,感情也越深厚C.认识浅薄 2020-12-29 …
2010年12月9日,国务院决定修改工伤保险条例,扩大了工伤认定的范围。上下班途中非机动车及地铁事故 2021-01-01 …