早教吧作业答案频道 -->化学-->
丙烷、乙烯等有机物在工业上有广泛的应用,回答下列问题:(1)已知下图1为各组物质能量总和及相互间转化的能量关系,写出丙烷气体(C3H8)分解得到石墨(C)和氢气的热化学方程式
题目详情
丙烷、乙烯等有机物在工业上有广泛的应用,回答下列问题:
(1)已知下图1为各组物质能量总和及相互间转化的能量关系,写出丙烷气体(C3H8)分解得到石墨(C)和氢气的热化学方程式___.
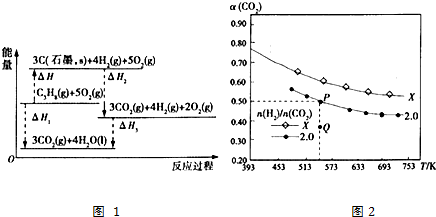
(2)在两个容积均为1L的密闭容器中以不同的氢碳比[
]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g)△H.CO2的平衡转化率α(CO2)与温度的关系如图2所示.
①此反应的平衡常数表达式K=___,P点对应温度下,K的值为___.
②该反应的△H___(填“>”“<”或“=”)0,判断的理由是___.
③氢碳比:X___(填“>”“<”或“=”)2.0.
④在氢碳比为2.0时,Q点v(逆)___(填“>”“<”或“=”)P点的v(逆).
(1)已知下图1为各组物质能量总和及相互间转化的能量关系,写出丙烷气体(C3H8)分解得到石墨(C)和氢气的热化学方程式___.

(2)在两个容积均为1L的密闭容器中以不同的氢碳比[
| n(H2) |
| n(CO2) |
①此反应的平衡常数表达式K=___,P点对应温度下,K的值为___.
②该反应的△H___(填“>”“<”或“=”)0,判断的理由是___.
③氢碳比:X___(填“>”“<”或“=”)2.0.
④在氢碳比为2.0时,Q点v(逆)___(填“>”“<”或“=”)P点的v(逆).
▼优质解答
答案和解析
(1)根据能量变化示意图可知,丙烷气体(C3H8)分解得到石墨(C)和氢气的热化学方程式为:C3H8(g)═3C(石墨,s)+4H2(g)△H=△H1-△H2-△H3,
故答案为:C3H8(g)═3C(石墨,s)+4H2(g)△H=△H1-△H2-△H3;
(2)①2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g),所以平衡常数K=
,
由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比
=2,设起始时氢气为2mol/L、二氧化碳为1mol/L,则二氧化碳浓度变化量为0.5mol/L,则:
2CO2(g)+6H2 (g)⇌C2H4(g)+4H2O(g)
起始浓度(mol/L):1 2 0 0
变化浓度(mol/L):0.5 1.5 0.25 1
平衡浓度(mol/L):0.5 0.5 0.25 1
代入平衡常数表达式K=
=
=64,
故答案为:
;64;
②由图可知,随温度升高CO2的平衡转化率减小,说明升高温度平衡逆向移动,升高温度平衡向吸热反应越大,则正反应为放热反应,故△H<0,
故答案为:<;温度升高CO2的平衡转化率减小,平衡逆向移动,故逆反应是吸热反应,正反应为放热反应;
③由图象可知X的碳氢比不等于2,在相同条件下反应达平衡时,二氧化碳的转化率增大了,说明是增大了氢气的量,提高二化碳的转化率,即碳氢比越大,二氧化碳转化率越大,
故答案为:>;
④在氢碳比为2.0时,P点达平衡,Q点未达平衡,此时二氧化碳的转化率比平衡时小,说明此时要继续转化更多的二氧化碳,反应物浓度在减小,生成物浓度在增大,正反应速率在减小,逆反应速率在增大,所以此时逆反应速率比平衡时逆反应速率小,
故答案为:<.
故答案为:C3H8(g)═3C(石墨,s)+4H2(g)△H=△H1-△H2-△H3;
(2)①2CO2(g)+6H2(g)⇌C2H4(g)+4H2O(g),所以平衡常数K=
| c(C2H4)•c4(H2O) |
| c2(CO2)•c6(H2) |
由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比
| n(H2) |
| n(CO2) |
2CO2(g)+6H2 (g)⇌C2H4(g)+4H2O(g)
起始浓度(mol/L):1 2 0 0
变化浓度(mol/L):0.5 1.5 0.25 1
平衡浓度(mol/L):0.5 0.5 0.25 1
代入平衡常数表达式K=
| c(C2H4)•c4(H2O) |
| c2(CO2)•c6(H2) |
| 0.25×14 |
| 0.52×0.56 |
故答案为:
| c(C2H4)•c4(H2O) |
| c2(CO2)•c6(H2) |
②由图可知,随温度升高CO2的平衡转化率减小,说明升高温度平衡逆向移动,升高温度平衡向吸热反应越大,则正反应为放热反应,故△H<0,
故答案为:<;温度升高CO2的平衡转化率减小,平衡逆向移动,故逆反应是吸热反应,正反应为放热反应;
③由图象可知X的碳氢比不等于2,在相同条件下反应达平衡时,二氧化碳的转化率增大了,说明是增大了氢气的量,提高二化碳的转化率,即碳氢比越大,二氧化碳转化率越大,
故答案为:>;
④在氢碳比为2.0时,P点达平衡,Q点未达平衡,此时二氧化碳的转化率比平衡时小,说明此时要继续转化更多的二氧化碳,反应物浓度在减小,生成物浓度在增大,正反应速率在减小,逆反应速率在增大,所以此时逆反应速率比平衡时逆反应速率小,
故答案为:<.
看了丙烷、乙烯等有机物在工业上有广...的网友还看了以下:
.下列说法错误的是A.书写热化学方程式时不但要注明反应物和生成物的状态,还需要注明反应环境的温度和 2020-04-08 …
完成下列实验所选择的装置或仪器正确的是()A.构成锌铜原电池B.测定酸碱中和反应中和热大小的量热计 2020-05-14 …
中和反应是典型的放热反应,酸与碱发生中和反应生成1mol水时所释放的热量称为中和热.下列关于中和热 2020-05-14 …
中和反应是典型的放热反应,酸与碱发生中和反应生成1mol水时所释放的热量称为中和热.下列关于中和热 2020-05-14 …
下列说法中正确的是()A.在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热 2020-05-14 …
下列说法正确的是()A.酸和碱发生中和反应生成水,这时的反应热叫中和热B.燃烧热或中和热是反应热的 2020-05-14 …
下列说法正确的是()A.在101kPa时,1mol物质完全燃烧时所放出的热量,叫该物质的燃烧热B. 2020-05-14 …
恒温,恒压下,已知反应A→2B的反应热为△H1和反应2A→C的反应热为△H2,则反应恒温、恒压下, 2020-06-14 …
下列反应中能产生SO2的是()①硫在空气中燃烧②亚硫酸钠和硫酸反应③碳和热的浓硫酸反应④铜和热的浓 2020-06-22 …
1.下列各组物质中,两种物质所含的化学键类型不同的是()AH2O和HNO3BNaCl和NH3CCaF 2021-02-16 …