早教吧作业答案频道 -->化学-->
氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.完成下列填空:(1)实验室配制氯化铝溶液时加入盐酸的目的是.(2)向A1C13溶液中通入过量气体或加入过量溶液,最终
题目详情
氯化铝可制备无机高分子混凝剂,在有机合成中有广泛的用途.完成下列填空:
(1)实验室配制氯化铝溶液时加入盐酸的目的是___.
(2)向A1C13溶液中通入过量气体或加入过量溶液,最终得到无色澄清溶液的是___(选填编号).
a.CO2 b.NaOH c.NaAlO2 d.Na2CO3
(3)用滴管向试管中滴加少重A1C13溶液时,滴管不得伸入试管中的理由是___.用试管夹夹持上述试管在酒精灯上加热时,不断上下移动试管的目的是___.
(4)另取适量A1C13溶液,用小火加热,使水蒸干,生成白色固体的组成可表示为:A1(OH)3Cl(6-n),为确定n的值,取3.490g白色固体,全部溶解在含有0.1120mol的HNO3的稀盐酸(足重)中,并加水稀释成100mL,将溶液分成两等份,进行如下实验:
①一份与足量氨水充分反应后过滤、洗涤、灼烧,最后得A12O3的质量为1.020g.判断加入氨水已足量的操作方法是___.过滤、洗涤后至少要灼烧___次(填写数字);测定样品中铝元素含量时不选择测定干燥A1 (OH) 3的质量,而是测定A12O3的质量的原因可能是___ (填编号).
a.A12O3的质量比A1(OH)3大,误差小
b.沉淀A1(OH)3时不完全
c.灼烧氧化铝时不分解
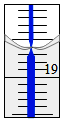
②从另一份溶液中取出20.00mL,用0.1290mol/L的标准NaOH溶液滴定过量的硝酸,滴定前滴定管读数为0.00mL,终点时滴定管液面(局部)如图所示,则滴定管的读数为___mL.
③根据实验数据计算n值的方法有多种,确定Al2 (OH) nCl( e-n)中n的值为___.

(1)实验室配制氯化铝溶液时加入盐酸的目的是___.
(2)向A1C13溶液中通入过量气体或加入过量溶液,最终得到无色澄清溶液的是___(选填编号).
a.CO2 b.NaOH c.NaAlO2 d.Na2CO3
(3)用滴管向试管中滴加少重A1C13溶液时,滴管不得伸入试管中的理由是___.用试管夹夹持上述试管在酒精灯上加热时,不断上下移动试管的目的是___.
(4)另取适量A1C13溶液,用小火加热,使水蒸干,生成白色固体的组成可表示为:A1(OH)3Cl(6-n),为确定n的值,取3.490g白色固体,全部溶解在含有0.1120mol的HNO3的稀盐酸(足重)中,并加水稀释成100mL,将溶液分成两等份,进行如下实验:
①一份与足量氨水充分反应后过滤、洗涤、灼烧,最后得A12O3的质量为1.020g.判断加入氨水已足量的操作方法是___.过滤、洗涤后至少要灼烧___次(填写数字);测定样品中铝元素含量时不选择测定干燥A1 (OH) 3的质量,而是测定A12O3的质量的原因可能是___ (填编号).
a.A12O3的质量比A1(OH)3大,误差小
b.沉淀A1(OH)3时不完全
c.灼烧氧化铝时不分解
②从另一份溶液中取出20.00mL,用0.1290mol/L的标准NaOH溶液滴定过量的硝酸,滴定前滴定管读数为0.00mL,终点时滴定管液面(局部)如图所示,则滴定管的读数为___mL.
③根据实验数据计算n值的方法有多种,确定Al2 (OH) nCl( e-n)中n的值为___.
▼优质解答
答案和解析
(1)氯化铝电离出的Al3+易水解,水解生成H+,水解的离子方程式为:Al3++3H2O⇌Al(OH)3+3H+,加入盐酸能抑制其水解,
故答案为:抑制氯化铝(或Al3+)水解;
(2)a.AlCl3和CO2 不反应,故溶液仍为澄清,故a正确;
b.AlCl3和过量的氢氧化钠反应生成NaAlO2溶液:AlCl3+4NaOH=3NaCl+NaAlO2+2H2O,得澄清溶液,故b正确;
c.AlCl3和NaAlO2发生双水 AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl,得不到澄清溶液,故c错误;
d.AlCl3和Na2CO3发生双水 2AlCl3+3Na2CO3+3H2O=2Al(OH)3↓+3CO2↑,得不到澄清溶液,故d错误;
故答案为:ab;
(3)向试管中滴加溶液时应“垂直、悬空”,目的是防止污染试剂;用试管夹夹持上述试管在酒精灯上加热时,要上下移动试管防止局部暴沸,
故答案为:防止试剂被污染;防止局部受热引起暴沸;
(4)①判断试剂已过量的方法是继续滴加,即当氨水加入过量时,去上层清液继续滴加氨水,则无沉淀生成;将所得的Al(OH)3沉淀至少灼烧2-3次,至两次质量差不超过0.1g即说明Al(OH)3分解完全得Al2O3,不选择测定干燥Al(OH)3的质量,而是测定Al2O3的质量的原因是干燥Al(OH)3时易分解失水而灼烧Al2O3不失水,所以c符合;
故答案为:静置,向上层淸液中继续滴加氨水,无沉淀生成;2;c;
②滴定管的0刻度在上,故滴定管的读数为18.60mL,则消耗的氢氧化钠的体积为18.60mL,
故答案为:18.60;
③根据0.1120mol HNO3的消耗有两个原因:被3.490gAl2(OH)nCl(6-n)中OH-消耗的和被0.1290mol/L的标准NaOH溶液消耗,可有:0.112mol=
×n+0.129mol/L×0.0186L×5,解得n=5,
故答案为:5.
故答案为:抑制氯化铝(或Al3+)水解;
(2)a.AlCl3和CO2 不反应,故溶液仍为澄清,故a正确;
b.AlCl3和过量的氢氧化钠反应生成NaAlO2溶液:AlCl3+4NaOH=3NaCl+NaAlO2+2H2O,得澄清溶液,故b正确;
c.AlCl3和NaAlO2发生双水 AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl,得不到澄清溶液,故c错误;
d.AlCl3和Na2CO3发生双水 2AlCl3+3Na2CO3+3H2O=2Al(OH)3↓+3CO2↑,得不到澄清溶液,故d错误;
故答案为:ab;
(3)向试管中滴加溶液时应“垂直、悬空”,目的是防止污染试剂;用试管夹夹持上述试管在酒精灯上加热时,要上下移动试管防止局部暴沸,
故答案为:防止试剂被污染;防止局部受热引起暴沸;
(4)①判断试剂已过量的方法是继续滴加,即当氨水加入过量时,去上层清液继续滴加氨水,则无沉淀生成;将所得的Al(OH)3沉淀至少灼烧2-3次,至两次质量差不超过0.1g即说明Al(OH)3分解完全得Al2O3,不选择测定干燥Al(OH)3的质量,而是测定Al2O3的质量的原因是干燥Al(OH)3时易分解失水而灼烧Al2O3不失水,所以c符合;
故答案为:静置,向上层淸液中继续滴加氨水,无沉淀生成;2;c;
②滴定管的0刻度在上,故滴定管的读数为18.60mL,则消耗的氢氧化钠的体积为18.60mL,
故答案为:18.60;
③根据0.1120mol HNO3的消耗有两个原因:被3.490gAl2(OH)nCl(6-n)中OH-消耗的和被0.1290mol/L的标准NaOH溶液消耗,可有:0.112mol=
| 3.490g |
| (267-18.5n)g/mol |
故答案为:5.
看了氯化铝可制备无机高分子混凝剂,...的网友还看了以下:
溶液凝固过程系统的水溶液随着温度不断降低,并不断析出,因此溶液的浓度会不断上升.这句话对不对?还有 2020-05-22 …
DIC的血液凝固障碍表现为A:血液凝固性升高B:纤溶活性增高C:高凝和低凝同时发生D:先高凝后转为 2020-06-07 …
酸和碱在生产和生活中有广泛的用途.酸和碱都能与酸碱指示剂反应.指示剂遇酸或碱的溶液显示不同的颜色. 2020-06-26 …
溶液凝固的过程是怎样的?初步备选模型:a,溶剂凝固,溶质继续保持在未凝固的溶剂中直到饱和;b,溶剂 2020-06-30 …
血液中的钙离子在血液凝固过程中起重要作用,缺乏则血液不能凝固,草酸钾溶液能与血液中的钙离子发生反应 2020-07-03 …
在实验中手不慎被玻璃割破,可用FeCl3溶液应急止血,其主要原因可能是A.FeCl3溶液具有杀菌消 2020-07-12 …
硝基苯和苯可无限混溶,二者凝固点分别为5.7度,5.5度,凝固点降低指数为8.1,5.12.二者按 2020-07-16 …
(2014•工业园区一模)下列有关溶液的叙述不正确的是()A.同种溶质的饱和溶液一定比不饱和溶液的 2020-08-02 …
血液中的钙离子在血液凝固过程中起着重要作用,钙离子缺乏则血液不能凝固。草酸钾溶液能与血液中的钙离子发 2020-11-11 …
阿司匹林清除血渍的原理血液凝固的关键过程是血浆中的纤维蛋白原转变为不溶的纤维蛋白。多聚体纤维蛋白交织 2020-12-24 …