早教吧作业答案频道 -->化学-->
X、Y、Z、W、G是元素周期表中原子序数依次增大的五种元素.X元素是元素周期表中核电荷数最小的元素.Y的一种核素常用于考古,某一种同素异形体为自然界最硬的物质.ZX3气体溶于水呈碱
题目详情
X、Y、Z、W、G是元素周期表中原子序数依次增大的五种元素.X元素是元素周期表中核电荷数最小的元素.Y的一种核素常用于考古,某一种同素异形体为自然界最硬的物质.ZX3气体溶于水呈碱性.W的外围电子排布是3s1.G2+离子的M层d轨道只有5个电子.请回答下列问题:
(1)W在元素周期表中的位置是___;W和Z形成的化合物水溶液呈碱性,用离子方程式表示其原因___.
(2)Z原子的第一电离能比氧原子的___(填“大”或“小”);G的基态原子电子排布式是___.
(3)X与Y可形成多种化合物,其中一种化合物的分子式是X6Y6,分子中只有σ键,该分子的结构简式是___;该化合物中Y的杂化轨道类型是___.
(4)G的最高价氧化物对应水化物的钾盐,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是___.
(5)可用YX4还原ZOx以消除污染.已知:
YX4(g)+4ZO2(g)═4ZO(g)+YO2(g)+2X2O(g)△H=-574kJ•mol-1
YX4(g)+4ZO(g)═2Z2(g)十YO2(g)+2X2O(g)△H=-1160kJ•mol-1
试写出用YX4还原ZO2至Z2的热化学方程式:___.
(1)W在元素周期表中的位置是___;W和Z形成的化合物水溶液呈碱性,用离子方程式表示其原因___.
(2)Z原子的第一电离能比氧原子的___(填“大”或“小”);G的基态原子电子排布式是___.
(3)X与Y可形成多种化合物,其中一种化合物的分子式是X6Y6,分子中只有σ键,该分子的结构简式是___;该化合物中Y的杂化轨道类型是___.
(4)G的最高价氧化物对应水化物的钾盐,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是___.
(5)可用YX4还原ZOx以消除污染.已知:
YX4(g)+4ZO2(g)═4ZO(g)+YO2(g)+2X2O(g)△H=-574kJ•mol-1
YX4(g)+4ZO(g)═2Z2(g)十YO2(g)+2X2O(g)△H=-1160kJ•mol-1
试写出用YX4还原ZO2至Z2的热化学方程式:___.
▼优质解答
答案和解析
X、Y、Z、W、G是元素周期表中原子序数依次增大的五种元素,X是元素周期表中核电荷数最小的元素,故X为H元素;Y的一种核素常用于考古,其一种同素异形体为自然界最硬的物质,则Y为C元素;ZX3气体溶于水呈碱性,则Z为N元素;W的外围电子排布是3s1,则W为Na;G2+离子的M层d轨道只有5个电子,原子核外电子排布式为1s22s22p63s23p63d54s2,则G为Mn.
(1)W是Na元素,位于元素周期表第三周期第IA族;W和Z形成的化合物为Na3N,水溶液呈碱性,用离子方程式表示其原因:N3-+H2O⇌NH3+OH-;
故答案为:第三周期第IA族;N3-+H2O⇌NH3+OH-;
(2)N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能大于氧原子;G为Mn元素,基态原子价电子排布式是1s22s22p63s23p63d54s2,
故答案为:大;1s22s22p63s23p63d54s2;
(3)H与C可形成多种化合物,其中一种化合物的分子式是H6C6,分子中只有σ键,该分子的结构简式是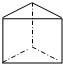 ,碳原子形成4个σ键,没有孤对电子,碳原子杂化方式为sp3杂化,
,碳原子形成4个σ键,没有孤对电子,碳原子杂化方式为sp3杂化,
故答案为: ;sp3;
;sp3;
(4)G的最高价氧化物对应水化物的钾盐为KMnO4,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
(5)已知:①CH4 (g)+4NO2 (g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g)△H=-1160kJ•mol-1
根据盖斯定律①+②得:2CH4 (g)+4NO2 (g)=2CO2(g)+2N2 (g)+4H2O(g)△H=-1734kJ•mol-1,
即热化学方程式为CH4 (g)+2NO2 (g)=CO2(g)+N2 (g)+2H2O(g)△H=-867kJ•mol-1,
故答案为:CH4 (g)+2NO2 (g)=CO2(g)+N2 (g)+2H2O(g)△H=-867kJ•mol-1.
(1)W是Na元素,位于元素周期表第三周期第IA族;W和Z形成的化合物为Na3N,水溶液呈碱性,用离子方程式表示其原因:N3-+H2O⇌NH3+OH-;
故答案为:第三周期第IA族;N3-+H2O⇌NH3+OH-;
(2)N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能大于氧原子;G为Mn元素,基态原子价电子排布式是1s22s22p63s23p63d54s2,
故答案为:大;1s22s22p63s23p63d54s2;
(3)H与C可形成多种化合物,其中一种化合物的分子式是H6C6,分子中只有σ键,该分子的结构简式是
 ,碳原子形成4个σ键,没有孤对电子,碳原子杂化方式为sp3杂化,
,碳原子形成4个σ键,没有孤对电子,碳原子杂化方式为sp3杂化,故答案为:
 ;sp3;
;sp3;(4)G的最高价氧化物对应水化物的钾盐为KMnO4,在酸性条件下,常用于测定溶液中Fe2+的含量,该反应的离子方程式是:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O,
故答案为:MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O;
(5)已知:①CH4 (g)+4NO2 (g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4 (g)+4NO(g)=2N2 (g)+CO2 (g)+2H2O(g)△H=-1160kJ•mol-1
根据盖斯定律①+②得:2CH4 (g)+4NO2 (g)=2CO2(g)+2N2 (g)+4H2O(g)△H=-1734kJ•mol-1,
即热化学方程式为CH4 (g)+2NO2 (g)=CO2(g)+N2 (g)+2H2O(g)△H=-867kJ•mol-1,
故答案为:CH4 (g)+2NO2 (g)=CO2(g)+N2 (g)+2H2O(g)△H=-867kJ•mol-1.
看了X、Y、Z、W、G是元素周期表...的网友还看了以下:
进入12月份以来,嘉兴市几次出现了大雾天气.由于大雾天气能见度较低,给市民出行带来很大不便进入12 2020-05-17 …
天然气灶烧水,燃烧0.5立方米的天然气,是10万克的水,从20摄氏度升高到70摄氏度,已知水的比热 2020-07-10 …
氯气常用于生活用水的杀菌,其原因是()A.氯气有毒B.氯气有刺激性气味C.氯气溶于水,与水反应可生 2020-07-26 …
根据你具有的生物学知识素养判断下列说法,正确的是()A.解剖家鸽发现,家鸽的食道位于胸腔,而胃、肠 2020-07-29 …
地球大气的演化经历了原始大气、次生大气和现在大气.(1)现在大气的成分是在千万年前固定下来的,主要成 2020-11-04 …
换煤气的时候会中毒吗?今天第一次换煤气,由于是第一次,就有点凑近着换的,当转开是有些气体溢出,但是这 2020-11-28 …
以下关于动物的说法错误的是()A.蜗牛身体柔软,具有贝壳,属于软体动物B.麻雀每呼吸一次,要在肺和气 2020-12-07 …
氯气(Cl2)是黄绿色气体,氯气溶于水部分以Cl2分子存在于溶液中,部分与水反应Cl2+H2O=HC 2020-12-07 …
目前南昌市有很多家庭已用上了天然气.天然气与煤气相比,其优点之一是天然气的热值(选填“较大”或“较小 2021-01-02 …
关于动物的叙述,正确的是()A.章鱼、鱿鱼都属于鱼类,它们鳃内含有丰富的毛细血管,有利于在水中呼吸B 2021-01-07 …