早教吧作业答案频道 -->化学-->
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等.①基态Fe3+的M层电子排布式为.②尿素(H2NCONH2)分子中C、N原子的杂化方式分
题目详情
(1)过渡金属元素铁能形成多种配合物,如:[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]和Fe(CO)x等.
①基态Fe3+的M层电子排布式为___.
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是___、___;C、N、O 三种元素的第一电离能由大到小的顺序为___
③Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于___(填晶体类型)
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图1,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为___.已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a=___cm. (用含ρ、NA的计算式表示)
(3)下列说法正确的是___
A.因为晶格能CaO比KCl高,所以KCl比CaO熔点低
B.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
C.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(4)图2是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体.
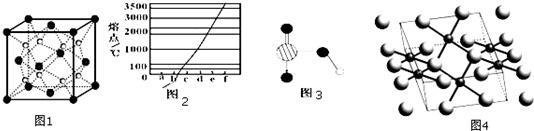
①图中d单质的晶体堆积方式类型是___.
②单质a、b、f 对应的元素以原子个数比1:1:1形成的分子中含___个σ键,___个π键.
③图3是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:___.
(5)如图4是某金属氧化物的晶体结构示意图.图中,小球代表金属原子,大球代表氧原子,细线框出其晶胞,则金属原子的配位数___.该金属氧化物的化学式为___(金属用M表示)
①基态Fe3+的M层电子排布式为___.
②尿素(H2NCONH2)分子中C、N原子的杂化方式分别是___、___;C、N、O 三种元素的第一电离能由大到小的顺序为___
③Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于___(填晶体类型)
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图1,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为___.已知该晶胞的密度为ρ g/cm3,阿伏加德罗常数为NA,求晶胞边长a=___cm. (用含ρ、NA的计算式表示)
(3)下列说法正确的是___
A.因为晶格能CaO比KCl高,所以KCl比CaO熔点低
B.SO2与CO2的化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大
C.分子晶体中,共价键键能越大,该分子晶体的熔沸点越高
(4)图2是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体.

①图中d单质的晶体堆积方式类型是___.
②单质a、b、f 对应的元素以原子个数比1:1:1形成的分子中含___个σ键,___个π键.
③图3是上述六种元素中的一种元素形成的含氧酸的结构,请简要说明该物质易溶于水的原因:___.
(5)如图4是某金属氧化物的晶体结构示意图.图中,小球代表金属原子,大球代表氧原子,细线框出其晶胞,则金属原子的配位数___.该金属氧化物的化学式为___(金属用M表示)
▼优质解答
答案和解析
(1)①Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5,则M层电子排布式为:3s23p63d5,
故答案为:3s23p63d5;
②尿素(H2NCONH2)分子中C原子含有3个σ键且不含孤电子对,所以其杂化方式为sp2,N原子分别含有3个,σ键且含有一个孤电子对,所以N原子采用sp3杂化,;
同周期从左到右第一电离能增大,但是第IIA与IIIA、第VA与VIA族反常,则C、N、O 三种元素的第一电离能由大到小的顺序为N>O>C;
故答案为:sp2;sp3;N>O>C;
③,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,
故答案为:分子晶体;
(2)由Na2O晶胞结构结构可知,晶胞中黑色球数目=8×
+6×
=4,白色球数目=8,故白色球为Na+离子、黑色球为O2-,以晶胞中上面心O2-离子为研究对象,距一个O2-周围最近的Na+离子有8个,位于晶胞中上层4个Na+及上面晶胞中的下层4个Na+,8个Na+离子构成的几何体中每个都是正方形,形成立方体结构;
该晶胞质量=4×
g,该晶胞的密度为ρ g•cm-3,则晶胞边长a=
=
cm,
故答案为:立方体;
;
(3)A.离子晶体的晶格能与电荷成正比、与离子半径成反比,钙离子电荷大于钾离子、钙离子半径小于钾离子,O离子电荷大于Cl离子、氧离子半径小于氯离子,KCl比CaO晶格能小,KCl比CaO熔点低,故正确;
B.SO2是V型结构、CO2分子结构呈直线型,故错误;
C.分子晶体中,分子晶体的熔.沸点越高与其相对分子质量成正比,与化学键大小无关,故错误;
故选A.
(4)①d单质是热和电的良导体,且熔点较高,则为铜,铜为面心立方最密堆积,故答案为:面心立方最密堆积;
②根据熔点知,a是H元素,b是N元素,f是C元素,a、b、f 对应的元素以原子个数比1:1:1形成的分子为HCN,其结构为H-C≡N,共价单键为σ键,共价双键中一个是σ键一个是π键,三键中一个是σ键两个是π键,所以该分子中含有2个σ键2个π键,
故答案为:2;2;
③根据图知,该分子中含有一个氢原子、三个氧原子和一个氮原子,为硝酸分子,硝酸分子正负电荷重心不重合,为极性分子,且硝酸和水能形成氢键而增大硝酸的溶解性,
故答案为:硝酸分子是极性分子,易溶于极性溶剂的水中,硝酸分子中氢氧键易与水分子间形成氢键.
(5))由晶胞结构可知,每个金属原子周围有4个O原子,金属原子的配位数为4;
从图中看出金属原子在面心上有4个原子,体心有2个原子,故晶胞中金属原子数=4×
+2=4,氧原子在棱上有8个原子,体心2个,故晶胞中氧原子数=8×
+2=4,则化学式为MO.
故答案为:4;MO.
故答案为:3s23p63d5;
②尿素(H2NCONH2)分子中C原子含有3个σ键且不含孤电子对,所以其杂化方式为sp2,N原子分别含有3个,σ键且含有一个孤电子对,所以N原子采用sp3杂化,;
同周期从左到右第一电离能增大,但是第IIA与IIIA、第VA与VIA族反常,则C、N、O 三种元素的第一电离能由大到小的顺序为N>O>C;
故答案为:sp2;sp3;N>O>C;
③,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,
故答案为:分子晶体;
(2)由Na2O晶胞结构结构可知,晶胞中黑色球数目=8×
| 1 |
| 8 |
| 1 |
| 2 |
该晶胞质量=4×
| 62 |
| NA |
| 3 |
| ||||
| 3 |
| ||
故答案为:立方体;
| 3 |
| ||
(3)A.离子晶体的晶格能与电荷成正比、与离子半径成反比,钙离子电荷大于钾离子、钙离子半径小于钾离子,O离子电荷大于Cl离子、氧离子半径小于氯离子,KCl比CaO晶格能小,KCl比CaO熔点低,故正确;
B.SO2是V型结构、CO2分子结构呈直线型,故错误;
C.分子晶体中,分子晶体的熔.沸点越高与其相对分子质量成正比,与化学键大小无关,故错误;
故选A.
(4)①d单质是热和电的良导体,且熔点较高,则为铜,铜为面心立方最密堆积,故答案为:面心立方最密堆积;
②根据熔点知,a是H元素,b是N元素,f是C元素,a、b、f 对应的元素以原子个数比1:1:1形成的分子为HCN,其结构为H-C≡N,共价单键为σ键,共价双键中一个是σ键一个是π键,三键中一个是σ键两个是π键,所以该分子中含有2个σ键2个π键,
故答案为:2;2;
③根据图知,该分子中含有一个氢原子、三个氧原子和一个氮原子,为硝酸分子,硝酸分子正负电荷重心不重合,为极性分子,且硝酸和水能形成氢键而增大硝酸的溶解性,
故答案为:硝酸分子是极性分子,易溶于极性溶剂的水中,硝酸分子中氢氧键易与水分子间形成氢键.
(5))由晶胞结构可知,每个金属原子周围有4个O原子,金属原子的配位数为4;
从图中看出金属原子在面心上有4个原子,体心有2个原子,故晶胞中金属原子数=4×
| 1 |
| 2 |
| 1 |
| 4 |
故答案为:4;MO.
看了 (1)过渡金属元素铁能形成多...的网友还看了以下:
有这样一道数学题;90%^90%^90%^90%^90%=59%.一项工作做到90%已经很不错了但 2020-04-27 …
有这样一道数学题;90%^90%^90%^90%^90%=59%.一项工作做到90%已经很不错了但 2020-04-27 …
把下列各数填入对应的集合中,|-6|,0.3无限不循环小数,0,负五又六分之一,-12,八分之三, 2020-05-13 …
甲数是乙数的5分之4,甲数比乙数少百分之【 】,乙数比甲数多百分之【 】甲数比乙数少5分之1,即甲 2020-05-16 …
基因与脱氧核苷酸的关系稍微具体一点儿~我知道脱氧核苷酸是由碱基、磷酸和脱氧核糖组成的,那基因呢?没 2020-05-17 …
具有独立遗传的两对相对性状的纯种杂交(AABB×aabb)F1自交的F2F2中新组成的的重组类型占 2020-05-17 …
5比80少百分之几,35是70的百分之几,24比48少百分之几,50比20多百分之几,110比11 2020-06-13 …
如图是人的排尿反射的反射弧结构简图(-•-<表示从树突到胞体到轴突),方框甲代表大脑皮层的部分区域 2020-06-19 …
CO和CO2的混合气体36g,完全燃烧后测得CO2的体积为22.4L(标准状况下).(1)求混合气 2020-06-27 …
把下面的分数化成小数。不能化成有限小数的,保留两位小数。3分之25分之一20分之1把下面的分数化成 2020-06-27 …