早教吧作业答案频道 -->化学-->
(1)下列反应中,属于吸热反应的是.①物质燃烧②炸药爆炸③酸碱中和反应④二氧化碳通过炽热的碳⑤Ba(OH)2•8H2O与NH4Cl反应⑥铁粉与稀盐酸反应⑦煅烧石灰石(主要成分
题目详情
(1)下列反应中,属于吸热反应的是___.
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥铁粉与稀盐酸反应 ⑦煅烧石灰石(主要成分是CaCO3)制生石灰(CaO) ⑧生石灰与水作用制熟石灰 ⑨食物因氧化而腐败.
(2)已知反应:
①N2(g)+O2(g)═2NO(g)△H1 ②2H2(g)+O2(g)═2H2O(g)△H2
③N2(g)+3H2(g)═2NH3(g)△H3 利用上述三个反应,计算4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H4的反应焓变为___ (用含△H1、△H2、△H3的式子表示).
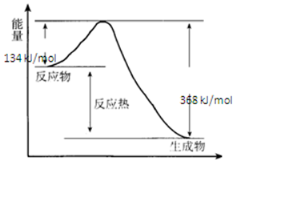
(3)在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.
①该反应是___ (填“吸热”或“放热”)反应.
②该反应的热化学方程式为___.
③改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是___.
a.浓度b.压强c.温度d.催化剂
④反应体系中加入催化剂对反应热是否有影响?___ (填“是”或“否”),原因是___.
①物质燃烧 ②炸药爆炸 ③酸碱中和反应 ④二氧化碳通过炽热的碳 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥铁粉与稀盐酸反应 ⑦煅烧石灰石(主要成分是CaCO3)制生石灰(CaO) ⑧生石灰与水作用制熟石灰 ⑨食物因氧化而腐败.
(2)已知反应:
①N2(g)+O2(g)═2NO(g)△H1 ②2H2(g)+O2(g)═2H2O(g)△H2
③N2(g)+3H2(g)═2NH3(g)△H3 利用上述三个反应,计算4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H4的反应焓变为___ (用含△H1、△H2、△H3的式子表示).
(3)在400℃、101kPa时,NO2(g)+CO(g)=NO(g)+CO2(g)反应过程的能量变化如图所示.
①该反应是___ (填“吸热”或“放热”)反应.
②该反应的热化学方程式为___.
③改变下列条件都可使该反应的反应速率改变,其中通过降低活化能加快反应速率的是___.
a.浓度b.压强c.温度d.催化剂
④反应体系中加入催化剂对反应热是否有影响?___ (填“是”或“否”),原因是___.

▼优质解答
答案和解析
(1)①物质燃烧是放热反应; ②炸药爆炸是放热反应; ③酸碱中和反应是放热反应; ④二氧化碳通过炽热的碳是吸热反应; ⑤Ba(OH)2•8H2O与NH4Cl反应是吸热反应; ⑥铁粉与稀盐酸反应是放热反应; ⑦煅烧石灰石(主要成分是CaCO3)制生石灰(CaO)是吸热反应; ⑧生石灰与水作用制熟石灰是放热反应; ⑨食物因氧化而腐败是放热反应.故答案为:④⑤⑦;
(2)N2(g)+O2(g)═2NO(g)△H1
②2H2(g)+O2(g)═2H2O(g)△H2
③N2(g)+3H2(g)═2NH3(g)△H3
结合盖斯定律可知,①×2+②×3-③×2可得4NH3(g)+5O2(g)═4NO(g)+6H2O(g),
则△H4=2△H1+3△H2-2△H3,
故答案为:2△H1+3△H2-2△H3.
(3)①据图分析,反应物能量高于生成物,反应放热,故答案为:放热;
②△H=生成物与反应物能量差=134KJ/mol-368KJ/mol=-234KJ/mol,其热化学方程式为:NO2(g)+CO(g)
NO(g)+CO2(g)△H=-234 kJ•mol-1
故答案为:NO2(g)+CO(g)
NO(g)+CO2(g)△H=-234 kJ•mol-1;
③催化剂能降低反应的活化能,浓度、压强通过增大活化分子的浓度加快反应速率,温度是增大活化分子百分数增大反应速率,故选:d;
④应体系中加催化剂,对反应热没有影响,因为,催化剂只能改变化学反应的速率和途径,不能改变化学反应始态和终态的能量,因此对反应热没有影响,故答案为:否;催化剂只能改变化学反应的速率和途径,不能改变化学反应始态和终态的能量,因此对反应热没有影响.
(2)N2(g)+O2(g)═2NO(g)△H1
②2H2(g)+O2(g)═2H2O(g)△H2
③N2(g)+3H2(g)═2NH3(g)△H3
结合盖斯定律可知,①×2+②×3-③×2可得4NH3(g)+5O2(g)═4NO(g)+6H2O(g),
则△H4=2△H1+3△H2-2△H3,
故答案为:2△H1+3△H2-2△H3.
(3)①据图分析,反应物能量高于生成物,反应放热,故答案为:放热;
②△H=生成物与反应物能量差=134KJ/mol-368KJ/mol=-234KJ/mol,其热化学方程式为:NO2(g)+CO(g)
| ||
| 101kPa |
故答案为:NO2(g)+CO(g)
| ||
| 101kPa |
③催化剂能降低反应的活化能,浓度、压强通过增大活化分子的浓度加快反应速率,温度是增大活化分子百分数增大反应速率,故选:d;
④应体系中加催化剂,对反应热没有影响,因为,催化剂只能改变化学反应的速率和途径,不能改变化学反应始态和终态的能量,因此对反应热没有影响,故答案为:否;催化剂只能改变化学反应的速率和途径,不能改变化学反应始态和终态的能量,因此对反应热没有影响.
看了(1)下列反应中,属于吸热反应...的网友还看了以下:
离子方程式H++OH-═H2O所表示的反应是()A.所有酸和碱之间的中和反应B.所有强酸和强碱之间 2020-05-13 …
下列关于中和反应的说法中错误的是[]A.中和反应要放出热量B.中和反应一定有盐生成C.中和反应一定 2020-05-14 …
能用离子方程式:表示的化学反应是[]A.酸碱中和反应B.一元酸与一元碱的中和反应C.强酸与强碱的中 2020-05-14 …
下列反应属于氧化还原反应且焓变△H小于0的是()A.Ba(OH)2•8H2O和NH4Cl反应B.Z 2020-05-14 …
下列变化中,既属于氧化还原反应又属于吸热反应的是()A.铝和盐酸反应B.灼热的碳与二氧化碳反应C. 2020-05-14 …
离子方程式H++OH-═H2O所表示的反应是()A.所有酸和碱之间的中和反应B.所有强酸和强碱之间 2020-05-14 …
下列关于中和反应的说法中错误的是()A.中和反应要放出热量B.中和反应一定有盐生成C.中和反应一定 2020-05-14 …
有关中和反应的说法中,错误的是()A.中和反应一定是酸和碱的反应B.凡是生成盐和水的化学反应都是中 2020-05-14 …
离子方程式H++OH-=H2O所表示的反应是()。A.所有酸和碱之间的中和反应B.强酸溶液与强碱溶 2020-05-14 …
下列反应属于吸热反应的是()。A.铝粉和三氧化铁的反应B.氢氧化钠和稀硫酸的中和反应C.氯化铵和消石 2021-02-01 …