早教吧作业答案频道 -->化学-->
环己酮是一种重要的有机化工原料,主要用于制造己内酰胺和己二酸.+Na2Cr2O7+H2SO455℃~60℃+H2O实验室可用环己醇氧化制取环己酮(已知该反应为放热反
题目详情
环己酮是一种重要的有机化工原料,主要用于制造己内酰胺和己二酸.
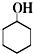 +Na2Cr2O7+H2SO4
+Na2Cr2O7+H2SO4
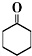 +H2O
+H2O
实验室可用环己醇氧化制取环己酮(已知该反应为放热反应):环己醇、环己酮和水的部分物理性质见下表:
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
实验步骤如下:
①将重铬酸钠溶于适量水,边搅拌边慢慢加入浓H2SO4,将所得溶液冷至室温备用.
②在一圆底烧瓶(乙)中加入适量环己醇,并将①中溶液分三次加入圆底烧瓶,每加一次都应振摇混匀.
控制瓶内温度在55℃~60℃之间,充分反应0.5h.
③向②反应后的圆底烧瓶内加入少量水,并接入图所示装置中,将T形管的活塞K打开,甲瓶中有适量水,加热甲,至有大量水蒸气冲出时,关闭K,同时接通冷凝水.
④将步骤③锥形瓶中收集到的液体经过以下一系列操作可得纯净的环己酮:a、蒸馏,除去乙醚后,收集151℃~155℃馏分;b、水层用乙醚(乙醚沸点34.6℃,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸)萃取,萃取液并入有机层;c、过滤;d、往液体中加入NaCl 固体至饱和,静置,分液; e、加入无水MgSO4固体.根据以上步骤回答下列问题:
(1)步骤①所得溶液分三次加入环己醇的原因是___.
(2)步骤③利用图示装置进行实验的目的是___,实验过程中要经常检查甲中玻管内的水位.若玻管内的水位升高过多,其可能原因是___,此时应立即采取的措施是___.
(3)步骤④中操作的正确顺序是___,上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需___,在上述操作d中加入NaCl 固体的作用是___,e中加入无水MgSO4的作用是___,蒸馏除乙醚的过程中采用的加热方式为___.
(4)写出该实验中可能发生的一个副反应的化学方程式___.
 +Na2Cr2O7+H2SO4
+Na2Cr2O7+H2SO4 | 55℃~60℃ |
| |
 +H2O
+H2O实验室可用环己醇氧化制取环己酮(已知该反应为放热反应):环己醇、环己酮和水的部分物理性质见下表:
| 物质 | 沸点(℃) | 密度(g•cm-3,20℃) | 溶解性 |
| 环己醇 | 161.1(97.8)* | 0.9624 | 能溶于水和醚 |
| 环己酮 | 155.6(95)* | 0.9478 | 微溶于水,能溶于醚 |
| 水 | 100.0 | 0.9982 |
实验步骤如下:

①将重铬酸钠溶于适量水,边搅拌边慢慢加入浓H2SO4,将所得溶液冷至室温备用.
②在一圆底烧瓶(乙)中加入适量环己醇,并将①中溶液分三次加入圆底烧瓶,每加一次都应振摇混匀.
控制瓶内温度在55℃~60℃之间,充分反应0.5h.
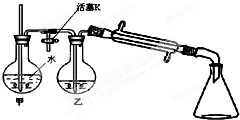
③向②反应后的圆底烧瓶内加入少量水,并接入图所示装置中,将T形管的活塞K打开,甲瓶中有适量水,加热甲,至有大量水蒸气冲出时,关闭K,同时接通冷凝水.
④将步骤③锥形瓶中收集到的液体经过以下一系列操作可得纯净的环己酮:a、蒸馏,除去乙醚后,收集151℃~155℃馏分;b、水层用乙醚(乙醚沸点34.6℃,易燃烧,当空气中含量为1.83~48.0%时易发生爆炸)萃取,萃取液并入有机层;c、过滤;d、往液体中加入NaCl 固体至饱和,静置,分液; e、加入无水MgSO4固体.根据以上步骤回答下列问题:
(1)步骤①所得溶液分三次加入环己醇的原因是___.
(2)步骤③利用图示装置进行实验的目的是___,实验过程中要经常检查甲中玻管内的水位.若玻管内的水位升高过多,其可能原因是___,此时应立即采取的措施是___.
(3)步骤④中操作的正确顺序是___,上述操作c、d中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需___,在上述操作d中加入NaCl 固体的作用是___,e中加入无水MgSO4的作用是___,蒸馏除乙醚的过程中采用的加热方式为___.
(4)写出该实验中可能发生的一个副反应的化学方程式___.
▼优质解答
答案和解析
(1)环己醇氧化为环己酮为放热反应,温度过高会引起副反应,故答案为:环己醇氧化为环己酮为放热反应,防止温度过高副反应增多;
(2)蒸馏出产品环已酮;玻管内的水位升高过多,说明压强过大,系统有堵塞现象,应让水蒸汽发生器和大气相通,故答案为:蒸馏出产品环已酮;系统有堵塞现象;打开止水夹K(让水蒸汽发生器和大气相通);
(3)环己酮的提纯时应首先加入NaCl固体,使水溶液的密度增大,水与有机物更容易分离开,然后向有机层中加入无水MgSO4,除去有机物中少量的水,然后过滤,除去硫酸镁晶体,再进行蒸馏即可,则操作为d b e c a;
分液需要的主要仪器为分液漏斗,过滤需要由漏斗组成的过滤器;联系制取肥皂的盐析原理,即增加水层的密度,有利于分层,环己酮的提纯时应首先加入NaCl固体,使水溶液的密度增大,将水与有机物更容易分离开来;乙醚沸点34.6℃,可用水浴加热,
故答案为:d b e c a;漏斗、分液漏斗;增加水层的密度,有利于分层;干燥剂;水浴加热;
(4)羟基能发生消去反应,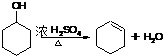 ,故答案为:
,故答案为: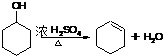 .
.
(2)蒸馏出产品环已酮;玻管内的水位升高过多,说明压强过大,系统有堵塞现象,应让水蒸汽发生器和大气相通,故答案为:蒸馏出产品环已酮;系统有堵塞现象;打开止水夹K(让水蒸汽发生器和大气相通);
(3)环己酮的提纯时应首先加入NaCl固体,使水溶液的密度增大,水与有机物更容易分离开,然后向有机层中加入无水MgSO4,除去有机物中少量的水,然后过滤,除去硫酸镁晶体,再进行蒸馏即可,则操作为d b e c a;
分液需要的主要仪器为分液漏斗,过滤需要由漏斗组成的过滤器;联系制取肥皂的盐析原理,即增加水层的密度,有利于分层,环己酮的提纯时应首先加入NaCl固体,使水溶液的密度增大,将水与有机物更容易分离开来;乙醚沸点34.6℃,可用水浴加热,
故答案为:d b e c a;漏斗、分液漏斗;增加水层的密度,有利于分层;干燥剂;水浴加热;
(4)羟基能发生消去反应,
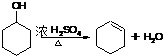 ,故答案为:
,故答案为: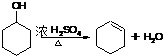 .
.
看了环己酮是一种重要的有机化工原料...的网友还看了以下:
有关于碳酸氢化物和碱的反应碳酸氢钙少量时和氢氧化钠反应生成碳酸钙碳酸钠和水而当碳酸氢钠和氢氧化钡反 2020-04-25 …
碳酸钡和硫酸能反应吗碳酸钙和硫酸不能反应 那碳酸钡和硫酸应该也一样啊生成硫酸钡难溶 覆盖在表面 阻 2020-05-16 …
急氧化钠和硫酸会直接反应吗?还是氧化钠和水先反应生成氢氧化钠,再和硫酸反应?我觉得,氧化钠不论是直 2020-05-16 …
这句话“盐是酸和碱中和反应的产物”对否?盐难道一定是酸碱中和反应的产物吗活泼金属和酸发生的置换反应 2020-07-09 …
碳酸氢钠与稀盐酸的反映是放热反应还是吸热反应在高中做实验时,做碳酸钠和稀盐酸与碳酸氢钠和稀盐酸反应的 2020-11-05 …
下列各组物质中,常温下能反应产生气体的是A.铁和浓硫酸B.铝和浓硫酸C.铜和浓盐酸D.铜和浓硝酸其它 2020-12-01 …
酸溶液与指示剂反应的规律是什么?金属和酸反应中,对金属和酸都有哪些要求?以铁与稀硫酸反应为例得出反应 2021-01-10 …
化学反应及基本反应类型.C+O2=CO2,属于反应稀硫酸和金属镁反应生成硫酸镁1和氢气.属于反应盐酸 2021-01-23 …
1.写出下列物质的化学式.氯酸钾氯化铵碳酸硫酸碳酸氢钠石灰石2.完成下列反应化学方程式.锌和稀硫酸反 2021-02-06 …
(2/2)盐酸反应,镁和稀盐酸反应,铝和稀盐酸反应,铁和硫酸铜溶液反应,铜和硝酸银反应 2021-02-18 …