早教吧作业答案频道 -->化学-->
NO2是形成雾霾天气的原因之一.(1)重型车辆常在排气管内喷淋尿素[CO(NH2)2]溶液,使NO2转化为无污染物质.采用“喷淋”的目的是,反应的活化能(选填“增大”“减小”“不变”
题目详情
NO2是形成雾霾天气的原因之一.
(1)重型车辆常在排气管内喷淋尿素[CO(NH2)2]溶液,使NO2转化为无污染物质.采用“喷淋”的目的是___,反应的活化能___(选填“增大”“减小”“不变”),配平该反应的化学方程式:___.【已知:CO(NH2)2中N呈-3价】
___NO2+___CO(NH2)2═___N2+___CO2+___H2O
(2)以CO2与NH3为原料可合成化肥尿素.已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-l59.5KJ•mol-1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(l)△H=-160.5KJ•mol-1
③H2O(l)═H2O(g)△H=+44.0KJ•mol-1
写出CO2与NH3合成尿素和气态水的热化学反应方程式___.
(3)恒温下将1.6molNH3和0.8molCO2放入容积为8L的恒容密闭容器中,反应生成NH2CO2NH4(s),下列各项能说明反应达到平衡状态的是___.
a.容器内气体压强保持不变 b.CO2与NH3的速率之比为1:2
c.NH2CO2NH4(s)质量保持不变 d.容器内温度保持不变
该反应达到平衡时,测得CO2的物质的量浓度为0.05mol•L-1.则平衡时CO2的转化率α=___;若其他条件不变,移去少量NH2CO2NH4,CO2的转化率___(选填“增大”“减小”“不变”).
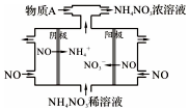
(4)为减少NO2排放,可将NO2转化为NO后通入如图所示装置,同时补充气体物质A使NO全部转化为NH4NO3,该装置中总化学反应方程式是___.

(1)重型车辆常在排气管内喷淋尿素[CO(NH2)2]溶液,使NO2转化为无污染物质.采用“喷淋”的目的是___,反应的活化能___(选填“增大”“减小”“不变”),配平该反应的化学方程式:___.【已知:CO(NH2)2中N呈-3价】
___NO2+___CO(NH2)2═___N2+___CO2+___H2O
(2)以CO2与NH3为原料可合成化肥尿素.已知:
①2NH3(g)+CO2(g)═NH2CO2NH4(s)△H=-l59.5KJ•mol-1
②NH2CO2NH4(s)═CO(NH2)2(s)+H2O(l)△H=-160.5KJ•mol-1
③H2O(l)═H2O(g)△H=+44.0KJ•mol-1
写出CO2与NH3合成尿素和气态水的热化学反应方程式___.
(3)恒温下将1.6molNH3和0.8molCO2放入容积为8L的恒容密闭容器中,反应生成NH2CO2NH4(s),下列各项能说明反应达到平衡状态的是___.
a.容器内气体压强保持不变 b.CO2与NH3的速率之比为1:2
c.NH2CO2NH4(s)质量保持不变 d.容器内温度保持不变
该反应达到平衡时,测得CO2的物质的量浓度为0.05mol•L-1.则平衡时CO2的转化率α=___;若其他条件不变,移去少量NH2CO2NH4,CO2的转化率___(选填“增大”“减小”“不变”).
(4)为减少NO2排放,可将NO2转化为NO后通入如图所示装置,同时补充气体物质A使NO全部转化为NH4NO3,该装置中总化学反应方程式是___.
▼优质解答
答案和解析
(1)尿素以喷淋的形式进入排气管,可增大与NO2气体的接触面积,加快了反应速率,但不改变反应的活化能;NO2中氮元素为+4价,转化为N2中0价,化合价降低4价,CO(NH2)2中氮元素-3价,转化为N2中0价,化合价降得6价,故最小公倍数为24,故NO2前系数为产6,CO(NH2)2前系数为产4,再结合原子守恒配平生成物;
故答案为:增大接触面积,加快反应速率;不变;6; 4;7; 4; 8;
(2)①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJ•mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)△H=-160.5kJ•mol-1
③H2O(l)=H2O(g)△H=+44.0kJ•mol-1
依据热化学方程式和盖斯定律计算①+②+③得到CO2与NH3合成尿素和气态水的热化学反应方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-276.0KJ/mol;
故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-276.0 KJ/mol;
(3)a.反应前后气体反应物和生成物的系数和不等,正反应是体积减小的方向,在恒温恒容条件下,压强不变是平衡状态,故a正确;b.伴随反应的进行,CO2与NH3的速率之比始终为1:2,无法判断是平衡状态,故b错误;c.NH2CO2NH4(s)质量保持不变可说明是平衡状态,故c正确;d.反应在恒温条件下进行,无法判断是平衡状态,故d错误;
2NH3+CO2⇌NH2CO2NH4,
起始量(mol/L) 0.2 0.1 0
变化量(mol/L) 0.1 0.05 0
平衡量(mol/L) 0.1 0.05 0
CO2的转化率=
×100%=
=50%
改变NH2CO2NH4(s)质量平衡不移动,CO2的转化率不变;
故答案为:ac;50%;不变;
(4)电解NO制备NH4NO3,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总电极反应方程式为:8NO+7H2
3NH4NO3+2HNO3可知补充的A为NH3,使NO全部转化为NH4NO3总化学反应方程式是8NO+2NH3+7H2O=5NH4NO3;
故答案为:8NO+2NH3+7H2O=5NH4NO3.
故答案为:增大接触面积,加快反应速率;不变;6; 4;7; 4; 8;
(2)①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=-l59.5kJ•mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)△H=-160.5kJ•mol-1
③H2O(l)=H2O(g)△H=+44.0kJ•mol-1
依据热化学方程式和盖斯定律计算①+②+③得到CO2与NH3合成尿素和气态水的热化学反应方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-276.0KJ/mol;
故答案为:2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(g)△H=-276.0 KJ/mol;
(3)a.反应前后气体反应物和生成物的系数和不等,正反应是体积减小的方向,在恒温恒容条件下,压强不变是平衡状态,故a正确;b.伴随反应的进行,CO2与NH3的速率之比始终为1:2,无法判断是平衡状态,故b错误;c.NH2CO2NH4(s)质量保持不变可说明是平衡状态,故c正确;d.反应在恒温条件下进行,无法判断是平衡状态,故d错误;
2NH3+CO2⇌NH2CO2NH4,
起始量(mol/L) 0.2 0.1 0
变化量(mol/L) 0.1 0.05 0
平衡量(mol/L) 0.1 0.05 0
CO2的转化率=
| 消耗量 |
| 起始量 |
| 0.05mpl/l |
| 0.1mol/l |
改变NH2CO2NH4(s)质量平衡不移动,CO2的转化率不变;
故答案为:ac;50%;不变;
(4)电解NO制备NH4NO3,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总电极反应方程式为:8NO+7H2
| ||
故答案为:8NO+2NH3+7H2O=5NH4NO3.
看了NO2是形成雾霾天气的原因之一...的网友还看了以下:
不要说数太小可忽略物理书中说在真空中不同质量物体从同一高度下落是同时落地,但我绝的是错了,依据万有 2020-04-25 …
传统的熨斗用高温的底板直接压烫熨斗衣物,一不小心就会将衣物烫坏.现在大多采用蒸汽熨斗,使用时它会通 2020-05-16 …
关于火箭反冲问题在一般计算中,火箭在飞行期间,发动机不断喷出燃气流,火箭的质量不断发生变化,是一个 2020-06-02 …
事物是否分层次...就好似物质可分为化合物和单质而单质又可分为金属单质和非金属单质听不懂不要喷口水 2020-06-06 …
为了提高某种农作物的产量,农场通常采用喷施药物的方法控制其高度.已知该农作物的平均高度y(米)与每 2020-06-11 …
"每每听到,先是猝不及防,随之便捧腹,或忍不住喷饭,且不能忘."中的“捧腹”和“喷饭”是指什么?" 2020-06-23 …
物理简答题急传统的熨斗用高温的底板直接压烫衣物,一不小心就会将衣物烫坏,现在大多采用蒸汽式熨斗,使 2020-06-24 …
物理学家把由反粒子组成的物质称作反物质。1928年英国物理学家狄拉克预言反物质的存在。1997年美国 2020-11-05 …
某植物正常授粉形成幼果后,用较高浓度的生长素类似物喷洒幼果,可能出现的是A.种某植物正常授粉形成幼果 2020-11-22 …
由不同的物质组成的两物体,若体积相同,其质量与密度成.即密度的物体质量大.密度的物体质量小在帮我解决 2021-02-20 …