早教吧作业答案频道 -->化学-->
常温下,铜与稀硫酸几乎不反应,但在一定温度下,铜与浓硫酸反应生成硫酸铜、水和一种气体.小明很好奇,设计如下实验探究铜丝与浓硫酸反应后的产物.提出问题生成的气体是什
题目详情
常温下,铜与稀硫酸几乎不反应,但在一定温度下,铜与浓硫酸反应生成硫酸铜、水和一种气体.小明很好奇,设计如下实验探究铜丝与浓硫酸反应后的产物.
【提出问题】生成的气体是什么?
【查阅资料】SO2能使品红溶液褪色;硫酸铜固体为白色,硫酸铜溶液为蓝色.
【猜想与假设】猜想一:氢气;猜想二:___.
【设计实验】如图所示
【实验结论】该反应的化学方程式为:___,该气体可以用___来吸收以防止大气污染.
【反思与评价】
(1)铜丝可以上下抽动的作用是___.
(2)试管中出现白色固体的原因是___.
某研究小组利用如图装置探究铜与浓硫酸反应的产物.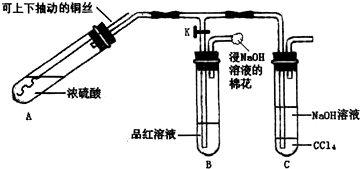
实验步骤与现象如下:
①检查装置气密性,向A中加入5mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K.
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热.回答下列问题:
(1)溶液中白色固体是___ (填化学式),C中CCl4的作用是___.
(2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝.写出A中可能发生反应的化学方程式:___、___.
(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生.
①分离的操作名称为:___:
②白色沉淀为:___;
③产生白色沉淀的原因可能是___.
【提出问题】生成的气体是什么?
【查阅资料】SO2能使品红溶液褪色;硫酸铜固体为白色,硫酸铜溶液为蓝色.
【猜想与假设】猜想一:氢气;猜想二:___.
【设计实验】如图所示
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 向试管中加入5mL浓硫酸,将铜丝伸入浓硫酸中,给试管加热. | 有白色固体出现,产生气泡 | |
| 2 | 用燃着的木条引燃产生的气体 | 未听见爆鸣声 | 猜想一 ___. (填“成立”或“不成立”) |
| 3 | 猜想二成立 |
【反思与评价】
(1)铜丝可以上下抽动的作用是___.
(2)试管中出现白色固体的原因是___.
某研究小组利用如图装置探究铜与浓硫酸反应的产物.

实验步骤与现象如下:
①检查装置气密性,向A中加入5mL浓硫酸,打开K,将铜丝伸入浓硫酸中,给A处加热,观察到B中品红溶液褪色,再关闭K.
②实验观察到A中液面下铜丝变黑,产生气泡,液面上方产生大量白雾,一段时间后溶液中有白色固体出现,拉出铜丝,停止加热.回答下列问题:
(1)溶液中白色固体是___ (填化学式),C中CCl4的作用是___.
(2)取出铜丝,用蒸馏水洗净后伸入到稀硫酸中,铜丝变亮、溶液变蓝.写出A中可能发生反应的化学方程式:___、___.
(3)分离出C中的上层液体,滴加过量稀盐酸和BaCl2溶液,有白色沉淀产生.
①分离的操作名称为:___:
②白色沉淀为:___;
③产生白色沉淀的原因可能是___.
▼优质解答
答案和解析
【猜想与假设】依据质量守恒定律,化学反应前后元素种类不变,所以猜想二是二氧化硫;
【设计实验】氢气具有可燃性,点燃会发生爆鸣声,所以
【实验结论】浓硫酸和铜在加热的条件下生成硫酸铜、水和二氧化硫,化学方程式为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,氢氧化钠会与二氧化硫反应,所以该气体能用氢氧化钠溶液来吸收以防止大气污染;
【反思与评价】(1)通过铜丝的上下抽动,可以控制反应的发生和停止;
(2)铜和浓硫酸反应生成硫酸铜,在加热的条件下,导致容器内的溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜;
(1)铜和浓硫酸反应生成硫酸铜,在加热的条件下,导致容器内的溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜,二氧化硫难溶于四氯化碳,可以防止倒吸;
(2)浓硫酸和铜在加热的条件下生成硫酸铜、水和二氧化硫,铜和浓硫酸在加热的条件下生成氧化铜、水和二氧化硫,化学方程式为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑、Cu+H2SO4(浓)
CuO+H2O+SO2↑;
(3)①两种互不相溶的液体采用分液的方法分离,所以分离出C中的上层液体,采用分液的方法分离;
②氯化钡和亚硫酸钠反应生成亚硫酸钡,亚硫酸钡和稀盐酸反应生成氯化钡、水和二氧化硫,滴入过量的稀盐酸和氯化钡,有白色沉淀生成,说明沉淀是硫酸钡沉淀;
③亚硫酸钡能被氧气氧化成硫酸钡沉淀,硫酸钡与盐酸不反应.
故答案为:【猜想与假设】二氧化硫;
【设计实验】氢气具有可燃性,点燃会发生爆鸣声,所以
【实验结论】Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,氢氧化钠溶液;
【反思与评价】(1)便于控制反应的发生和停止;
(2)有无水硫酸铜固体析出;
(1)无水CuSO4,防止倒吸;
(2)Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑、Cu+H2SO4(浓)
CuO+H2O+SO2↑;
(3)①分液;
②硫酸钡;
③装置中的氧气参加了反应.
【设计实验】氢气具有可燃性,点燃会发生爆鸣声,所以
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 向试管中加入5mL浓硫酸,将铜丝伸入浓硫酸中,给试管加热. | 有白色固体出现,产生气泡 | |
| 2 | 用燃着的木条引燃产生的气体 | 未听见爆鸣声 | 猜想一 不成立 |
| 3 | 猜想二成立 |
| ||
【反思与评价】(1)通过铜丝的上下抽动,可以控制反应的发生和停止;
(2)铜和浓硫酸反应生成硫酸铜,在加热的条件下,导致容器内的溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜;
(1)铜和浓硫酸反应生成硫酸铜,在加热的条件下,导致容器内的溶剂减少,且浓硫酸具有吸水性,所以会析出白色固体硫酸铜,二氧化硫难溶于四氯化碳,可以防止倒吸;
(2)浓硫酸和铜在加热的条件下生成硫酸铜、水和二氧化硫,铜和浓硫酸在加热的条件下生成氧化铜、水和二氧化硫,化学方程式为:Cu+2H2SO4(浓)
| ||
| ||
(3)①两种互不相溶的液体采用分液的方法分离,所以分离出C中的上层液体,采用分液的方法分离;
②氯化钡和亚硫酸钠反应生成亚硫酸钡,亚硫酸钡和稀盐酸反应生成氯化钡、水和二氧化硫,滴入过量的稀盐酸和氯化钡,有白色沉淀生成,说明沉淀是硫酸钡沉淀;
③亚硫酸钡能被氧气氧化成硫酸钡沉淀,硫酸钡与盐酸不反应.
故答案为:【猜想与假设】二氧化硫;
【设计实验】氢气具有可燃性,点燃会发生爆鸣声,所以
| 步骤 | 实验操作 | 实验现象 | 实验结论 |
| 1 | 向试管中加入5mL浓硫酸,将铜丝伸入浓硫酸中,给试管加热. | 有白色固体出现,产生气泡 | |
| 2 | 用燃着的木条引燃产生的气体 | 未听见爆鸣声 | 猜想一不成立 |
| 3 | 猜想二成立 |
| ||
【反思与评价】(1)便于控制反应的发生和停止;
(2)有无水硫酸铜固体析出;
(1)无水CuSO4,防止倒吸;
(2)Cu+2H2SO4(浓)
| ||
| ||
(3)①分液;
②硫酸钡;
③装置中的氧气参加了反应.
看了常温下,铜与稀硫酸几乎不反应,...的网友还看了以下:
构建知识网络,可以帮助我们理解知识间的内在联系.如图是盐酸与不同类别物质之间反应的知识网络.(1) 2020-05-13 …
一元二次方程问题1、若二次根式√-4^2+12x-9有意义,则x的取值范围是2、写出一个两根互为倒 2020-05-14 …
醋酸菌对氧气的含量特别敏感,即使是短时间处于无氧环境中,也会引起醋酸菌的死亡,根据这一事实可以得出 2020-05-14 …
英语翻译1:我需要想出一个好主意2:我们必须在英语课堂上写下这生单词3:他在2008年开办了一家公 2020-05-20 …
一个人行走,6分钟有车从身后过,2分钟从前面开来,人车速度均匀,问几分钟开出一辆车需要过程,谢谢了 2020-06-15 …
“一带一路”铸就辉煌新闻视角,央视新闻联播从2015年4月4日起推出系列报道《一带一路共建繁荣》第 2020-06-25 …
为什么化肥中磷酸一铵有效磷是44%我是说在复混肥配方中,如果用磷酸一铵作为原料之一的话,一般磷酸一 2020-07-02 …
请数学高手回答,要一元一次方程某学校组织学生到100千米外的地方夏令营,汽车只能坐一半的人,另一半 2020-08-03 …
帮个忙猜下字谜啦一点一横长,一撇向西方,并排两棵树,栽在石头上.()左看马靠它,右看它靠马,两边一起 2020-11-07 …
1.根据酸能电离出的氢离子的数目可将酸分为一元酸{如HCL},二元酸{如H2CO3},三元酸如{H3 2020-11-17 …