早教吧作业答案频道 -->化学-->
氮元素可形成多种金属氮化物,如氮化钠(Na3N)、氮化镁(Mg3N2)和叠氮化钠(NaN3)等.(1)下列说法正确的是.A.氮元素的电负性较大,因此常温下氮气很稳定B.第一电离能:N>O&g
题目详情
氮元素可形成多种金属氮化物,如氮化钠(Na3N)、氮化镁(Mg3N2)和叠氮化钠(NaN3)等.
(1)下列说法正确的是___.
A.氮元素的电负性较大,因此常温下氮气很稳定
B.第一电离能:N>O>Mg>Na
C.NH3分子间有氢键,因此热稳定性NH3强于PH3
D.Mg3N2与NaN3结构类似,与水作用可产生NH3
(2)氮化镁是离子化合物,与水作用可产生NH3.
①写出氮离子的核外电子排布式:___;
②Mg3N2与足量盐酸充分反应后,含氮的产物1mol中,含共价键___mol;
(3)叠氮化钠(NaN3)受到撞击可分解产生大量的N2,可应用于汽车的安全气囊,制取叠氮化钠的方法如下:
Ⅰ.金属钠与液态氨反应得NaNH2;
Ⅱ.NaNH2和N2O按物质的量之比为2:1反应可生成NaN3,NaOH和一种气体X.
①X的等电子体有多种,写出一种属于阳离子的等电子体:___;
②NH
中氮原子的杂化方式为___,NH
的立体构型是___;
③NH
和NH3中,键角∠HNH的大小:NH
___(填“大于”“小于”或“等于“)NH3.
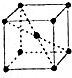
(4)金属钠的晶胞为提心立方堆积,其晶胞示意图如图所示:
①该晶胞中钠原子的配位数为___;
②实验测得钠的密度为ρg/cm3,用NA表示阿伏加德罗常数,则钠原子的半径为___cm.

(1)下列说法正确的是___.
A.氮元素的电负性较大,因此常温下氮气很稳定
B.第一电离能:N>O>Mg>Na
C.NH3分子间有氢键,因此热稳定性NH3强于PH3
D.Mg3N2与NaN3结构类似,与水作用可产生NH3
(2)氮化镁是离子化合物,与水作用可产生NH3.
①写出氮离子的核外电子排布式:___;
②Mg3N2与足量盐酸充分反应后,含氮的产物1mol中,含共价键___mol;
(3)叠氮化钠(NaN3)受到撞击可分解产生大量的N2,可应用于汽车的安全气囊,制取叠氮化钠的方法如下:
Ⅰ.金属钠与液态氨反应得NaNH2;
Ⅱ.NaNH2和N2O按物质的量之比为2:1反应可生成NaN3,NaOH和一种气体X.
①X的等电子体有多种,写出一种属于阳离子的等电子体:___;
②NH
| - 2 |
| - 2 |
③NH
| - 2 |
| - 2 |
(4)金属钠的晶胞为提心立方堆积,其晶胞示意图如图所示:
①该晶胞中钠原子的配位数为___;
②实验测得钠的密度为ρg/cm3,用NA表示阿伏加德罗常数,则钠原子的半径为___cm.
▼优质解答
答案和解析
(1)A.氮气常温下很稳定,是因为分子中含有氮氮三键,键能较大,与N元素电负性无关,故A错误;B.Mg元素原子3s能级为全满稳定状态、N元素原子2p能级为半满稳定状态,第一电离能高于同周期相邻元素的,非金属性越强...
看了氮元素可形成多种金属氮化物,如...的网友还看了以下:
我国是世界上大江大河众多的国家之一.据此回答5--8题.下列对长江流域开发利用的方式,合理的是() 2020-05-13 …
几道汉译英,这是如此冷的一个天(it)以至于我穿了大衣(sothat)(suchthat)两个句子 2020-06-06 …
下列句子中,加点词语使用不正确的一项是()A.那天我经过母校,发现原来的平房已经销声匿迹,新的校舍 2020-06-12 …
右图为大豆种子纵剖图,据图回答:(1)填出下列番号所代表的结构名称.a;b;d;e.(2)如果此大 2020-06-21 …
2009年秋冬之交,全球爆发了大规模甲型流感,在全社会人民的共同努力下,此病得到了有效的控制.(1 2020-06-23 …
写出下面句子的修辞手法1、他摘下毡帽,头上冒着热气,是一股白色的烟.()2、骆驼真沉得住气.()3 2020-06-29 …
下面是大气对地面的保温作用示意图,据此回答(1)~(3)题:下面是大气对地面的保温作用示意图,据此 2020-07-05 …
一物体恰能在一个斜面体上沿斜面匀速下滑,可以证明此时斜面不受地面的摩擦力作用,若沿斜面方向用力向下推 2020-11-03 …
食堂大米的总质量和所用的天数的关系如下表所用天数12345大米的总质量(千克)10020030040 2020-11-06 …
1982年上海市委和市出版局作出决定,委托上海书店以影印的方式保存并出版全套《申报》.之所以下如此大 2020-12-16 …